Загальні хімічні властивості амінокислот, які визначаються властивостями карбоксильної і аміногруп
Властивості карбоксильної групи
Як і всі інші сполуки, що містять карбоксильну групу, амінокислоти при взаємодії з основами утворюють солі, а в результаті реакцій із спиртами і амінами утворюють, відповідно, ефіри і аміди.
Важливу роль в біохімії відіграє реакція декарбоксилування амінокислот, в результаті якої карбоксильна група зникає і залишається тільки аміногрупа:
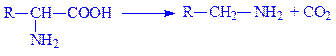
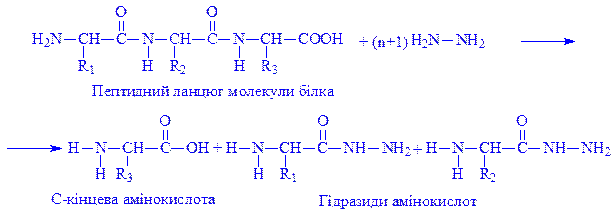
Методи визначення С-кінцевих амінокислот.Для вивчення С-кінцевих амінокислот часто використовують метод гідразинолізу, розроблений японським ученим Ф. Акабборі, який грунтується на гідролізі поліпептидного ланцюга білкової молекули гідразином. При цьому С-кінцева амінокислота відщеплюється у вільному стані, а всі інші амінокислоти – у вигляді сполук з гідразином:
Гідролізат потім обробляють 2,4-динітрофторбензолом, у результаті чого гідразиди перетворюються на ДНФ-гідразиди, а С-кінцева амінокислота – на ДНФ-амінокислоту (див. нижче).
Після цього ДНФ-гідразиди екстракцією (оцтово-етиловим ефіром) відділяють від ДНФ-амінокислот.
Для визначення С-кінцевої амінокислоти застосовують також ферментативний метод, використовуючи панкреатичні карбоксипептидази.
Так, карбоксипептидаза А відщеплює від білка або пептиду лише той амінокислотний залишок, який має вільну карбоксильну групу.
Інформацію про послідовність С-кінцевих амінокислот у ланцюгу можна отримати під час визначення швидкості відщеплення кожного наступного С-кінцевого залишку амінокислоти. Необхідно відзначити, що карбоксипептидаза А малоактивна до залишків С-кінцевих амінокислот лізину, аргініну і проліну. Тому залишки цих амінокислот досліджують з використанням карбоксипептидази В.
Властивості аміногрупи
Як і всі сполуки, що містять аміногрупу, амінокислоти взаємодіють з кислотами, утворюючи солі.
Відділення аміногрупи від амінокислоти може бути здійснено багатьма способами. Найважливіший з них – окислювальне дезамінування:
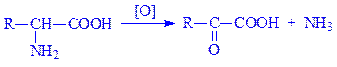
Аміногрупа вступає в реакцію приєднання з формаліном:
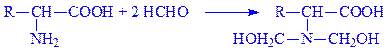
Інтерес до цієї реакції обумовлений тим, що вона призводить до блокування амінної функції амінокислоти. Сполука, що утворюється, володіє тільки кислотними властивостями і її кількісне визначення можна здійснити простою нейтралізацією лугом (формалінове титрування по Серенсену).
Наведені нижче реакції широко використовуються при дослідженні будови білків.
