Аминоацил-тРНК синтетазы (аминоацил-тРНК лигазы)
Основные компоненты белоксинтезирующей системы
| Необходимые компоненты | Функции |
| 1 . Аминокислоты | Субстраты для синтеза белков |
| 2. тРНК | тРНК выполняют функцию адаптеров. Они акцепторным концом взаимодействуют с аминокислотами, а антикодоном - с кодоном мРНК. |
| 3. Аминоацил-тРНК синтетазы | Каждая аа-тРНК-синтетаза катализирует реакцию специфического связывания одной из 20 аминокислот с соответствующей тРНК |
| 4.мРНК | Матрица содержит линейную последовательность кодонов, определяющих первичную структуру белков |
| 5. Рибосомы | Рибонуклеопротеиновые субклеточные структуры, являющиеся местом синтеза белков |
| 6. АТФ, ГТФ | Источники энергии |
| 7. Белковые факторы инициации, элонгации, терминации | Специфические внерибосомные белки, необходимые для процесса трансляции (12 факторов инициации: elF; 2 фактора элонгации: eEFl, eEF2, и факторы терминации: eRF) |
| 8. Ионы магния | Кофактор, стабилизирующий структуру рибосом |
Основные компоненты белоксинтезирующей системы
Как видно из табл. 4- 3 , для синтеза полипептидной цепи необходимо большое количество компонентов, совместное и согласованное взаимодействие которых приводит к образованию белка.
Аминокислоты
Все 20 аминокислот, входящих в структуру белков организма человека , должны присутствовать в достаточном количестве . Это требование прежде всего относится к незаменимым (т.е. не синтезирующимся в организме) аминокислотам, так как недостаточное снабжение клетки хотя бы одной незаменимой аминокислотой приводит к снижению, а иногда и полной остановке синтеза белка на кодоне, требующем включения этой аминокислоты в белок.
мРНК.Содержит информацию о структуре синтезируемого белка и используется в качестве матрицы.
тРНК.У человека около 50 различных тРНК обеспечивают включение аминокислот в белок. тРНК называют " адапторные молекулы",так как к акцепторному концу этих молекул может быть присоединена определённая аминокислота, а с помощью антикодона они узнают специфический кодон на мРНК. В процессе синтеза белка на рибосоме связывание антикодонов тРНК с кодонами мРНК происходит по принципу комплементарности и антипараллельности.
| Антикодон тРНКАрг | (3')- G-С-С -(5') |
| Кодоны Apr: | (5')-C-G-G-(3') |
Однако оказалось, что число тРНК для каждой аминокислоты не совпадает с числом кодирующих её кодонов в мРНК, и, следовательно, некоторые тРНК способны связываться больше чем с одним кодоном.
Исследование этого вопроса позволило установить следующее:
- первые два основания кодона и последние два основания антикодона образуют обычные прочные пары (гуанинцитозин и аденинурацил) и вносят наибольший вклад в специфичность декодирования;
- связывание третьего основания кодона с первым основанием антикодона происходит слабее, чем с первыми двумя, и это позволяет некоторым тРНК прочитывать больше чем один кодон.
Гипотеза, объясняющая характер кодонан-тикодонового взаимодействия, получила название"гипотезы качания"(т.е. третье основание большинства кодонов имеет определённую степень свободы при образовании пары с соответствующим антикодоном и как бы "качается").
Так, например, одна из аргининовых тРНК имеет антикодон 5'-I-C-G-3', который может узнавать 3 разных аргининовых кодона:
| Антикодон | (3')-G-C-I-(5') | (3')-G-C-I- | (3')-G-C-I- |
| Кодоны | (3)-С-G-А-(3') | (5')-C-G-U- | (5')-C-G-C- |
Аминоацил-тРНК синтетазы (аминоацил-тРНК лигазы)
В цитозоле клеток 20 различных аминокислот присоединяются α-карбоксильной группой к 3'-гидроксильному акцепторному концу соответствующих тРНК с образованием сложноэфирной связи. Эти реакции катализирует семейство ферментов, носящее название аминоацил-тРНК синтетаз (аа-тРНК-синтетаз). Каждый член этого семейства узнаёт только одну определённую аминокислоту и те тРНК, которые способны связываться с этой аминокислотой. Из этого следует, что в группу тРНК синтетаз входит 20 различных ферментов. Они осуществляют активацию аминокислот в 2 стадии: на первой стадии аминокислота присоединяется к ферменту и реагирует с АТФ с образованием богатого энергией промежуточного соединения - аминоацил-АМФ. На второй стадии аминоацильный остаток аминоациладенилата, оставаясь связанным с ферментом, взаимодействует с молекулой соответствующей тРНК с образованием аминоацил-тРНК (рис. 4-36).
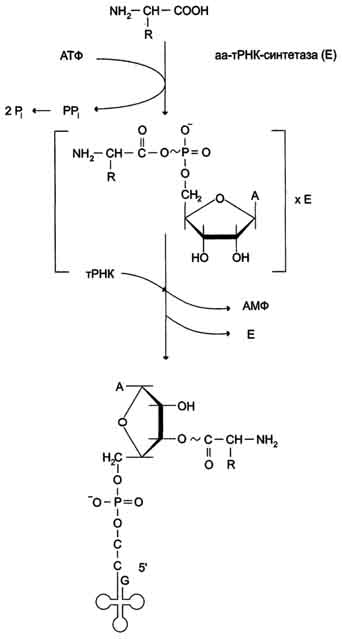
Рис. 4-36. Образование аминоацил-тРНК. Аминокислота взаимодействует с АТФ и активируется, образуя аминоациладенилат, который, не освобождаясь из связи с ферментом (Е), отдаёт активированную аминокислоту тРНК с образованием аминоацил-тРНК (аа-тРНК).
Суммарную реакцию, катализируемую аминоацил-тРНК синтетазами в присутствии ионов Mg2+, можно представить следующим образом:
Аминокислота +тРНК + АТФ -" аминоацил - тРНК + АМФ + PPi.
Для каждой аминокислоты существует свой фермент - своя аминоацил тРНК синтетаза: для глутамата - глутамил-тРНК синтетаза, гистидина - гистидил-тРНК синтетаза и т.д.
Аминокислоты присоединяются к 3'- или 2'-ОН группам рибозы на 3'-конце тРНК, где все тРНК имеют общую нуклеотидную последовательность -ССА.
Энергия, заключённая в макроэргической сложноэфирной связи аминоацил-тРНК, впоследствии используется на образование пептидной связи в ходе синтеза белка.
Пирофосфат, выделяющийся в ходе этой реакции, гидролитически расщепляется с образованием двух молекул ортофосфата и выделением энергии, что делает реакцию активации аминокислот необратимой.
Чрезвычайно высокая специфичность аа-тРНК синтетаз в связывании аминокислоты с соответствующими тРНК лежит в основе точности трансляции генетической информации. В активном центре этих ферментов есть 4 специфических участка для узнавания: аминокислоты, тРНК, АТФ и четвёртый - для присоединения молекулы Н2О, которая участвует в гидролизе неправильных аминоациладенилатов. За счёт существования в активном центре этих ферментов корректирующего механизма, обеспечивающего немедленное удаление ошибочно присоединённого аминокислотного остатка, достигается поразительно высокая точность работы: на 1300 связанных с тРНК аминокислот встречается только одна ошибка.
Аминокислота, присоединяясь к тРНК, в дальнейшем не определяет специфических свойств аа-тРНК, так как её структуру не узнаёт ни рибосома, ни мРНК. Участие в синтезе белка зависит только от структуры тРНК, а точнее, от комплементарного взаимодействия антикодона аминоацил-тРНК с кодоном мРНК.
Антикодон расположен в центральной (антикодоновой) петле тРНК. Узнавание тРНК аа-тРНК синтетазами не всегда происходит по антикодоновой петле. Активный центр некоторых ферментов обнаруживает комплементарное соответствие другим участкам пространственной структуры тРНК.
Рибосомы
Рибосомы представляют собой рибонуклео-протеиновые образования - своеобразные "фабрики", на которых идёт сборка аминокислот в белки. Эукариотические рибосомы имеют константу седиментации 80S и состоят из 40S (малой) и 60S (большой) субъединиц. Каждая субъединица включает рРНК и белки. В 40S субъединицу входит рРНК с константой седиментации 18S и около 30-40 белков . В 60S субъединице обнаружено 3 вида рРНК: 5S, 5,8S и 28S и около 50 различных белков.
Белки входят в состав субъединиц рибосомы в количестве одной копии и выполняют структурную функцию, обеспечивая взаимодействие между мРНК и тРНК, связанными с аминокислотой или пептидом.
В присутствии мРНК 40S и 60S субъединицы объединяются с образованием полной рибосомы, масса которой примерно в 650 раз больше массы молекулы гемоглобина.
В рибосоме есть 2 центра для присоединения молекул тРНК: аминоацильный ( А ) и пептидильный (Р) центры, в образовании которых участвуют обе субъединицы. Вместе центры А и Р включают участок мРНК, равный 2 кодонам. В ходе трансляции центр А связывает аа-тРНК, строение которой определяет кодон , находящийся в области этого центра. В структуре этого кодона зашифрована природа аминокислоты, которая будет включена в растущую полипептидную цепь. Центр Р занимает пептидил-тРНК, т.е. тРНК, связанная с пептидной цепочкой, которая уже синтезирована.
У эукариотов различают рибосомы 2 типов: "свободные", обнаруживаемые в цитоплазме клеток, и связанные с эндоплазматическим ретикулумом (ЭР). Рибосомы, ассоциированные с ЭР, ответственны за синтез белков "на экспорт", которые выходят в плазму крови и участвуют в обновлении белков ЭР, мембраны аппарата Гольджи, митохондрий или лизосом.
Митохондрии содержат свой набор рибосом. Митохондриальные рибосомы мельче, чем рибосомы эукариотов, прокариотов и имеют константу седиментации 55S. Они также состоят из двух субъединиц, но отличаются от эукариотических рибосом количеством и составом рРНК и белков.
Белковые факторы
В каждой стадии белкового синтеза на рибосоме: инициации, элонгации и терминации участвует разный набор внерибосомных белковых
факторов. Эти белки связываются с рибосомой или её субъединицами на определённых стадиях процесса и стабилизируют или облегчают функционирование белоксинтезирующей машины.
