Ингибиторы биосинтеза белка
на стадии репликации
Антимицин Д – встраивается в молекулу ДНК и блокирует синтез новой ДНК;
Новобиацин – ингибирует ДНК-гиразу (топоизомеразу);
на стадии транскрипции
Рифамицин – блокирует РНК-полимеразу;
на стадии трансляции
Тетрациклин, левомицетин – связывают либо малую, либо большую субъединицу рибосомы и тем самым блокируют синтез белка;
Пенициллин – блокирует синтез белков, входящих в оболочку микроорганизмов.
Посттрансляционная модификация белков
Многие синтезированные белки в последующем подвергаются посттрансляционной модификации.
· частичный протеолиз – отщепление «ненужных» участков
(профермент→фермент; прогормон→гормон);
· модификация отдельных аминокислот:
· окисление (пролин→гидроксипролин в коллагене);
· фосфолирирование (присоединение фосфата);
· гликозилирование (присоединение углевода);
· карбоксилирование (присоединение группы СООН в некоторых факторах свёртывания крови);
· присоединение простетической группы;
· замыкание дисульфидных мостиков;
· изменение олигомерности белка (объединение нескольких мономеров).
В посттрансляционной модификации белков играют важную роль белки - шапероны (они «следят» за правильностью модификации).
Билет 28
1.Транспортные формы липидов крови
Гидрофобные липиды не могут транспортироваться кровью самостоятельно. Они переносятся в следующих формах:
1. липопротеиды (липопротеины) – белково-липидные комплексы;
2. хиломикроны –липидные капли, образующиеся в млечном соке;
3. свободные жирные кислоты транспортируются в комплекте с альбуминами.
Хиломикроны - это мельчайшие капельки липида с размерами около 500 нм, плотностью 0,95 г/см3, состоящие из 2% белка и 90% ТАГ. Хиломикроны синтезируются в слизистой кишечника, считаются транспортной формой пищевых (экзогенных) липидов в организме. Хиломикроны попадают сначала в лимфу, а затем разносятся кровью в основном в жировые депо (>50%), а также в печень, лёгкие, мышечную ткань.
Липопротеиды (ЛП) являются основной транспортной формой липидов.
По электрофоретической подвижности различают: пре β - ЛП, β - ЛП, α - ЛП
По плотности выделяют:
- ЛП очень низкой плотности (ЛПОНП);
- ЛП низкой плотности (ЛПНП);
- ЛП высокой плотности (ЛПВП);
- ЛП промежуточной плотности;
- ЛП очень высокой плотности.
Все ЛП построены по общему принципу. В центре частицы находится гидрофобное ядро, в которое входят ТАГ и эфиры холестерина (Эх), вокруг него формируется гидрофильная оболочка, в которую входят фосфолипиды (ФЛ), холестерин (Х-ОН). На поверхности располагаются белки - апопротеины (АроPt).
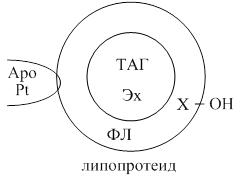
Различают несколько видов АроPt: A, B, C, E. Они формируют структуру липопротеидных частиц, взаимодействуют с тканевыми рецепторами к ЛП, являются активаторами ферментов обмена ЛП.
ЛП осуществляют транспорт липидов, жирорастворимых витаминов и гидрофобных гормонов.
Закономерности строения липопротеидов в ряду: ЛПОНП →ЛПНП→ЛПВП представлены в таблице.
ЛПОНП – синтезируется в печени, считаются основной транспортной формой эндогенных липидов. В эндотелии сосудов ЛПОНП и хиломикроны подвергаются действию фермента липопротеидной липазы, которая расщепляет в их составе ТАГ. В результате в составе ЛП повышается доля холестерина, и ЛПОНП превращаются в ЛПНП.
ЛПНП считаются транспортной формой холестерина от печени к органам и тканям. В тканях имеются рецепторы к ЛПНП, при участии которых происходит поглощение холестерина с последующим использованием его на построение мембран, синтез стероидов, депонированием в виде эфиров.
ЛПВП синтезируется в печени в виде дисковидных структур. Они считается транспортной формой холестерина из тканей к печени.
Большая часть переносимых кровью липидов откладывается в жировых депо, к которым относятся подкожно-жировая клетчатка, большой и малый сальники.В раннем детском возрасте у детей важным видом жировой ткани является бурая жировая ткань. Она локализована в основном на спине, на груди, имеет бурый оттенок, который обусловлен большим содержанием митохондрий и Fе - содержащих цитохромов.
Содержание липидов в крови взрослых:
Общие липиды 4-8 г/л
ТАГ 1-2,5 ммоль/л
ФЛ 2,5-3,0 ммоль/л
Холестерин 3,5-5,2 ммоль/л
Свободные жирные кислоты 0,5 – 1,0 ммоль/л
Гиперлипопротеинемия – это состояние при котором происходит нарушение липидного обмена с увеличением количества жиров в крови, повышается уровень холестеринакак низкой плотности, так и высокой, а также триглицеридов. Это состояние способствует развитию атеросклероза, сердечно-сосудистых заболеваний, гипертонии
Влияние глюкагона на липидный обмен проявляется в активации липаз ,расщепляющих триглицериды с образованием свободных жирных кислот.(ВЫСВОБОЖДАЕТ ЖИР ДЛЯ ЭНЕРГИИ)
Под влиянием инсулина в жировой ткани возрастает количество тириглицеридов. Под влиянием инсулина в крови снижается содержание летучих жирных кислот, которые используются для образования жира в печени и в других тканях. (НАКАПЛИВАЕТ ЖИР)
АДРЕНАЛИН УСИЛИВАЕТ ЛИПОЛИЗ(РАСПАД ЖИРОВ)И ТОРМОЗИТ ИХ СИНТЕЗ
2.Обмен фенилаланина и тирозина и его нарушения
Фенилаланин – незаменимая аминокислота. Основной реакцией превращения фенилаланина в организме является окисление его в тирозин при участи фермента фенилаланингидроксилазы и кофермента тетрагидробиоптерина. При врожденном дефекте данного фермента развивается заболевание фенилкетонурия, при котором фенилаланин переходит в токсичные для ткани мозга соединения фенилпируват, фенилацетат. А возникающий дефицит тирозина блокирует синтез нейромедиаторов. Фенилкетонурия сопровождается развитием слабоумия (фенилпировиноградная олигофрения). 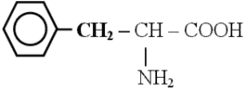
Тирозин – заменимая аминокислота. Она используется на синтез многих важных веществ:
d) синтез тироксина (гормона щитовидной железы);
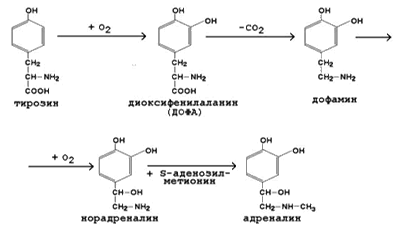
e) путём окисления переходит в диоксифенилаланин (ДОФА), который затем в коже используется для синтеза меланинов, а в эндокринных железах – для синтеза норадреналина, адреналина, дофамина (катехоламины);
f) путём трансаминирования превращается в фумаровую кислоту, которая используется для синтеза углеводов, и в ацетоуксусную кислоту, идущуюна синтез ацетоновых тел.
Окисление тирозина
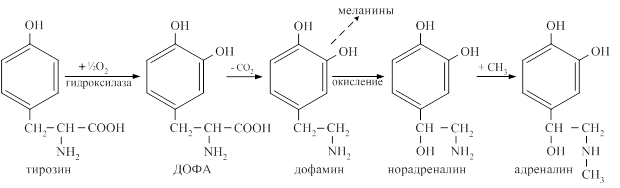
При нарушении активности ферментов синтеза меланинов развивается альбинизм, при котором снижается фотопротекторная, антиоксидантная, иммуномодулирующая функция меланинов.
Трансаминирование тирозина
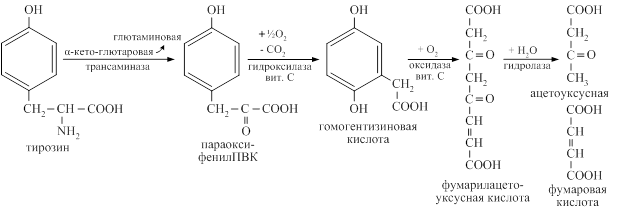
При врожденном дефекте трансаминазы, гидроксилазы, гидролазы развиваются различные виды тирозинозов. При отсутствии оксидазы гомогентизиновой кислоты наблюдается алкатонурия, характеризующаяся повышенным выделением с мочой гомогентизиновой кислоты, которая при контакте с воздухом переходит в продукты тёмного цвета.
Синтез катехоламинов(адр и надпоч),тироксина,меланина
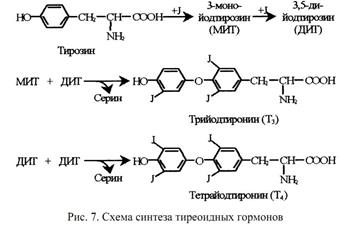 т.е при синтезе тиреоидных гормонов нужно добавить 2 йода
т.е при синтезе тиреоидных гормонов нужно добавить 2 йода
синтез меланина из тирозина:Это происходит за счет активации тирозиназы в меланоцитах, что в свою очередьобусловлено высвобождением эйкозаноидов и эндотелина-1 . 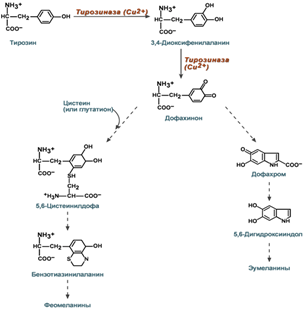
ТРНК
 Транспортные РНК (тРНК) осуществляют транспорт аминокислот на рибосомы, к месту синтеза белка. Молекулярная масса тРНК составляет около 30 000 д. Полинуклеотидная цепь тРНК включает в свой состав 70-80 нуклеотидов. На долю тРНК приходится около 15% всего запаса РНК клетки. В тРНК содержится большое количество минорных нуклеотидов (модифицированные формы обычных оснований). Между комплементарными нуклеотидами участков тРНК возникают водородные связи, и формируется её вторичная структура в виде трилистника (форма «клеверного листа»). В составе тРНК выделяют 2 важных функциональных участка. На средней петле располагается антикодон, комплементарный кодонам иРНК, на открытом конце – акцепторный участок, к которому присоединяется аминокислота. Для переноса каждой аминокислоты в клетках имеется «своя» тРНК.
Транспортные РНК (тРНК) осуществляют транспорт аминокислот на рибосомы, к месту синтеза белка. Молекулярная масса тРНК составляет около 30 000 д. Полинуклеотидная цепь тРНК включает в свой состав 70-80 нуклеотидов. На долю тРНК приходится около 15% всего запаса РНК клетки. В тРНК содержится большое количество минорных нуклеотидов (модифицированные формы обычных оснований). Между комплементарными нуклеотидами участков тРНК возникают водородные связи, и формируется её вторичная структура в виде трилистника (форма «клеверного листа»). В составе тРНК выделяют 2 важных функциональных участка. На средней петле располагается антикодон, комплементарный кодонам иРНК, на открытом конце – акцепторный участок, к которому присоединяется аминокислота. Для переноса каждой аминокислоты в клетках имеется «своя» тРНК.
тРНК имеет 3-ю структуру, которая представляет собой компактное наложение петель друг на друга.
Различают изоакацепторные тРНК, которые переносят одну и ту же аминокислоту, но отличаются структурой и одним нуклеотидом в антикодоне.
В процессе трансляции-На первой подготовительной стадии происходит активация аминокислот и связывание их со «своей» транспортной РНК. В этой стадии участвуют ферменты аминоацил-тРНК-синтетазы. Это специфичные ферменты, обеспечивающие соединение аминокислоты с соответствующей тРНК.Чрезвычайно высокая специфичность аа-тРНК синтетаз в связывании аминокислоты с соответствующими тРНК лежит в основе точности трансляции генетической информации. В активном центре этих ферментов есть 4 специфических участка для узнавания: аминокислоты, тРНК, АТФ и четвёртый - для присоединения молекулы Н2О, за счёт существования в активном центре этих ферментов корректирующего механизма, обеспечивающего немедленное удаление ошибочно присоединённого аминокислотного остатка, достигается поразительно высокая точность работы

Билет 29
