Функционирование малат-аспартатного и глицерофосфатного шунта
Обмен восстановительными эквивалентами между цитозолем и митохондриями может идти в обоих направлениях, определяя пути их переноса между митохондриальным и цитозольным компартментами.
Экспорт НАДН из цитозоля в митохондрии в изолированных гепатоцитах, так же как и в перфузируемой печени, осуществляется помощью трех челночных механизмов — малат-аспартатного и алицерофосфатного шунтов, а также шунта длинноцепочечных жирных кислот, связанного с бета-окислением.
Образуемый в цитозоле гепатоцитов НАДН реоксидируется главным образом во внутренней мембране митохондрий с помощью малат-аспартатного шунта. В результате его активности происходит поступление малата в митохондрии, окисление цитозольного пула НАДН малатдегидрогеназой, трансаминирование внутримитохондриального оксалоацетата аспартатаминотрансферазой, сопровождаемое оттоком аспартата и альфа-кетоглутарата в цитозоль и антипортным поступлением глутамата в митохондрии. Трансаминирование аспартата и альфа-кетоглутарата в цитозоле с регенерацией глутамата и оксалоацетата завершают цикл. Возможности такого механизма обмена восстановительными эквивалентами в гепатоцитах показаны разными исследователями. Ранее считалось, что этот шунт легко обратим за счет того, что трансаминирование, дегидрогенизация и транспорт метаболитов симметричны в двух компартментах клетки. Но тогда трудно объяснить, почему отношение НАДН/НАД+ в митохондриях, водная фаза вторых составляет всего 10% от общего объема клетки, больше, чем в растворимой фазе цитозоля. Это противоречие стало понятным, когда было обнаружено, что аспартат активно транспортируется из митохондрий в обмен на глутамат с сопутствующим переносом одного протона в митохондрии. Движущей силой этого обмена является трансмембранный электрический потенциал, зависящий от функции дыхательной цепи. Это же является причиной того, что поступление аспартата из цитозоля в митохондрии протекает очень медленно, в связи с чем экспорт НАДН из митохондрий в цитозоль с помощью малат-аспартатного шунта практически невозможен.
Вторым существенным механизмом переноса восстановительных эквивалентов в гепатоцитах из цитозоля в митохондрии является альфа-глицерофосфатный шунт. Он не связан с транспортом анионов через плазматическую мембрану, так как роль субстрат-связывающего фактора в этом случае на внешней стороне внутренней мембраны митохондрий выполняет флавиновый фермент альфа-глицерофосфатдегидрогеназа. Его мощность в гепатоцитах составляет примерно 1/3 от мощности малат-аспартатного шунта. Оба эти шунта могут использоваться в гепатоцитах одновременно. Их роль установлена также при инициации глюконеогенеза ксилитолом или сорбитолом в цикле мочевины и при окислении этанола. Во всех этих случаях осуществляется экспорт НАДН из цитозоля в митохондрии.
Импорт НАДН в цитозоль из митохондрий гепатоцитов происходит только в случае глюконеогенеза из пирувата. Он реализуется с помощью малат-пируватного шунта. Оксалоацетат — продукт карбоксилирования пирувата в митохондриях — при физиологических концентрациях транспортируется через митохондриальную мембрану с очень низкой скоростью. Поэтому его отток из митохондрий по кинетическим причинам не может конкурировать со скоростью оттока малата в цитозоль, где из малата снова происходит образование оксалоацетата в малатдегидрогеназной реакции, его последующая конверсия в фосфоенолпируват, а затем в пируват, поступление пирувата в митохондрии и карбоксилирование последнего с восстановлением до малата.
Одно из обязательных звеньев глюконеогенеза — НАД-зависимая реакция. Если предшественником глюконеогенеза является лактат, НАДН в гепатоцитах образуется путем прямой дисмутации лактата в глицеральдегид-3-фосфатдегидрогеназной реакции. Однако в присутствии экзогенного пирувата источником цитозольного АДН является транспорт восстановительных эквивалентов из митохондрий. Малат-аспартатный шунт в таких условиях не может осуществить этот перенос из-за очень низкой скорости транспорта аспартата из цитозоля. Поэтому он реализуется в циклической энергозависимой регенерации пирувата фосфоенолпируваткарбоксилазой и пируваткиназой (на 1 моль образующегося внемитохондриального НАДН потребляется 1 моль АТФ). Если предшественниками глюконеогенеза являются аминокислоты, например аланин, восстановительные эквиваленты не генерируются в цитозоле в дегидрогеназных реакциях. Вместо этого в гепатоцитах осуществляется непрямая их генерация за счет конверсии аспартата в малат в реакции цикла мочевины.
Что касается НАДФН, то в настоящее время достоверно описана лишь одна возможность однонаправленного его экспорта из митохондрий в цитозоль в условиях активации НАДФН-зависимых реакций во внемитохондриальном компартменте при его дефиците в нем (истощение по гликогену, активация системы микросомального окисления). В этом случае используется цитрат-альфа-кетоглутаратный шунт.
Таким образом, регуляция редокс-состояний в двух компартментах осуществляется путем двустороннего обмена НАДФН преимущественно за счет работы челночных механизмов транспорта анионов. Подтверждением этому служат не только ингибиторный анализ и очевидная компартментализация метаболитов, участвующих в работе шунтов, но и высокая способность клетки к перераспределению концентрационных градиентов при изменении направления метаболических потоков.
24.3
Ацетил КоА-важное соединение в обмене веществ, используемое во многих биохимических реакциях. Его главная функция – доставлять атомы углерода с ацетил-группой в цикл трикарбоновых кислот, чтобы те были окислены с выделением энергии. По своей химической структуре ацетил-КоА – тиоэфир между коферментом А (тиолом) и уксусной кислотой (носителем ацильной группы). Ацетил-КоА образуется во время второго шага кислородного клеточного дыхания, декарбоксилирования пирувата, который происходит в матриксе митохондрии. Ацетил-КоА затем поступает в цикл трикарбоновых кислот.
Путь переноса в цитозоль с описание образования ацетил-КоА:
При поступлении глюкозы в клетки она в цитозоле окисляется до пирувата ,пируват проходит через внутреннюю мембрану митохондрий и окисляется в матриксе до ацетил-КоА. Образовавшийся ацетил-КоА конденсируется с оксалоацетатом (ЩУК) с образованием цитрата, а цитрат выходит из митохондрии в цитозоль.
Поступивший в цитозоль цитрат, во-первых, служит источником ацетил-КоА и восстановительных эквивалентов для синтеза высших жирных кислот, а, во-вторых, активирует фермент ацетил-КоА-карбоксилазу, стимулируя тем самым образование малонил-КоА, также не-
обходимого для синтеза высших жирных кислот. В результате при избытке глюкозы в клетке запускается синтез жирных кислот.
Малонил-КоА в свою очередь угнетает перенос высших жирных кислот из цитозоля в матрикс митохондрий, ингибируя активность внешней ацетил-КоА:карнитин-ацилтрансферазы, выключая таким образом окисление высших жирных кислот.
Билет №25
Репликация ДНК
Реплика́ция ДНК — процесс синтеза дочерней молекулы дезоксирибонуклеиновой кислоты на матрице родительской молекулы ДНК. Этот процесс обеспечивает точную передачу генетической информации из поколения в поколение. По имеющимся данным, в репликации ДНК, включающей узнавание точки начала процесса, расплетение родительских цепей ДНК в репликационной вилке, инициацию биосинтеза дочерних цепей и дальнейшую их элонгацию и, наконец, окончание (терминация) процесса, участвует более 40 ферментов и белковых факторов, объединенных в единую ДНК-репликазную систему, называемую реплисомой.
Цепи молекулы ДНК расходятся, образуют репликационную вилку, и каждая из них становится матрицей, на которой синтезируется новая комплементарная цепь. В результате образуются две новые двуспиральные молекулы ДНК, идентичные родительской молекуле.
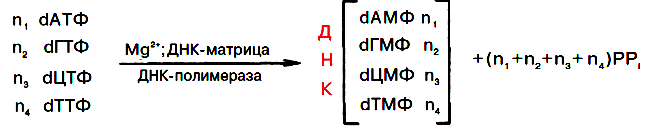
Ферменты хеликазы (расплетают концы), топоизомеразы (раскручивают суперспирализованные витки) и ДНК-связывающие белки расплетают ДНК, удерживают матрицу в разведённом состоянии и вращают молекулу ДНК. Правильность репликации обеспечивается точным соответствием комплементарных пар оснований и активностью ДНК-полимераз, способных распознать и исправить ошибку. Источниками энергии и одновременно с этим субстратами являются dATP, dGTP, dTTP, dCTP. У прокариот выделено три типа ДНК-полимераз. Функцию элонгации выполняет ДНК-полимераза ІІІ. ДНК-полимеразы І и ІІ выполняют репарационные функции. Для затравки (инициации) требуется олигорибонуклеотид, который синтезируется праймазой.
Свойства процесса репликации:
6) матричный — последовательность синтезируемой цепи ДНК однозначно определяется последовательностью материнской цепи в соответствии с принципом комплементарности;
7) полуконсервативный — одна цепь молекулы ДНК, образовавшейся в результате репликации, является вновь синтезированной, а вторая — материнской;
8) идёт в направлении от 5’-конца новой молекулы к 3’-концу;
9) полунепрерывный — одна из цепей ДНК синтезируется непрерывно, а вторая — в виде набора отдельных коротких фрагментов (фрагментов Оказаки);
10) начинается с определённых участков ДНК, которые называются сайтами инициации репликации (англ. origin).
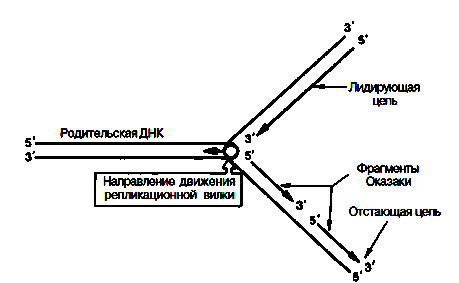
Сложность процесса репликации ДНК объясняется тем, что обе цепи реплицируются одновременно, хотя имеют разное направление (5'–>3' и 3'–>5'); кроме того, рост дочерних цепей также должен происходить в противоположных направлениях. Элонгация каждой дочерней цепи может осуществляться только в направлении 5'–>3'. Р. Оказаки высказал предположение, подтвержденное экспериментальными данными, что синтез одной из дочерних цепей осуществляется непрерывно в одном направлении, в то время как синтез другой дочерней цепи происходит прерывисто, путем соединения коротких фрагментов (в честь автора названы фрагментами Оказаки), в свою очередь синтезирующихся в противоположном направлении.
Как видно, синтез ведущей цепи ДНК идет всегда в направлении 5'–>3', соответствующем направлению движения репликационной вилки. Сохраняя правило синтеза дочерних молекул ДНК 5'–>3', синтез на второй цепи родительской ДНК идет в направлении, противоположном движению репликационной вилки. В зависимости от типа клетки фрагменты Оказаки имеют разные размеры – от нескольких сот до нескольких тысяч нуклеотидов (150–200 у эукариот и 1000–2000 у бактерий).
 Образование каждого фрагмента Оказаки требует наличия короткого затравочного комплементарного праймера – участка РНК, синтез которого катализируется праймазой. Затем при участии ДНК-полимеразы III синтезируются длинные участки ДНК. РНК-затравки далее вырезаются при участии ДНК-полимеразы I, а свободные места их (бреши) замещаются (достраиваются) комплементарными дезоксирибонуклеотидами под действием той же ДНК-полимеразы I; наконец, сшивание разъединенных участков отстающей цепи осуществляется при помощи ДНК-лигаз.
Образование каждого фрагмента Оказаки требует наличия короткого затравочного комплементарного праймера – участка РНК, синтез которого катализируется праймазой. Затем при участии ДНК-полимеразы III синтезируются длинные участки ДНК. РНК-затравки далее вырезаются при участии ДНК-полимеразы I, а свободные места их (бреши) замещаются (достраиваются) комплементарными дезоксирибонуклеотидами под действием той же ДНК-полимеразы I; наконец, сшивание разъединенных участков отстающей цепи осуществляется при помощи ДНК-лигаз.
По имеющимся данным, в репликации ДНК, включающей узнавание точки начала процесса, расплетение родительских цепей ДНК в репликационной вилке, инициацию биосинтеза дочерних цепей и дальнейшую их элонгацию и, наконец, окончание (терминация) процесса, участвует более 40 ферментов и белковых факторов, объединенных в единую ДНК-репликазную систему, называемую реплисомой.Рассмотрим подробнее её компоненты в прокариотической клетке:
Основным ферментом, катализирующим биосинтез новообразованной ДНК (стадию элонгации репликации ДНК), являются ДНК-полимеразы III. Имеются доказательства, что в димерной форме ДНК-полимераза III катализирует сопряженный синтез ведущей (лидирующей) и отстающей цепей ДНК при репликации.
ДНК-полимеразы I катализирует отщепление затравочного олигорибонуклеотидного праймера и заполнение образующихся после этого пробелов (ниш) дезоксирибонуклеотидами. ДНК-полимеразы II из Е. coli выполняет ≪ремонтные≫ функции, исправляя повреждения цепей ДНК.
Функцию раскручивания (расплетения) двойной спирали ДНК в репликационной вилке, происходящего за счет энергии гидролиза АТФ, выполняет специфический rep-белок, названный хеликазой. Образовавшиеся на определенное время одноцепочечные участки ДНК служат в качестве матрицы при репликации и стабилизируются при помощи особых белков, связывающихся с одноцепочечной ДНК (SSB-белки) и препятствующих обратному комплементарному взаимодействию цепей ДНК. В связи с этим их иногда называют дестабилизирующими двойную спираль белками. Имеются, кроме того, особые ферменты топоизомеразы (у прокариот одна из них названа ДНК-гиразой), которые играют особую роль в сверхспирализации, обеспечивая как репликацию, так и транскрипцию ДНК. Эти ферменты наделены способностью не только создавать супервитки, но и уничтожать суперспирализацию путем сшивания образующихся разрывов или разрезания ДНК.
В стадии инициации репликации ДНК участвует специфическая клеточная РНК-полимераза, названная праймазой, которая катализирует синтез короткого олигорибонуклеотида (от 10 до 60 нуклеотидов), т.е. праймера, с которого затем начинается синтез ДНК. В состав праймасомы входит также комплекс белков dna В и dna С, который вблизи репликационной вилки периодически участвует в формировании специфической вторичной структуры ДНК, подходящей для узнавания праймазой.
Важную функцию соединения двух цепей ДНК или замыкания двух концов одной цепи ДНК в процессе репликации либо репарации ДНК выполняют особые ферменты – ДНК-лигаза, катализирующая за счет энергии АТФ образование фосфодиэфирной связи между 3'-ОН-группой дезоксирибозы одной цепи и 5'-фосфатной группой другой цепи ДНК.
25 2 Синтез пальмитиновой кислоты Реакции. Мультиферментный комплекс, называемый синтетазой (синтазой) жирных кислот, состоит из 6 ферментов, связанных с так называемым ацилпереносящим белком (АПБ). Этот белок относительно термостабилен, имеет две свободные HS-группы (цистеина и фосфопантетеинового остатка, присоединенного к ОН-группе серина) и вовлекается в процесс синтеза высших жирных кислот практически на всех его этапах. Мол. масса АПБ составляет около 10000. Данный белок в синтетазной системе выполняет роль КоА. Заметим, что в животных тканях не удалось обнаружить свободного АПБ, подобного микробному. Из печени выделен полиэнзимный комплекс, содержащий все энзимы, необходимые для синтеза жирных кислот. Энзимы комплекса настолько прочно связаны друг с другом, что все попытки изолировать их в индивидуальном виде не увенчались успехом. Приводим последовательность реакций, происходящих при синтезе жирных кислот:
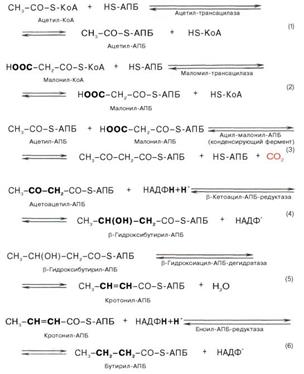
Далее цикл реакций повторяется. Допустим, что идет синтез пальмитиновой кислоты (С16). В этом случае образованием бутирил-АПБ завершается лишь первый из 7 циклов, в каждом из которых началом является присоединение молекулы малонил-АПБ к карбоксильному концу растущей цепи жирной кислоты. При этом отщепляется дистальная карбоксильная группа малонил-АПБ в виде СО2. Например, образовавшийся в первом цикле бутирил-АПБ взаимодействует с малонил-АПБ:

Завершается синтез жирной кислоты отщеплением HS-АПБ от ацил-АПБ под влиянием фермента деацилазы. Например:

Суммарное уравнение синтеза пальмитиновой кислоты можно записать так:
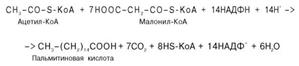
Или, учитывая, что на образование одной молекулы малонил-КоА из ацетил-КоА расходуются одна молекула АТФ и одна молекула СО2, которая затем отщепляется, суммарное уравнение можно представить в следующем виде:

3.Катаболизм аминокислот с разветвленной цепью: лейцина, изолейцина и валина – преимущественно осуществляется не в печени (место распада большинства остальных аминокислот), а в мышечной и жировой тканях, в почках и ткани мозга. Сначала все три аминокислоты подвергаются трансаминированию с α-кетоглутаратом под действием одного общего и специфического фермента – аминотрансферазы аминокислот с разветвленной цепью (КФ 2.6.1.42) (не содержится в печени) с образованием соответствующих α-кетокислот. Последующее окислительное декарбокси-лирование α-кетокислот приводит к образованию ацил-КоА-производных.
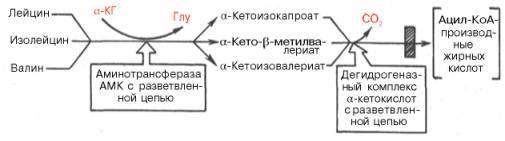
Следует отметить, что фермент, катализирующий окислительное де-карбоксилирование указанных α-кетокислот, высокоспецифичен (по аналогии с пируватдегидрогеназным и α-кетоглутаратдегидрогеназным комплексами) и также нуждается в присутствии всех пяти кофакторов (см. главу 10). Известно наследственное заболевание «болезнь кленового сиропа», при которой нарушено декарбоксилирование указанных α-кетокислот (вследствие синтеза дефектного дегидрогеназного комплекса), что приводит не только к накоплению в крови аминокислот и α-кетокислот, но и к их экскреции с мочой, издающей запах кленового сиропа. Болезнь встречается редко, проявляется обычно в раннем детском возрасте и приводит к нарушению функции мозга и летальному исходу, если не ограничить или полностью не исключить поступление с пищей лейцина, изолейцина и валина.
Пример – лейцин
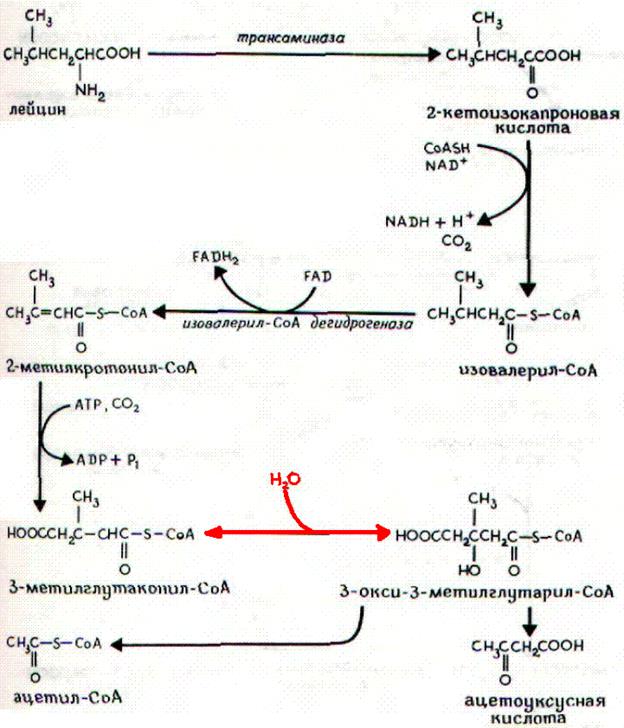
Билет №26
1.Реплика́ция ДНК — процесс синтеза дочерней молекулы дезоксирибонуклеиновой кислоты на матрице родительской молекулы ДНК. В ходе последующего деления материнской клетки каждая дочерняя клетка получает по одной копии молекулы ДНК, которая является идентичной ДНК исходной материнской клетки. Этот процесс обеспечивает точную передачу генетической информации из поколения в поколение. Репликацию ДНК осуществляет сложный ферментный комплекс, состоящий из 15—20 различных белков, называемый реплисомой
УОТСОНА—КРИКА МОДЕЛЬ ДНК, согласно к-рой молекула ДНК состоит из двух антипараллельных полинуклеотидных цепей, образующих правильную правозакрученную перевитую спираль и удерживаемых имеете водородными связями за счёт взаимодействия пар азотистых оснований.
В процессе репликации двойная спираль ДНК, состоящая из двух комплементарных полинуклеотидных цепей, раскручивается на отдельные цепи и одновременно начинается синтез новых полинуклеотидных цепей; при этом исходные цепи ДНК играют роль матриц. Новая цепь, синтезирующаяся на каждой из исходных цепей, идентична др. исходной цепи. Когда процесс завершается, образуются две идентичные двойные спирали, каждая из к-рых состоит из одной старой (исходной) и одной новой цепи. Таким образом от одного поколения к другому передается только одна из двух цепей, составляющих исходную молекулу ДНК,-т. наз. полуконсервативный механизм репликации.
Репликация состоит из большого числа последоват. этапов, к-рые включают узнавание точки началу репликации, расплетание исходного дуплекса (спирали), удержание его цепей в изолированном друг от друга состоянии, инициацию синтеза на них новых дочерних цепей, их рост (элонгацию), закручивание цепей в спираль и терминацию (окончание) синтеза. Все эти этапы репликации, обеспечивает ДНК-репликазная система, или реплисома. Функцион. единица репликации-репликон, представляющий собой сегмент (участок) хромосомы или внехромосомной ДНК, ограниченный точкой начала, в к-рой инициируется репликация, и точкой окончания, в к-рой репликация останавливается. Скорость репликации контролируется на стадии инициации. Эукариотич. хромосомы содержат большое число репликонов, каждый из к-рых также однократно инициируется за один клеточный цикл.
Начиная с точки инициации, репликация осуществляется в ограни-ченной зоне, перемещающейся вдоль исходной спирали ДНК. Эта активная зона репликации (т. наз. репликац. вилка) может двигаться в обоих направлениях. В ходе репликации рост цепи осуществляется благодаря взаимод. дезоксирибонуклеозидтрифосфата с 3'-ОН концевым ну-клеотидом уже построенной части ДНК; при этом отщепляется пирофосфат и образуется фосфодиэфирная связь. Рост полинуклеотидной цепи идет только с ее З'-конца, т. е. в направлении 5' : 3' . Фермент, катализирующий эту р-цию,-ДНК-полиме-раза -не способен начать матричный синтез на одноцепочечной ДНК, если нет хотя бы олигонуклеотидного биспирального участка (т. наз. затравочного олигонуклеотида) комплементарного матрице; затравочным олигонуклеотидом во мн. случаях является не ДНК, а РНК. Энергия, затрачиваемая на образование каждой новой фосфодиэфирной связи в цепи ДНК, обеспечивается расщеплением фосфатной связи между a- и b-фосфатными группами нуклеозидтрифосфата.
ДНК-полимераза имеет один центр связывания нуклеозидтрифосфата, общий для всех четырех нуклеотидов. Выбор из среды нуклеотида, основание к-рого комплементарно очередному основанию матрицы, протекает без ошибок, благодаря определяющему влиянию ДНК-матрицы (исходной цепи ДНК). Репликац. вилка асимметрична. Из двух синтезируемых дочерних цепей ДНК одна строится непрерывно, а другая-с перерывами. Первую наз. ведущей, или лидирующей, цепью, а вторую-отстающей. Синтез второй цепи идет медленнее; хотя в целом эта цепь строится в направлении 3' : 5', каждый из ее фрагментов в отдельности наращивается в направлении 5' : 3'. Благодаря такому прерывистому механизму синтеза, репликация обеих антипараллельных цепей осуществляется с участием одного фермента-ДНК-полимеразы, катализирующего наращивание нуклеотидной цепи только в направлении 5' : 3'.
В качестве затравок для синтеза фрагментов отстающей цепи служат короткие отрезки РНК, комплементарные матричной цепи ДНК. Эти РНК-затравки (праймеры), синтезируются на матрице отстающей цепи из рибонуклеозидтрифосфатов в направлении 5' : 3' с помощью фермента РНК-праймазы. РНК-праймеры затем наращиваются дезоксинуклеотидами с 3'-конца ДНК-поли-меразой, к-рая продолжает наращивание до тех пор, пока строящаяся цепь не достигает РНК-затравки, присоединенной к 5'-концу предыдущего фрагмента. Образующиеся таким образом фрагменты (т. наз. фрагменты Оказаки). Чтобы обеспечить образование непрерывной цепи ДНК из многих таких фрагментов, в действие вступает особая система репарации ДНК, удаляющая РНК-затравку и заменяющая ее на ДНК. Завершает весь процесс фермент ДНК-лигаза, катализирующий образование фосфодиэфирной связи между группой З'-ОН нового фрагмента ДНК и 5'-фосфатной группой предыдущего фрагмента. Образование этой связи требует затраты энергии.
Раскручивание двойной спирали и пространств. разделение цепей осуществляется белками. Геликазы расплетают короткие участки ДНК, находящиеся непосредственно перед репликац. вилкой. На разделение каждой пары оснований расходуется энергия гидролиза двух молекул АТФ до аденозиндифосфата и фосфата. К каждой из разделившихся цепей присоединяется неск. молекул ДНК-связывающих белков, к-рые препятствуют образованию комплементарных пар и обратному воссоединению цепей. Благодаря этому нуклеотидные последовательности цепей ДНК оказываются доступными для репликативной системы. Др. специфич. белки помогают праймазе получить доступ к матрице отстающей цепи. В результате праймаза связывается с ДНК и синтезирует РНК-затравки для фрагментов отстающей цепи. Для формирования новых спира-,лей не требуется ни затрат энергии, ни участия к.-л. "закручивающего" фермента.
2. Глюконеогенез– синтез глюкозы из неуглеводных продуктов. Такими продуктами или метаболитами являются в первую очередь молочная и пи-ровиноградная кислоты, так называемые гликогенные аминокислоты, гли-церол и ряд других соединений. Иными словами, предшественниками глюкозы в глюконеогенезе может быть пируват или любое соединение, превращающееся в процессе катаболизма в пируват или один из промежуточных продуктов цикла трикарбоновых кислот. У позвоночных наиболее интенсивно глюконеогенез протекает в клетках печени и почек (в корковом веществе). Большинство стадий глюконеогенеза представляет собой обращение реакции гликолиза. Только 3 реакции гликолиза (гексокиназная, фосфо-фруктокиназная и пируваткиназная) необратимы, поэтому в процесс глю-конеогенеза на 3 этапах используются другие ферменты. Рассмотрим путь синтеза глюкозы из пирувата.
Образование фосфоенолпирувата из пирувата. Синтез фосфоенолпирувата осуществляется в несколько этапов. Первоначально пируват под влияние пируваткарбоксилазы и при участии СО2 и АТФ карбоксилируется с образованием оксалоацетата:
1 
Первый этап синтеза протекает в митохондриях. Пируват-карбоксилаза, которая катализирует эту реакцию, является аллостери-ческим митохондриальным ферментом. В качестве аллостерического активатора данного фермента необходим ацетил-КоА. Мембрана митохондрий непроницаема для образовавшегося оксалоацетата. Последний здесь же, в митохондриях, восстанавливается в малат:
2 
Реакция протекает при участии митохондриальной НАД-зависимой малатдегидрогеназы. В митохондриях отношение НАДН/НАД+ относительно велико, в связи с чем внутримитохондриальный оксалоацетат легко восстанавливается в малат, который легко выходит из митохондрии через митохондриальную мембрану. В цитозоле отношение НАДН/НАД+ очень мало, и малат вновь окисляется при участии цитоплазматической НАД-за-висимой малатдегидрогеназы:
3 
Затем оксалоацетат в результате декарбоксилирования и фосфорили-рования под влиянием фермента фосфоенолпируваткарбоксилазы превращается в фосфоенолпируват. Донором фосфатного остатка в реакции служит гуанозинтрифосфат (ГТФ):
4 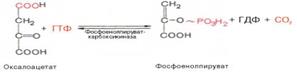
Далее идут обратимые реакции гликолиза:
1 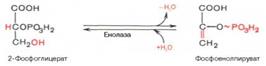
2 
3 
4 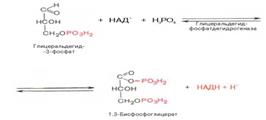
5 
6 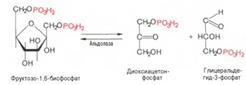
7. Далее следует фосфофруктокиназная реакция, которая необратима. Глюконеогенез идет в обход этой эндергонической реакции:

8. 
9. Образованиеглюкозыиз глюкозо-6-фосфата.

