В. Дефекты репарационных систем и наследственные болезни
Репарация необходима для сохранения нативной структуры генетического материала на протяжении всей жизни организма. Снижение активности ферментов репарационных систем приводит к накоплению повреждений (мутаций) в ДНК.
Причиной многих наследственных болезней человека выступает нарушение отдельных этапов процесса репарации.
Пигментная ксеродерма
У больных в системе репарации снижена активность ферментов, ответственных за удаление неправильных оснований, "застройку" бреши и другие функции. Дефект репарационной системы проявляется в сверхчувствительности к УФ-свету, что приводит к появлению красных пятен на коже, переходящих в незаживающие коросты и нередко в рак кожи.
Трихотиодистрофия
Заболевание связано с повышенной фоточувствительностью ДНК, вызванной снижением активности фермента, участвующего в удалении димеров тимина. Симптомы заболевания: ломкость волос вследствие нехватки серы в белках волос и их луковиц; часто умственная д физическая отсталость; аномалии кожи и зубов.
20.Регуляция клеточной активности. Гибель клеток – как нормальный физиологический процесс
Гибель (смерть) отдельных клеток или целых их групп постоянно встречается у многоклеточных организмов, также как гибель одноклеточных организмов. Причины гибели, процессы морфологического и биохимического характера развития клеточной смерти могут быть различными. Но все же их можно четко разделить на две категории: некроз (от греч. nekrosis - омертвление) и апоптоз (от греч. корней, означающих «отпадение» или «распадение»), который часто называют программируемой клеточной смертью (ПКС) или даже клеточным самоубийством (рис. 354).
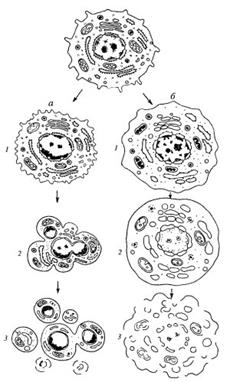 |
| Рис. 354. Два пути клеточной гибели а — апоптоз (программированная клеточная смерть): 1 — специфическое сжатие клетки и конденсация хроматина, 2 — фрагментация ядра, 3 — фрагментация тела клетки на ряд апоптических телец; 6 — некроз: 1 — набухание клетки, вакуолярных компонентов, конденсация хроматина (кариорексис), 2 — дальнейшее набухание мембранных органоидов, лизис хроматина ядра (кариолизис), 3 — разрыв мембранных компонентов клетки - лизис клетки |
Некроз
Этот вид клеточной смерти обычно связывается с нарушением внутриклеточного гомеостаза в результате нарушения проницаемости клеточных мембран, приводящим к изменению концентрации ионов в клетке, с необратимыми изменениями митохондрий, что сразу приводит к прекращению всех жизненных функций, включая синтез макромолекул. Некроз вызывают повреждения плазматической мембраны, подавление активности мембранных насосов под действием многих ядов, а также необратимые изменения энергетики при недостатке кислорода (при ишемии происходит закупорка кровеносного сосуда) или отравлении митохондриальных ферментов (действие цианидов). При этом при повышении проницаемости плазматической мембраны клетка набухает за счет ее обводнения, в цитоплазме происходит увеличение концентрации ионов Na+ и Са2+, закисление цитоплазмы, набухание вакуолярных компонентов и разрыв их мембран, прекращение синтеза белков в цитозоле, освобождение лизосомных гидролаз и лизис клетки. Одновременно с этими изменениями в цитоплазме изменяются и клеточные ядра: вначале они компактизируются (пикноз ядер), но по мере набухания ядра и разрыва его оболочки пограничный слой хроматина распадается на мелкие массы (кариорексис), а затем наступает кариолизис - растворение ядра. Особенностью некроза является то, что такой гибели подвергаются большие группы клеток (например, при инфаркте миокарда из-за прекращения снабжения кислородом участка сердечной мышцы). Обычным является то, что участок некроза подвергается атаке лейкоцитов и в зоне некроза развивается воспалительная реакция (см. рис. 354).
Апоптоз
В процессе развития организмов и их функционировании во взрослом состоянии часть клеток постоянно гибнет, но без их физического или химического повреждения, происходит как бы их «беспричинная» смерть. Гибель клеток наблюдается практически на всех стадиях онтогенеза. Многочисленны примеры отмирания клеток без повреждения при эмбриогенезе. Так, отмирают клетки вольфовых и мюллерова каналов при развитии мочеполовой системы у позвоночных, погибает часть нейробластов и гонадоцитов, клетки при метаморфозах насекомых и амфибий (резорбция хвоста у головастика и жабер у тритона) и т.д.
Во взрослом организме также постоянно происходит «спонтанная» гибель клеток. Миллионами погибают клетки крови — нейтрофилы, клетки эпидермиса кожи, клетки тонкого кишечника — энтероциты. Погибают фолликулярные клетки яичника после овуляции, клетки молочной железы после лактации. Таких примеров много. Особенно много примеров гибели клеток без непосредственного их повреждения при различных патологических процессах. Например, кастрация (удаление семенников) вызывает гибель клеток простатической железы, удаление гипофиза приводит к гибели клеток надпочечников. Другой пример — гибель шванновских клеток при дегенерации аксона. Шванновские клетки в поврежденном периферическом нерве взрослого животного, так же как и клетки-сателлиты и чувствительные нейроны в соответствующих спинномозговых узлах, погибают.
Эти наблюдения наводят на мысль, что клеточная смерть регулируется межклеточными взаимодействиями различным образом. Множество клеток многоклеточного организма нуждается в сигналах с тем, чтобы оставаться живыми. В отсутствие таких сигналов или трофических факторов в клетках развивается программа «самоубийства» или программируемой смерти. Например, клетки культуры нейронов погибают при отсутствии фактора роста нейронов (NGF), клетки простаты гибнут в отсутствие андрогенов семенника, клетки молочной железы — при падении уровня гормона прогестерона и т.д. В то же время клетки могут получать сигналы, которые в клетках-мишенях запускают процессы, приводящие к гибели по типу апоптоза. Так, гидрокортизон вызывает гибель лимфоцитов, а глютамат — нервных клеток в культуре ткани, фактор некроза опухоли (TNF) вызывает гибель самых различных клеток. Тироксин (гормон щитовидной железы) вызывает апоптоз клеток хвоста головастиков. Кроме этого существуют ситуации, когда апоптическая гибель клетки вызывается внешними факторами, например радиацией.
Понятие «апоптоз» было введено при изучении гибели части клеток печени при неполной перевязке портальной вены. При этом наблюдается своеобразная картина клеточной смерти, которая затрагивает лишь отдельные клетки в паренхиме печени. Процесс начинается с того, что соседние клетки теряют контакты, они как бы сморщиваются (первоначальное название этой формы гибели shrinkage necrosis - некроз сжатием клетки), в ядрах по их периферии происходит специфическая конденсация хроматина, затем ядро фрагментируется на отдельные части, вслед за этим сама клетка фрагментируется на отдельные тельца, отграниченные плазматической мембраной, — апоптические тельца.Апоптоз — процесс, приводящий не к лизису, не к растворению клетки, а к ее фрагментации, распаду. Судьба апоптических телец тоже необычна: они фагоцитируются макрофагами или даже нормальными соседними клетками. При этом не развивается воспалительная реакция.
Важно отметить, что во всех случаях апоптоза — во время ли эмбрионального развития, во взрослом ли организме, в норме или при патологических процессах — морфология процесса гибели клеток очень сходна. Это может говорить об общности процессов апоптоза в разных организмах и в разных органах.
Исследования на разных объектах показали, что апоптоз есть результат реализации генетически запрограммированной клеточной гибели. Первые доказательства наличия генетической программы клеточной смерти (ПКС) были получены при изучении развития нематоды Caenorhabditis elegans. Этот червь развивается всего за трое суток, и его малые размеры позволяют проследить за судьбой всех его клеток, начиная с ранних этапов дробления до половозрелого организма.
Оказалось, что при развитии С. elegans образуется всего 1090 клеток, из которых часть нервных клеток в количестве 131 штуки спонтанно погибает путем апоптоза и в организме остается 959 клеток. Были обнаружены мутанты, у которых процесс элиминации 131 клетки был нарушен. Были выявлены два гена ced-З и ced-4, продукты которых вызывают апоптоз 131 клетки. Если у мутантных C. elegans эти гены отсутствуют или изменены, то апоптоз не наступает и взрослый организм состоит из 1090 клеток. Был найден и другой ген - ced-9, который является супрессором апоптоза: при мутации ced-9 все 1090 клеток погибают. Аналог этого гена был обнаружен у человека: ген bcl-2 также является супрессором апоптоза различных клеток. Оказалось, что оба белка, кодируемые этими генами, — Ced-9 и Всl-2, имеют один трансмембранный домен и локализуются во внешней мембране митохондрий, ядер и эндоплазматического ретикулума.
Система развития апоптоза оказалась очень сходной у нематоды и позвоночных животных, она состоит из трех звеньев: регулятора, адаптера и эффектора. У C. elegans регулятором является Ced-9, который блокирует адаптерный белок Ced-4, который в свою очередь не активирует эффекторный белок Ced-З, протеазу, которая действует на белки цитоскелета и ядра (табл. 16).
| Развитие процесса программированной клеточной смерти (апоптоза) |
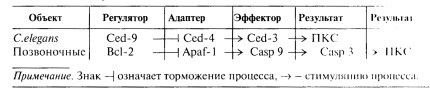 |
У позвоночных система ПКС более сложная. Здесь регулятором является белок Всl-2, который ингибирует адаптерный белок Араf-1, стимулирующий каскад активации специальных протеиназ — каспаз.
Каспазы— цистеиновые протеазы, которые расщепляют белки по аспарагиновой кислоте. В клетке каспазы синтезируются в форме латентных предшественников — прокаспаз. Существуют инициирующие и эффекторные каспазы. Инициирующие каспазы активируют латентные формы эффекторных каспаз. Субстратами для действия активированных каспаз служат более 60 различных белков. Это, например, киназа фокальных адгезионных структур, инактивация которой приводит к отделению апоптических клеток от соседей; это ламины, которые при действии каспаз разбираются; это цитоскелетные белки (промежуточные филаменты, актин, гельзолин), инактивация которых приводит к изменению формы клетки и к появлению на ее поверхности пузырей, которые дают начало апоптическим тельцам; это активируемая протеаза САD, которая расщепляет ДНК на олигонуклеотидные нуклеосомные фрагменты; это ферменты репарации ДНК, подавление которых предотвращает восстановление структуры ДНК, и многие другие.
Одним из примеров разворачивания апоптозного ответа может являться реакция клетки на отсутствие сигнала от необходимого трофического фактора, например фактора роста нервов (NGF), или андрогена (рис. 355).
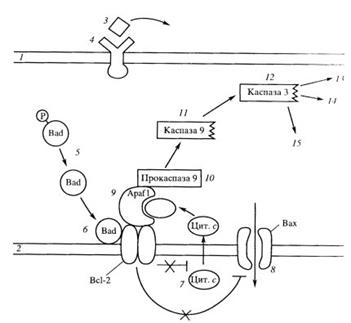 |
| Рис. 355. Одна из моделей развития апоптоза при отсутствии трофического фактора 1 — плазматическая мембрана; 2 — внешняя мембрана митохондрии; 3 —трофический фактор; 4 — рецептор трофического фактора; 5 — дефосфорилирование проапоптозного белка Bad; 6 — белок Bad инактивирует антиапоптозный белок Bcl-2; 7 — выход цитохрома с в цитозоль; 8 — активация апоптозного белка Вах, открывание ионных каналов; 9 — цитохром с активирует адаптерный белок Apaf-1; 10 — активация прокаспазы 9; 11 — активация каспазы 9; 12 — активация каспазы 3; 13 — конденсация и деградация хроматина; 14 —деградация ядерной ламины; 15 —деградация цитоскелета |
В цитоплазме клеток в присутствии трофических факторов находится в неактивной форме еще один участник реакции — фосфорилированный белок Bad. В отсутствие трофического фактора этот белок дефосфорилируется и связывается с белком Всl-2 на внешней митохондриальной мембране и этим ингибирует его антиапоптозные свойства. После этого активируется мембранный проапоптический белок Вах, открывая путь ионам, входящим в митохондрию. В это же время из митохондрий через образовавшиеся в мембране поры в цитоплазму выходит цитохром с, который связывается с адаптерным белком Apaf-1, который в свою очередь активирует прокаспазу 9. Активированная каспаза 9 запускает каскад других прокаспаз, в том числе каспазу 3, которые, будучи протеиназами, начинают переваривать мешенные белки (ламины, белки цитоскелета и др.), что вызывает апоптическую смерть клетки, ее распад на части, на апоптические тельца.
Апоптические тельца, окруженные плазматической мембраной разрушенной клетки, привлекают отдельные макрофаги, которые их поглощают и переваривают с помощью своих лизосом. Макрофаги не реагируют на соседние нормальные клетки, но узнают апоптические. Это связано с тем, что при апоптозе нарушается асимметрия плазматической мембраны и на ее поверхности появляется фосфатидилсерин, негативно заряженный фосфолипид, который в норме располагается в цитозольной части билипидной плазматической мембраны. Таким образом, путем избирательного фагоцитоза ткани как бы очищаются от погибших апоптозных клеток.
Как указывалось выше, апоптоз может быть вызван целым рядом внешних факторов, таких как радиация, действие некоторых токсинов, ингибиторов клеточного метаболизма. Необратимые повреждения ДНК вызывают апоптоз. Это связано с тем, что накапливающийся транскрипционный фактор — белок р53, не только активирует белок р21, который ингибирует зависящую от циклина киназу и останавливает клеточный цикл в G1- или G2-фазе (см. рис. 353), но и активирует экспрессию гена Ьах, продукт которого запускает апоптоз.
Избирательные повреждения митохондрий, при которых в цитоплазму высвобождается цитохром с, также являются частой причиной развития апоптоза. Особенно митохондрии и другие клеточные компоненты страдают при образовании токсически активных форм кислорода (АТК), под действием которых во внутренней мембране митохондрий образуются неспецифические каналы с высокой проницаемостью для ионов, в результате чего матрикс митохондрий набухает, а внешняя мембрана разрывается. При этом растворенные в межмембранном пространстве белки вместе с цитохромом с выходят в цитоплазму. Среди освободившихся белков есть факторы, активирующие апоптоз, и прокаспаза 9.
Многие токсины (рицин, дифтерийный токсин и др.), а также антиметаболиты могут вызывать гибель клеток путем апоптоза. При нарушении синтеза белка в эндоплазматическом ретикулуме в развитии апоптоза участвует локализованная там прокаспаза 12, которая активирует ряд других каспаз, и в том числе каспазу 3.
Элиминация — удаление отдельных клеток путем апоптоза, наблюдается и у растений. Здесь апоптоз включает в себя, так же как у животных клеток, фазу индукции, эффекторную фазу и фазу деградации. Морфология гибели клеток растений сходна с изменениями клеток животных: конденсация хроматина и фрагментация ядра, олигонуклеотидная деградация ДНК, сжатие протопласта, его дробление на везикулы, разрыв плазмодесм и т.д. Однако везикулы протопласта разрушаются гидролазами самих везикул, так как у растений нет клеток, аналогичных фагоцитам. Так, ПКС происходит при росте клеток корневого чехлика, при формировании перфораций у листьев, при образовании ксилемы и флоэмы. Опадание листьев связано с избирательной гибелью клеток определенной зоны черенка.
Биологическая роль апоптоза, или программированной смерти клеток, очень велика: это удаление отработавших свое или ненужных на данном этапе развития клеток, а также удаление измененных или патологических клеток, особенно мутантных или зараженных вирусами.
Итак, для того чтобы клетки в многоклеточном организме существовали, нужны сигналы на их выживание — трофические факторы, сигнальные молекулы. Эти сигналы могут быть переданы на расстояние и уловлены соответствующими рецепторными молекулами на клетках-мишенях (гормональная, эндокринная сигнализация), это может быть паракринная связь, когда сигнал передается на соседнюю клетку (например, передача нейромедиатора). При отсутствии таких трофических факторов реализуется программа апоптоза. В то же время апоптоз может вызываться сигнальными молекулами, например при резорбции хвоста головастиков под действием тироксина. Кроме того, действие ряда токсинов, влияющих на отдельные звенья метаболизма клетки, также может стать причиной клеточной гибели посредством апоптоза.
