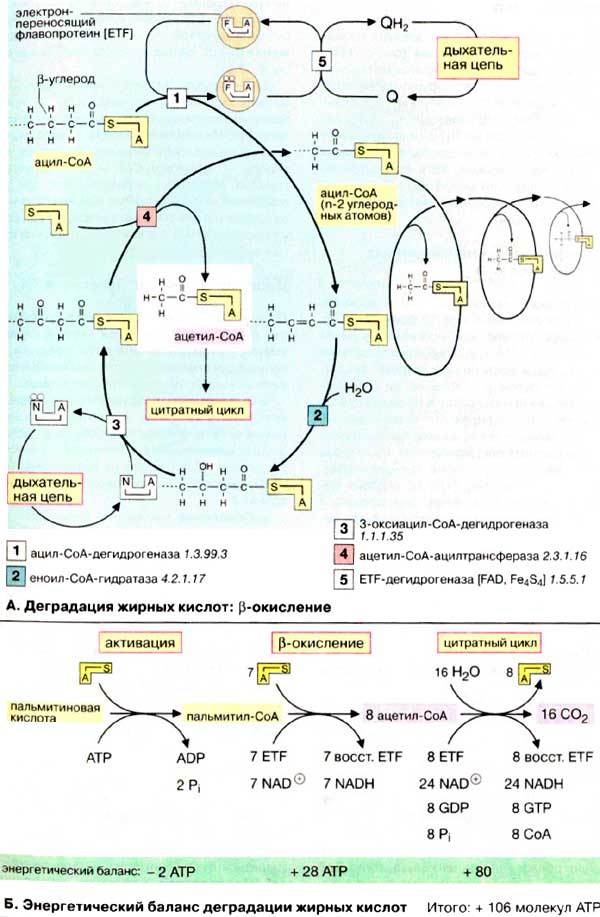
Б. Энергетический баланс деградации жирных кислот
Для расчета энергетического баланса деградации жирной кислоты в качестве примера рассмотрим молекулу пальмитиновой кислоты (16:0), которая окисляется полностью до 16 молекул СО2. На первой стадии жирная кислота активируется, потребляя две богатые энергией связи [АТФ (АТР)], с образованием пальмитоил-СоА состоящего из восьми C2-звеньев. Затем протекают семь циклов β-окисления. При этом образуются 7 молекул восстановленной формы флавопротеина (ETF) и 7 молекул НАДН + Н+. Оба соединения включаются в дыхательную цепь; окисление ETF через убихинон дает в итоге 1,5 молекулы АТФ, а НАДН + Н+ — 2,5 молекулы (см. рис. 143). Таким образом, β-окисление одного пальмитоильного остатка дает 28 молекул (7 х 4) АТФ. Окисление каждой молекулы ацетил-КоАприводит к образованию 10 молекул АТФ, что означает получение еще 80 молекул (8 x 10) АТФ. Из 28 + 80 молекул АТФ следует вычесть две молекулы АТФ, израсходованные при активации пальмитиновой кислоты (см. выше). Итак, при утилизации одной молекулы пальмитиновой кислоты синтезируются 106 молекул АТФ, что соответствует свободной энергии 3300 кДж/моль (106 х 30,5 кДж/моль АТФ). Выигрыш в энергии при деградации жирных кислот существенно выше по сравнению с распадом углеводов (32 молекулы АТФ на 1 молекулу глюкозы) и белков даже с учетом больших размеров молекул. Поэтому жиры представляют собой очень выгодную форму сохранения энергии.
Пентозофосфатный путь окисления глюкозы. Реакции окислительной и неокислительной стадий пентозофосфатного цикла. Современная схема пентозофосфатного пути окисления углеводов, отзеркаливающая его связь с гликолизом.
Пентозофосфатный путь, называемый также гексомонофосфатным шунтом, служит альтернативным путём окисления глюкозо-6-фосфата. Пентозофосфатный путь состоит из 2 фаз (частей) - окислительной и неокислительной.
В окислительной фазе глюкозо-6-фосфат необратимо окисляется в пентозу - рибулозо-5-фосфат, и образуется восстановленный NADPH.
В неокислительной фазе рибулозо-5-фосфат обратимо превращается в рибозо-5-фосфат и метаболиты гликолиза.
Пентозофосфатный путь обеспечивает клетки рибозой для синтеза пуриновых и пиримидиновых нуклеотидов и гидрированным ко-ферментом NADPH, который используется в восстановительных процессах.
Суммарное уравнение пентозофосфатного пути выражается следующим образом:
3 Глюкозо-6-фосфат + 6 NADP+ → 3 СО2 + 6 (NADPH + Н+) + 2 Фруктозо-6-фосфат + Глицеральдегид- 3 -фосфат.
Ферменты пентозофосфатного пути, так же, как и ферменты гликолиза, локализованы в цитозоле.
Наиболее активно Пентозофосфатный путь протекает в жировой ткани, печени, коре надпочечников, эритроцитах, молочной железе в период лактации, семенниках.
А. Окислительный этап
В окислительной части пентозофосфатного пути глюкозо-6-фосфат подвергается окислительному декарбоксилированию, в результате которого образуются пентозы. Этот этап включает 2 реакции дегидрирования.
Первая реакция дегидрирования - превращение глюкозо-6-фосфата в глюконолактон-6-фосфат - катализируется МАDР+-зависимой глюкозо-6-фосфатдегидрогеназой и сопровождается окислением альдегидной группы у первого атома углерода и образованием одной молекулы восстановленного кофермента NADPH.
Далее глюконолактон-6-фосфат быстро превращается в 6-фосфоглюконат при участии фермента глюконолактонгидратазы.
Фермент 6-фосфоглюконатдегидрогеназа катализирует вторую реакцию дегидрирования окислительной части, в ходе которой происходит также и декарбоксилирование. При этом углеродная цепь укорачивается на один атом углерода, образуется рибулозо-5-фосфат и вторая молекула гидрированного NADPH (рис. 7-62).
Восстановленный NADPH ингибирует первый фермент окислительного этапа пентозофосфатного пути - глюкозо-6-фосфатдегидрогеназу. Превращение NADPH в окисленное состояние NADP+ приводит к ослаблению ингибирования фермента. При этом скорость соответствующей реакции возрастает, и образуется большее количество NADPH.
Суммарное уравнение окислительного этапа пентозофосфатного пути можно представить в виде:
Глюкозо-6-фосфат + 2 NADP+ + Н2О → Рибулозо-5-фосфат + 2 NADPH + Н+ + СО2.
Реакции окислительного этапа служат основным источником NADPH в клетках. Гидрированные коферменты снабжают водородом биосинтетические процессы, окислительно-восстановительные реакции, включающие защиту клеток от активных форм кислорода. NADPH как донор водорода участвует в анаболических процессах, например в синтезе холестерина. Это источник восстановительных эквивалентов для цитохрома Р450, катализирующего образование гидроксильных групп при синтезе стероидных гормонов, жёлчных кислот, при катаболизме лекарственных веществ и других чужеродных соединений (см. разделы 8, 11, 12). Высокая активность фермента глюкозо-6-фосфатдегидрогеназы обнаружена в фагоцитирующих лейкоцитах, где NADPH-оксидаза использует восстановленный NADPH для образования супероксидного иона из молекулярного кислорода. Супероксидный ион генерирует другие активные формы кислорода, под действием которых и повреждаются молекулы ДНК, белков, липидов бактериальньж клеток. Синтез жирных кислот из углеводов в печени является основным путём утилизации NADPH и обеспечивает регенерацию окисленной формы NADP+. В печени глюкозо-6-фосфатдегидрогеназа, как и ключевые ферменты гликолиза и биосинтеза жирных кислот, индуцируется при увеличении соотношения инсулин/глюкагон после приёма богатой углеводами пищи.
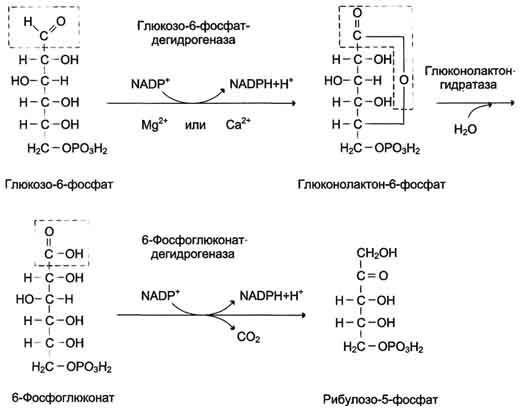
Окислительный этап пентозофосфатного пути.
Несмотря на то, что NADPH образуется также при окислении малата до пирувата и диоксида углерода (при участии НАDР+-зависимой малатдегидрогеназы) и дегидрировании изо-цитрата (при участии НАВР+-зависимой изоцитратдегидрогеназы), в большинстве случаев потребности клеток в восстановительных эквивалентах удовлетворяются за счёт пентозофосфатного пути.
Реакции окислительного пути протекают только в том случае, если восстановленный ко-фермент NADPH возвращается в исходное окисленное состояние NADP+ при участии NADPH-зависимых дегидрогеназ (т.е. при условии использования гидрированного NADPH в восстановительных процессах). Если потребности клетки в NADPH незначительны, рибо-зо-5-фосфат образуется в результате обратимых реакций неокислительного этапа пентозофосфатного пути, используя в качестве исходных веществ метаболиты гликолиза - глицеральдегид-3-фосфат и фруктозо-6-фосфат.
Б. Неокислительный этап
Неокислительный этап пентозофосфатного пути включает серию обратимых реакций, в результате которых рибулозо-5-фосфат превращается в рибозо-5-фосфат и ксилулозо-5-фосфат, и далее за счёт переноса углеродных фрагментов в метаболиты гликолиза - фруктозо-6-фосфат и глицеральдегид-3-фосфат. В этих превращениях принимают участие ферменты: эпимераза, изомераза, транскетолаза и трансальдолаза. Транскетолаза в качестве кофермента использует тиаминдифосфат. Неокислительный этап пентозофосфатного пути не включает реакции дегидрирования и поэтому используется только для синтеза пентоз.
Рибулозо-5-фосфат служит субстратом для двух ферментов. Фермент рибулозо-5-фосфат-З-эпимераза изменяет стехиометрическое положение одной ОН-группы у третьего атома углерода, превращая рибулозо-5-фосфат в ксилулозо-5-фосфат. Другой фермент - рибулозо-5-фосфатизомераза - катализирует превращение рибулозо-5-фосфата в рибозо-5-фосфат (рис. 7-63). Рибозо-5-фосфат, образующийся в неокислительной фазе, обеспечивает клетки рибозой, необходимой для синтеза нуклеотидов, которые служат предшественниками и структурными компонентами ко-ферментов дегидрогеназ и нуклеиновых кислот.
Ферменты транскетолаза и трансальдолаза катализируют перенос двух- и трёхуглеродных фрагментов, соответственно используя в качестве донора углеродных фрагментов кетозу, а альдозу - в качестве акцептора. Эти реакции протекают в 2 этапа: сначала происходит отщепление углеродного фрагмента от молекулы-донора, -а затем - перенос этого фрагмента на молекулу, выполняющую роль акцептора. Транскетолаза в неокислительной фазе пентозофосфатного пути катализирует 2 реакции. В первой реакции (рис. 7-64) транскетолаза расщепляет связь С-С между кетогруппой и соседним атомом углерода в молекуле ксилулозо-5-фосфат, в результате чего кетосахар превращается в альдозу, глицеральдегид-3-фосфат, содержащую на 2 атома углерода меньше. Образующийся после расщепления двухуглеродный фрагмент остаётся ковалентно связанным в каталитическом центре фермента с ко-ферментом тиаминдифосфатом. Далее фермент переносит двухуглеродный фрагмент на альдегидную группу альдосахара, образую новую кетозу - седргептулозо-7-фосфат.
Трансальдолаза переносит трёхуглеродный фрагмент от седогептулозо-7-фосфата на глицеральдегид-3-фосфат, образуя эритрозо-4-фосфат и фруктозо-6-фосфат (рис. 7-65).
Эта реакция подобна реакции альдольного расщепления гликолитического пути, за исключением того, что в данном случае трёхуглеродный фрагмент, содержащий кетогруппу, переносится на альдосахар глицеральдегид-3-фосфат, а в гликолитическом пути кетофрагмент высвобождается в виде дигидроксиацетонфосфата.
В следующей реакции, катализируемой транс-кетолазой, происходит перенос двухуглеродного фрагмента от ксилулозо-5-фосфата на эритрозо-4-фосфат. Продуктами этой реакции являются фруктозо-6-фосфат и глицеральдегид-3-фосфат (рис. 7-66).
Так как все реакции неокислительного этапа обратимы, образование рибозо-5-фосфата может происходить не только в результате изомерного превращения продукта окислительной фазы пентозофосфатного пути рибулозо-5-фосфата в рибозо-5-фосфат под действием изомеразы, но также и из промежуточных продуктов гликолиза - фруктозо-6-фосфата и глицеральдегид-3-фосфата. Последовательность превращений, приводящих к образованию рибозо-5-фосфата из таких продуктов гликолитического пути, можно представить в виде:
2 Фруктозо-6-фосфат + Глицеральдегид-3-фосфат → 2 Ксилулозо-5-фосфат + Рибозо-5-фосфат 2 Ксилулозо-5-фосфат → 2 Рибулозо-5-фосфат 2 Рибулозо-5-фосфат → 2 Рибозо-5-фосфат.
Суммарный результат метаболизма 3 молекул рибулозо-5-фосфата в неокислительной фазе пентозофосфатного пути - образование 2 молекул фруктозо-6-фосфата и 1 молекулы глицеральдегид-3-фосфата. Далее фруктозо-6-фосфат и глицеральдегид-3-фосфат могут превратиться в глюкозу. С учётом стехиометрического коэффициента, равного 2, для образования 5 молекул глюкозы (содержащих 30 атомов углерода) потребуются 4 молекулы фруктозо-6-фосфата и 2 молекулы глицеральдегид-3-фосфата (в сумме содержащие также 30 атомов углерода) или, соответственно, 6 молекул рибулозо-5-фосфата. Таким образом, неокислительный путь можно представить как процесс возвращения пентоз в фонд гексоз.
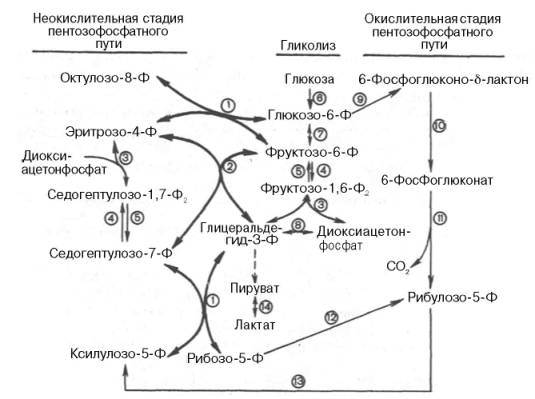
Рис. 10.13. Современная схема пентозофосфатного пути окисления углеводов, отражающая его связь с гликолизом (по Херсу).
1 - транскетолаза; 2 - трансальдолаза; 3 - альдолаза; 4 - фосфофруктокиназа; 5 - фруктозо-1,6-бисфосфатаза; 6 - гексокиназа; 7 - глюкозофосфатизомераза; 8 - триозофосфатизомераза; 9 -глюкозо-6-фосфатдегидрогеназа; 10 - 6-фосфоглюконолактоназа; 11 - 6-фосфоглюконатдегид-рогеназа; 12 - изомераза; 13 - эпимераза; 14 - лактатдегидрогеназа.
Билет№7
Опять ферменты
ЕДИНИЦА АКТИВНОСТИ ФЕРМЕНТА
выражение активности фермента в каталах (кат, kat): 1 кат есть каталитическая активность, способная осуществлять реакцию со скоростью, равной 1 молю в 1 с (1 моль/с).
УДЕЛЬНАЯ АКТИВНОСТЬ ФЕРМЕНТА
Для выражения активности в практической работе с ферментами часто пользуются произвольными понятиями удельной и молярной активности. Удельную активность фермента принято выражать числом единиц ферментативной активности на 1 мг белка (или числом каталов на 1 кг активного белка).
МОЛЯРНАЯ АКТИВНОСТЬ ФЕРМЕНТА
Количество молекул субстрата, подвергающихся превращению одной молекулой фермента в продукт в процессе реакции в единицу времени при полном насыщении фермента субстратом, принято называть числом оборотов фермента, или молярной активностью (молярная каталитическая активность выражается в каталах на 1 г-моль фермента).
