Процессы в живых организмах
РАЗДЕЛ I. СТРОЕНИЕ И СВОЙСТВА БЕЛКОВ
Занятие № 1
ТЕМА.БИОЛОГИЧЕСКАЯ РОЛЬ И ФИЗИКО-ХИМИ-
ЧЕСКИЕ СВОЙСТВА БЕЛКОВ. МЕТОДЫ ВЫДЕЛЕНИЯ
И ФРАКЦИОНИРОВАНИЯ БЕЛКОВ
Цель занятия:
1.Повторить физико-химические и изучить биологические
свойства белков.
2.Ознакомиться с методикой выделения белков.
3.Усвоить принцип разделения белков на фракции методом
высаливания.
Исходный уровень знаний:
- кислоты и основания в органической химии;
- химические свойства карбоксильной группы;
- механизм нуклеофильного замещения у тригонального ато-ма углерода;
- химические свойства аминогруппы: основность и нуклео-
фильность;
- строение, амфотерность и растворимость аминокислот;
- коллоидные растворы и их свойства.
Содержание занятия.
I.2. Элементарный состав белков.
Классификация и номенклатура аминокислот, входящих в состав белков.
Функции белков.
Характерные физико-химические свойства белков.
Методы выделения и очистки белков.
II.1. Работа: ВЫСАЛИВАНИЕ БЕЛКОВ
Высаливание - это осаждение белков с помощью больших концентраций нейтральных солей: NaCl, (NH4)2 SO4 и др.
Принцип метода.
Реакция высаливания обусловлена дегидратацией макромолекул белка с одновременной нейтрализацией электрического заряда. Для высаливания различных белков требуется определенная концентрация одних и тех же солей. При высаливании белок обычно не теряет своих нативных свойств. Он может, например, вновь проявлять ферментативную активность. Метод высаливания позволяет получить белки в кристаллическом виде и разделить белковую смесь на фракции, а именно: белки сыворотки крови - на альбумины (А) и глобулины (Г). Глобулины, имеющие большую молекулярную массу, высаливаются в полунасыщенном (50%), а альбумины - в насыщенном (100%) растворе сернокислого аммония.
Хлористый натрий осаждает глобулины при полном насыщении (100%) раствора, а для осаждения альбуминов требуется еще и его подкисление.
Высаливание белков является обратимой реакцией, т.к. осадок белка опять может раствориться после уменьшения концентрации солей диализом или разведением водой.
Для определения белка в растворе используется универсальная биуретовая реакция.
Химизм биуретовой реакции. Биуретовая реакция выявляет в белке пептидную ( -CO-NH- ) связь. В щелочной среде раствор белка при взаимодействии с ионами меди приобретает сине-фиолетовый цвет, а продукты его неполного гидролиза (пептоны) - розовое окрашивание. Биуретовую реакцию способны давать вещества, которые содержат не менее двух пептидных связей. Биуретовая реакция обусловлена образованием биуретового комплекса в результате соединения меди с пептидной группировкой белка. В щелочной среде лактимные формы образуются из лактамных форм. Биуретовая реакция схематично протекает так:
H R2 O H R4 O
| | || | | || Cu(OH)2+2NaOH
 H2N-CH-C-N-CH-C-N-CH-C-N-CH-C-N-CH- .....
H2N-CH-C-N-CH-C-N-CH-C-N-CH-C-N-CH- .....
| || | | || | |
R1 O H R3 O H R5
полипептид (лактамная форма)
R2 OH R4 OH
| | | |
 H2N-CH-C=N-CH-C=N-CH-C=N-CH-C=N-CH- ....
H2N-CH-C=N-CH-C=N-CH-C=N-CH-C=N-CH- ....
| | | | |
R1 OH R3 OH R5
полипептид (лактимная форма)
| Положительную биуретовую реакцию отдельные аминокислоты не дают. Исключение: гистидин и аспарагин, с которыми биуретовая реакция происходит при условии их больших концентраций в растворе. |
R2
|
R1-HC-C=N-CH-C=N-CH-R3
| | | |

 H2N O O C-ONa
H2N O O C-ONa
||
Cu — ―N
↑ ¦
| R4-CH
| | СOONa COONa
| C -ОNа | |
| || CH-NH2 CH-NH2

 └ ― ― ― — N | |
└ ― ― ― — N | |
 | CH2 CH2
| CH2 CH2
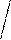


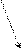

 CH-R5 | N N
CH-R5 | N N

 N Cu N
N Cu N
биуретовый медный комплекс медный комплекс с гистидином
фиолетового цвета в случае биуретовой реакции
ПРИМЕЧАНИЕ: при постановке биуретовой реакции нельзя добавлять избыток сульфата меди, так как синий осадок гидрата окиси меди маскирует фиолетовое окрашивание биуретового комплекса белка.
Порядок выполнения работы.
| Реактивы | 1 пробирка | 2 пробирка |
| Раствор белка | 20 кап. | 20 кап. |
| Порошок NaCl | до полного насыщения | - |
| Насыщенный раствор (NH4)2SO4 | - | 20 кап. |
| ФИЛЬТРОВАНИЕ | ||
| Осадок | Глобулины | Глобулины |
| К фильтрату 1 добавить | ||
| 1% раствор CH3COOH | 10-20 кап. | - |
| Порошок (NH4)2SO4 | - | до полного насыщения |
| ФИЛЬТРОВАНИЕ | ||
| Осадок | Альбумины | Альбумины |
| КОНТРОЛЬ - БИУРЕТОВАЯ РЕАКЦИЯ | ||
| Фильтрат 2 | 5 кап. | 5 кап. |
| 10% NaOH | 5 кап. | 5 кап. |
| 1% CuSO4 | 1 кап. | 1 кап. |
| РЕЗУЛЬТАТЫ: |
ВЫВОД:
III.2.Контрольные вопросы.
Какие факторы удерживают белки в растворе?
Чем обусловлен коллоидный характер белковых растворов?
На чем основаны реакции осаждения белков?
Какие физико-химические свойства белков позволяют их
фракционировать?
Что такое высаливание?
С помощью какой реакции можно выявить белок
в растворе?
Какую окраску имеют белковые и безбелковые растворы
при проведении биуретовой реакции?
Какие отдельные аминокислоты могут дать
положительную биуретовую реакцию?
Чем отличаются альбумины и глобулины?
Материал для самоподготовки. I а)1. с.19-49, II, III.
Занятие № 2
ТЕМА. СТРУКТУРНАЯ ОРГАНИЗАЦИЯ БЕЛКОВЫХ
МОЛЕКУЛ. МЕТОДЫ ОЧИСТКИ БЕЛКОВ
Цель занятия: 1.Изучить структурную организацию белковой
молекулы как основу функционирования всех белков.
2.Ознакомиться с особенностями структуры фибриллярных
белков.
3.Освоить методы очистки белков от примесей на примере
диализа.
Исходный уровень знаний:
- аминокислоты: строение, классификация;
- ковалентные и нековалентные связи: характеристика, при-
меры;
- физико-химические свойства белков.
Содержание занятия.
I.2. Строение глобулярных белков (первичная, вторичная, третичная, четвертичная структуры).
Особенности строения молекулы фибриллярных белков.
Взаимосвязь структуры и функции белков.
Видовая специфичность первичной структуры и антигенные свойства белков.
Методы очистки белков (хроматография, электрофорез, диализ и др.).
Гидролиз белка (виды, условия, продукты полного и неполного гидролиза).
II.1. Работа: ДИАЛИЗ БЕЛКА
Принцип метода.
Диализ основан на способности полупроницаемых мембран пропускать сквозь поры низкомолекулярные вещества и задерживать высокомолекулярные коллоидные частицы. Ди-ализ является удобным методом очистки белков. При диализе коллоидный раствор помещают в коллодиевый или целлофановый мешочек и погружают в дистиллированную или водопроводную воду. Молекулы солей, сахаров и других низкомолекулярных веществ легко диффундируют через мембраны, а вещества коллоидной природы остаются в мешочке.
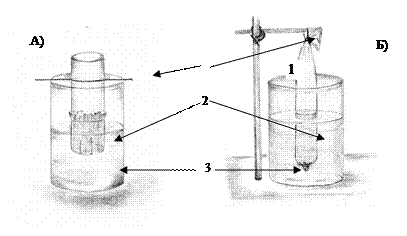 |
Рис. 1. Варианты устройства системы для диализа белка. А) диализатор из стеклянного цилиндра с дном из полупроницаемой мембраны. Б) диализатор из коллодиевого мешочка. 1-держатель, 2-диализуемый раствор, 3-диализат.
Порядок выполнения работы.
В коллодиевый мешочек (диализатор) налить 5 мл солевого раствора белка. Погрузить в стакан с дистиллированной водой на 1 час. Через час с небольшими порциями диализата (наружная жидкость) проделать реакции на хлориды и белок и убедиться в том, что минеральные соли продиффундировали во внешний сосуд, а белок остался в содержимом мешочка.
Проба на белок (биуретовая реакция).
| Реактивы (кап.) | 1 пробирка (диализуемый раствор) | 2 пробирка (диализат) |
| Исследуемая жидкость | ||
| 10% раствор NaOH | ||
| 1% раствор CuSO4 | ||
| РЕЗУЛЬТАТЫ: | ||
| Проба на хлориды | ||
| Исследуемая жидкость | ||
| 10% раствор HNO3 | ||
| 1% раствор AgNO3 | ||
| РЕЗУЛЬТАТЫ: |
ВЫВОД:
III.2. Контрольные вопросы.
Что такое диализ?
Что такое диализат и диализуемая жидкость?
Какие реакции используются для контроля диализа?
Как используется диализ в медицине?
Материал для самоподготовки. I а)1. с.26-32, 49-71; II; III.
Занятие № 3
ТЕМА.КЛАССИФИКАЦИЯ БЕЛКОВ. ХИМИЯ ПРОСТЫХ И
СЛОЖНЫХ БЕЛКОВ. МЕТОДЫ ОСАЖДЕНИЯ БЕЛКОВ
Цель занятия: 1.Ознакомиться с классификацией белков, харак-
теристиками отдельных групп белков и пептидов.
2.Освоить методы осаждения белков.
Исходный уровень знаний:
- строение и свойства белков;
- биологическая роль белков.
Содержание занятия.
I.2. Характеристика основных групп простых белков.
Принцип классификации сложных белков.
Характеристика природных пептидов.
Содержание белков и аминокислот в крови в норме и при патологии.
I.3. Контрольная работа.
СВОДНЫЕ ВОПРОСЫ К КОНТРОЛЬНОЙ РАБОТЕ
ПО РАЗДЕЛУ "СТРОЕНИЕ И СВОЙСТВА БЕЛКОВ"
1. Определение класса белков. Элементарный состав, наименьшая структурная единица, молекулярная масса белков.
2. Классификация аминокислот, входящих в состав белков, основанная на полярности радикалов; примеры неполярных, полярных, положительно- и отрицательно заряженных аминокислот.
3. Амфотерность и растворимость аминокислот. Функциональные группы аминокислот, участвующие в образовании ковалентных, ионных, электростатических и гидрофобных (Ван-дер-Ваальса) связей белковой молекулы.
4. Структура и название аминокислот, производных пропионовой, масляной, валериановой, капроновой, янтарной и глутаровой кислот.
5. Структура и название окси- и серусодержащих, гомо- и гетероциклических аминокислот.
6. Факторы, удерживающие белок в растворе. Изоэлектрическая точка белков. Методы осаждения белков, значение для медицины. Обратимое и необратимое осаждение. Примеры.
7. Основные физико-химические свойства белков. Свойства коллоидных растворов, отличительные от свойств истинных растворов. Методы выделения и очистки белков. Диализ, значение для медицины.
8. Методы обнаружения белков в растворе и изучения качественного состава белка. Гидролиз белка, виды гидролиза, промежуточные и конечные продукты. Применение белковых гидролизатов в лечебной практике.
9. Назовите трипептид, например:
H3C-CH-CH2-CH-CO-NH-CH-CO-NH-CH-COOH
| | | |
CH3 NH2 CH3 CH2
|
CH2-S-CH3
 |  | ||

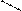 -CH2-CH-CO-NH-CH-CO-N
-CH2-CH-CO-NH-CH-CO-N
 | | |
| | |
NH2 (CH2)3 COOH
|
CH2NH2
10. Напишите трипептид: а) глицил-валил-изолейцин;
б) лейцил-тирозил-гистидин; в) аланил-метионил-триптофан и т.п.
11. Белки - основа жизненных процессов. Значение работ А.Я.Данилевского, Э.Фишера, Л.Полинга в формировании представлений о строении белков. Уровни структурной организации белковой молекулы.
12. Первичная структура, формирующие её связи. Зависимость биологических свойств белков от характера аминокислотной последовательности в полипептидной цепи ( HbA, HbS ).
13. Конформация пептидных цепей в белках: вторичная и третичная структуры, связи, определяющие эти структуры. Об-ратимая и необратимая денатурация белков; причины, значение.
14. Высшая форма организации белковой молекулы - четвертичная структура. Кооперативные изменения конформации протомеров (на примере гемоглобина и миоглобина).
15. Зависимость функциональных свойств белков от их конформации. Способность к специфическим взаимодействиям ("узнавание") как основа функционирования всех белков. Антигенные свойства белков.
16. Биологические функции белков. Различия белкового состава органов. Изменение белкового состава при онтогенезе и болезнях.
17. Классификация белков. Химия сложных белков. Важ-нейшие представители простых и сложных белков в организме человека.
18. Структурные белки. Классификация, особенности строения, распределение в тканях. Самосборка многомолекулярных белковых структур на примере коллагеновых волокон.
II.1. Работа № 1. ОСАЖДЕНИЕ БЕЛКОВ ПРИ КИПЯЧЕНИИ
Принцип метода основан на денатурации большинства белков при нагревании их растворов при температуре свыше 5О-6О0С, что приводит к потере растворимости, особенно в изоэлектрической точке.
Почти все белки свертываются и осаждаются при нагревании в нейтральной и слабокислой среде. В сильнокислых и щелочных средах растворы белков при кипячении денатурируют, но не коагулируют и могут дать осадок лишь при добавлении достаточного количества какой-либо нейтральной соли (NaCl, сернокислый аммоний и др.). Устойчивость белка в растворе зависит от приобретения (+) заряда в случае сильнокислой среды и усиления (-) заряда в щелочной среде.
+H+ -H+

 H3N+-CH-COOH H3N+-CH-COO- H2N-CH-COO-
H3N+-CH-COOH H3N+-CH-COO- H2N-CH-COO-
| | |
 R R R
R R R
молекула заряжена цвиттерионная молекула заряжена
"+" форма аминокислоты "-"
рН = 2-3 рН = 4-9 рН = 9-10
(биполярная форма)
При понижении рН диссоциация карбоксильной группы подавляется и молекула становится положительно заряженной. При повышении pH происходит отрыв связанного протона аминокислоты и молекула приобретает отрицательный заряд. Более полное и быстрое осаждение происходит при достижении изоэлектрической точки. Изоэлектрической точкой называют такое значение рН, при котором суммарный электрический заряд белка равен нулю и, следовательно, белок при этом в электрическом поле теряет подвижность, т.е. остается на старте. Для большинства белков изоэлектрическая точка соответствует слабокислой среде (в пределах от 5,5 до 6,9).
Итак, важную роль в денатурации белков при нагревании играет концентрация водородных ионов, т.е. определенная реакция среды, и присутствие солей.
Порядок выполнения работы:
| Реактивы (кап.) | Пробирки | ||||
| 1 | 2 | 3 | 4 | 5 | |
| 1% раствор яичного белка | |||||
| 1% раствор CH3COOH | - | - | |||
| насыщенный раст-вор NaCl | - | - | - | - | |
| 10% раствор NaOH | - | - | - | - | |
| КИПЯЧЕНИЕ | |||||
| Реакция среды | Нейт-ральная | слабо-кислая | сильнокислая | сильнокислая, + электролит | щело-чная |
| РЕЗУЛЬТАТЫ: |
ВЫВОД:
Работа № 2a. ОСАЖДЕНИЕ БЕЛКОВ СОЛЯМИ
ТЯЖЕЛЫХ МЕТАЛЛОВ
Принцип метода.
Осаждение белков солями тяжелых металлов в отличие от высаливания происходит при небольших концентрациях солей. Белки при взаимодействии с солями тяжелых металлов (свинца, меди, серебра, ртути и др.) адсорбируют их, образуя солеобразные и комплексные соединения, растворимые в избытке этих солей (за исключением солей AgNO3, HgCl2), но нерастворимые в воде.
Растворение осадка в избытке солей называется адсорбционной пептизацией. Данное явление происходит вследствие возникновения одноименного (+) заряда на частицах белка. Способность белка прочно связывать ионы тяжелых металлов в виде нерастворимых осадков в воде используется как противоядие при отравлении солями ртути, меди, свинца и др. Обычно применяют белки молока и яиц сразу после отравления, пока эти соли еще находятся в желудке и не успели всосаться. Вслед за введением белка у больного вызывают рвоту, чтобы удалить остатки яда из организма.
Порядок выполнения работы.
| Реактивы (кап.) | Пробирки | ||
| 1 | 2 | 3 | |
| а) Раствор яичного белка | |||
| 1% раствор CuSO4 | - | - | |
| 5% раствор Pb(CH3COO)2 | - | - | |
| 5% pаствор AgNO3 | - | - | |
| РЕЗУЛЬТАТЫ: | |||
| б) продолжение опыта в тех же пробирках (добавить) | |||
| 1% раствор CuSO4 | 5-10 | - | - |
| 5% pаствоp Pb(CH3COO)2 | - | 5-10 | - |
| 5% pаствоp AgNO3 | - | - | 5-10 |
| РЕЗУЛЬТАТЫ: |
ВЫВОД:
Работа № 2б. ОСАЖДЕНИЕ БЕЛКОВ КОНЦЕНТРИРОВАН-
НЫМИ МИНЕРАЛЬНЫМИ КИСЛОТАМИ
Принцип метода.
Концентрированные минеральные кислоты вызывают денатурацию белка и образуют комплексные соли белка с кислотами. В избытке всех минеральных кислот, за исключением азотной, выпавший осадок белка растворяется. Качественная реакция с концентрированной HNО3 лежит в основе количественного определения белка в моче по методу Робертса-Столь-никова-Брендберга.
Порядок выполнения работы:
| Реактивы (кап.) | I этап | II этап | ||
| Пробирки | ||||
| Концентрированная HNO3 | - | - | ||
| Концентрированная H2SO4 | - | - | ||
| Раствор белка | - | - | ||
| Примечание: Раствор белка осторожно наслоить на кислоту по стенке пробирки, наклоненной под углом 450. | ||||
| РЕЗУЛЬТАТЫ: |
ВЫВОД:
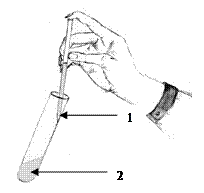 |
Рис. 2. Наслаивание пробы на концентрированную кислоту:
1 -раствор белка; 2-кислота.
III.2. Контрольные вопросы.
Какие факторы удерживают белки в растворе?
Чем обусловлена реакция осаждения белков?
Что такое коагуляция белков? Виды коагуляции.
Что такое денатурация белка? Виды денатурации.
При каких условиях происходит: коагуляция
с денатурацией; коагуляция без денатурации;
денатурация без коагуляции?
Что такое адсорбционная пептизация?
Как используется в медицине реакция адсорбционной
пептизации?
Материал для самоподготовки: I а)1. с.19-74, 662-565. II, III.
РАЗДЕЛ II. ФЕРМЕНТЫ
Занятие № 4
ТЕМА. СТРОЕНИЕ И ОСНОВНЫЕ
СВОЙСТВА ФЕРМЕНТОВ
Цель занятия: 1.Повторить материал по физико-химическим
свойствам белков.
2.Ознакомиться с современными представлениями о структу-
ре ферментов, изучить их характерные свойства.
Исходный уровень знаний:
- строение и физико-химические свойства белков;
- понятие о катализаторах.
Содержание занятия.
I.2. Понятие о катализе.
Химическая природа ферментов.
Свойства ферментов.
Строение ферментов (функциональные центры, их строение).
Факторы, определяющие активность ферментов.
Витамины как коферменты.
Понятие об изоферментах.
Мультимолекулярные ферментные системы.
II.1.Работа № 1.ВЛИЯНИЕ ТЕМПЕРАТУРЫ НА
АКТИВНОСТЬ АМИЛАЗЫ СЛЮНЫ
Принцип метода и химизм.
Амилаза слюны (a-1,4-гликозидаза) катализирует гидролиз a-1,4-гликозидной связи крахмала и гликогена до дисахарида мальтозы с промежуточным образованием декстринов различного размера. Нерасщепленный крахмал с йодом дает синее окрашивание, амилодекстрины - фиолетовое, эритродекстрины - красно-бурое, ахродекстрины и мальтоза - желтое (цвет водного раствора йода, т.е. окрашивания с йодом не дают). Конечные продукты гидролиза крахмала - мальтоза и глюкоза - имеют свободную альдегидную группу и могут быть обнаружены реакцией Троммера, в основе которой лежит окислительно-восстановительная реакция. При нагревании альдегидная группа окисляется до глюконовой кислоты, а медь гидрата окиси меди (голубого цвета) - восстанавливается в гидрат закиси меди (желтого цвета). При дальнейшем нагревании образуется красная закись меди:
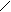
 H O
H O

 C=O + 2CuSO4 + 5NaOН ® C–O–Na + 2CuOH + 2Na2SO4 + 2H2O
C=O + 2CuSO4 + 5NaOН ® C–O–Na + 2CuOH + 2Na2SO4 + 2H2O
 R R
R R
Одним из характерных свойств ферментов является термолабильность, т.е. чувствительность фермента к температуре. Для многих ферментов максимальная ферментативная скорость наблюдается при 38-400C. Эта температура называется температурным оптимумом. При нагревании свыше 700С они утрачивают свои свойства биологических катализаторов. Степень инактивирования зависит от длительности теплового воздействия. Замедление и прекращение ферментативной реакции происходит вследствие тепловой денатурации белковой молекулы фермента. При низких температурах ферменты не денатурируются, но скорость реакции резко снижается за счет снижения кинетической энергии молекул. О действии фермента судят по исчезновению субстрата или появлению продуктов реакции.
Порядок выполнения работы:
В чистую пробирку собрать примерно 2 мл нативной (неразведенной) слюны и кипятить в течение 5 минут, охладить.
| Реагенты (кап.) | Пробирки | ||
| 1-я | 2-я | 3-я | |
| 1% раствор крахмала | |||
| Нативная слюна, разведенная в 10 раз | - | - | |
| Прокипяченная неразведенная слюна | - | - | |
| Дистиллированная вода | - | - | |
| Поместить в термостат при 380С на 10 мин. Из содержимого каждой пробирки отлить по 5 капель в дополнительные пробирки. а) йодная проба (на крахмал) | |||
| Реагенты (кап.) | Пробирки | ||
| 1-а | 2-а | 3-а | |
| Исследуемый раствор | |||
| Раствор йода в йодистом калии | |||
| РЕЗУЛЬТАТЫ: | |||
| б) реакция Троммера (на глюкозу и мальтозу) | |||
| Реагенты (кап.) | 1-б | 2-б | 3-б |
| Исследуемый раствор | |||
| 10% раствор NаОН | |||
| 1% раствор CuSO4 | |||
| РЕЗУЛЬТАТЫ: |
ВЫВОД:
Работа № 2. ВЛИЯНИЕ РЕАКЦИИ СРЕДЫ НА АКТИВ-
НОСТЬ ФЕРМЕНТОВ И ОПРЕДЕЛЕНИЕ
ОПТИМУМА рН
Принцип метода и химизм.
Для разных ферментов существует свой оптимум рН среды, когда фермент наиболее активен. Например, оптимум рН пепсина (фермент желудочного сока) - 1,5-2,0; аргиназы (фермент печени) - 9,5. Для амилазы слюны оптимум рН - 6,8-7.2; в кислой и щелочной среде активность ее снижается за счет взаимодействия белковой молекулы с ионами раствора.
Химизм реакции см. выше (раб. N1).
Порядок выполнения работы:
Слюну развести в 10 раз. Взять 5 пробирок и приготовить смеси в соответствии с таблицей (все растворы берутся в каплях).
| Реактивы | Пробирки | ||||
| 1 | 2 | 3 | 4 | 5 | |
| раствор 1 | |||||
| раствор 2 | |||||
| 1% раствор NaCl | |||||
| рН | 5,8 | 6,9 | 7,4 | 7,9 | 8,5 |
| 0,5% раствор крахмала | |||||
| Слюна разведенная | |||||
| Перемешать, поместить в термостат при температуре 380С на 10 минут | |||||
| раствор йода | |||||
| Окраска | |||||
| Продукты гидролиза крахмала |
ВЫВОД:
Работа № 3. СПЕЦИФИЧНОСТЬ ДЕЙСТВИЯ
АМИЛАЗЫ СЛЮНЫ
Принцип метода.
Ферменты обладают специфичностью, т.к. способны катализировать только определённые химические реакции. Специфичность действия ферментов бывает абсолютная, относительная и стереохимическая. Она определяется тем, что только некоторые строго определённые функциональные группы, входящие в состав ферментов, могут участвовать в образовании фермент-субстратных комплексов.
Амилаза слюны ускоряет гидролиз только полисахаридов, не оказывая действия на дисахариды. Мальтаза слюны ускоряет гидролиз образующегося дисахарида мальтозы и не оказывает действия на сахарозу.
Химизм реакции см. в работе N 1.
Порядок выполнения работы:
| Реактивы (кап.) | 1-я пробирка | 2-я пробирка |
| Слюна, разведенная 1:5 | ||
| 1% раствор крахмала | - | |
| 1% раствор сахарозы | - | |
| Поместить в термостат при температуре 380С на 10 минут | ||
| Реактив Фелинга | ||
| Нагреть до кипения и кипятить 1 мин | ||
| РЕЗУЛЬТАТЫ: |
ВЫВОД:
III.2. Контрольные вопросы.
Как и почему активность ферментов зависит от температуры?
Что такое температурный оптимум ферментов?
Как и почему активность ферментов зависит от рН среды
(график)?
Какие ферменты активны в кислой; нейтральной;
щелочной среде?
Что такое специфичность ферментов?
Какие виды специфичности ферментов Вы знаете?
Примеры.
Укажите качественную реакцию на крахмал.
Материал для самоподготовки: I а) 1. с.44-49, 114-129,
139-143; II; III.
Занятие № 5
ТЕМА. МЕХАНИЗМ ДЕЙСТВИЯ ФЕРМЕНТОВ,
КИНЕТИКА ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ
Цель занятия: Ознакомиться с современными представлениями о механизме действия ферментов и кинетике ферментативных реакций.
Исходный уровень знаний:
- белковая природа ферментов;
- структура сложных ферментов;
- строение молекулы фермента;
- кинетика химических реакций.
Содержание занятия.
I.2. Современные представления о механизме действия ферментов (гипотеза Фишера, Кошланда).
Полифункциональный катализ.
Кинетика ферментативных реакций. Константа Михаэлиса.
Зависимость активности ферментов от различных факторов.
Определение активности ферментов: принцип, значение в медицине.
II.1. Работа № 1. АКТИВНОСТЬ a - АМИЛАЗЫ СЛЮНЫ.
Принцип метода.
Метод основан на определении наименьшего количества амилазы (при максимальном разведении слюны), полностью расщепляющего весь добавленный крахмал. Амилазная активность слюны выражается количеством (в мл) 0,1% раствора крахмала, которое расщепляется 1 мл неразведенной слюны при температуре 380С в течение 30 минут. В норме амилазная активность равна 160 - 320. Амилазная активность обозначается А 380/30'. Этот метод широко используется для определения амилазной активности крови и мочи.
Порядок выполнения работы:
В 10 пробирок налить по 1 мл воды. В 1-ю пробирку добавить 1 мл слюны, разведённой в 10 раз. Содержимое пробирки перемешать несколько раз, втягивая и выпуская жидкость из пипетки. Набрать в пипетку 1,0 мл смеси и перенести её во 2-ю пробирку. Содержимое тоже перемешать и 1,0 мл перенести в 3-ю пробирку и т. д. до 10 пробирки. Из 10-ой пробирки 1,0 мл смеси вылить.
| 1 мл слюны |
| 1 мл смеси |
  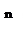 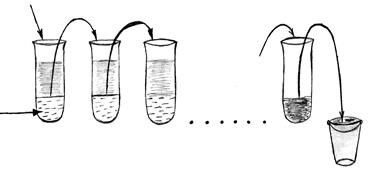 |
Рис. 3. Разведение слюны
Во все пробирки добавить по 1,0 мл воды и по 2,0 мл 0,1% раствора крахмала, встряхивая, перемешать и поместить в термостат при 380С на 30 минут. После инкубации пробирки охладить водопроводной водой, добавить по 1 капле 0,1% раствора йода и перемешать. Отметить окраску в каждой пробирке и, пользуясь таблицей, сделать расчет.
Расчет: отметить пробирку, где гидролиз крахмала прошел полностью при наименьшем количестве фермента и по количеству неразведённой слюны (А) в данной пробирке рассчитать амилазную активность (Х) следующим образом:
А мл слюны расщепили 2,0 мл 0,1% раствора крахмала.
1 мл слюны расщепил Х мл раствора крахмала.
В 3-й пробирке, например, А =1/80 мл.
| Пробирки | ||||||||||
| Разведение слюны | ||||||||||
| Окраска р-ра с йодом |
ВЫВОД:
Работа № 2. АКТИВНОСТЬ АМИЛАЗЫ
(ДИАСТАЗЫ) МОЧИ
Принцип метода.
Метод основан на определении времени, необходимого для полного расщепления крахмала в присутствии 1 мл мочи. Условно за единицу активности амилазы мочи принимают количество фермента, расщепляющего 2 мг крахмала за 15 минут. Активность амилазы выражают количеством единиц в 1 мл мочи. В норме она составляет 1-2 ЕД, а по методу Вольгемута колеблется от 16 до 64 ЕД.
Моча здоровых людей обладает низкой амилазной активностью по сравнению с амилазой слюны. Определение активности a-амилазы в моче и сыворотке крови широко используется в клинике при диагностике заболеваний поджелудочной железы. В первые сутки заболевания амилазная активность увеличивается в моче и сыворотке крови в десятки раз, а затем постепенно возвращается к норме. При почечной недостаточности амилаза в моче отсутствует.
В детском возрасте увеличение активности амилазы наблюдается при эндемическом паротите, что указывает на одновременное поражение поджелудочной железы вирусом паротита. Вирус гриппа также поражает поджелудочную железу, но реже.
Порядок выполнения работы.
На сухую чашку Петри капнуть в разных местах по 1 капле 0,1% раствора йода в йодиде калия (всего 8-10 капель). В пробирку внести 2 мл 0,1% раствора крахмала, содержащего 2 мг крахмала, 1 мл 0,85% р-ра хлорида натрия и поместить пробирку в термостат при 370С на 2 минуты. Через 2 минуты добавить в пробирку 0,5 мл мочи, перемешать и отметить время начала реакции. Затем каждые 2-3 минуты переносить каплю смеси из пробирки на чашку Петри в каплю раствора йода до появления желтой (или бесцветной) окраски и отметить время реакции в минутах. Активность амилазы мочи рассчитать по формуле:
15
 Х =
Х =
Т ∙ 0,5
где Х - активность амилазы в 1 мл мочи;
15 - время, необходимое для полного расщепления 2 мг крахмала в минутах;
0,5 - количество мочи, взятое в реакционную смесь в мл;
Т - время реакции в минутах.
РЕЗУЛЬТАТ:
ВЫВОД:
III.2. Контрольные вопросы.
Какую реакцию катализирует амилаза?
Укажите промежуточные и конечные продукты гидролиза
крахмала.
Чему равна в норме диастаза мочи?
При каких заболеваниях повышается активность диастазы
мочи (у взрослых и детей)?
Когда в моче отсутствует амилаза?
Напишите формулы витаминов В2 и РР, укажите
соответствующие коферменты.
Материал для самоподготовки: Iа) 1. с.129-139, 143-152; II; III
Занятие № 6
ТЕМА. РЕГУЛЯЦИЯ АКТИВНОСТИ ФЕРМЕНТОВ.
КЛАССИФИКАЦИЯ, НОМЕНКЛАТУРА И
ПРАКТИЧЕСКОЕ ПРИМЕНЕНИЕ ФЕРМЕНТОВ.
Цель занятия: Ознакомиться со способами регуляции ферментов in vivo, принципами количественной характеристики, классификации, номенклатуры ферментов, применением их в медицине.
Исходный уровень знаний:
- строение холоферментов;
- специфичность действия ферментов;
- механизм образования фермент-субстратного комплекса;
- зависимость активности ферментов от различных факторов.
Содержание занятия.
I.2. Факторы, регулирующие активность ферментов in vivo.
Активирование ферментов, его виды.
Типы ингибирования ферментов.
Классы ферментов, примеры.
Номенклатура ферментов.
Разделы медицинской энзимологии, примеры.
Иммобилизованные ферменты.
Ферменты плазмы крови.
II.1. Работа № 1. ВЛИЯНИЕ АКТИВАТОРОВ И ИНГИБИТО-
РОВ НА АКТИВНОСТЬ АМИЛАЗЫ СЛЮНЫ
Принцип метода и химизм.
Активаторы стимулируют действие ферментов, но не принимают участия в реакции. Активаторы некоторых ферментов: для амилазы слюны - хлорид натрия; для пепсина - ионы Н+ хлористо-водородной кислоты; для липазы - желчные кислоты; для аденозинтрифосфатазы - Мg++, Mn++.
Ингибиторы тормозят действие ферментов вплоть до полной остановки реакции. Ингибиторами часто являются продукты промежуточных или конечных реакций какого-либо биохимического процесса. Примеры ингибиторов: ДФФ (диизопропилфторфосфат) - для холинэстеразы и трипсина; синильная кислота - для цитохромоксидазы; малоновая кислота - для сукцинатдегидрогеназы; сульфат меди - для амилазы слюны.
Активаторы и ингибиторы изменяют активность фермента, влияя на его активный или аллостерический центр.
