Увеличение ферментами стерического коэффициента
Стерический коэффициент вводится для реакций, в которых участвуют крупные молекулы, имеющие пространственную структуру. Стерический коэффициент показывает долю удачных пространственно соответствующих столкновений активных молекул. Например, он равен 0,4, если 4 из 10 столкновений активных молекул привели к образованию продукта реакции.
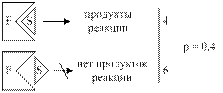
Ферменты увеличивают стерический коэффициент, так как они изменяют строение молекулы субстрата в фермент - субстратном комплексе, в результате чего комплементарность фермента и субстрата возрастает. Кроме того, ферменты за счёт своих активных центров упорядочивают расположение молекул субстрата в пространстве (до взаимодействия с ферментом молекулы субстрата располагаются хаотично) и облегчают протекание реакции.
Номенклатура ферментов
Ферменты имеют несколько типов названий.
1) Тривиальные названия (трипсин, пепсин).
2) Рабочая номенклатура. В данном названии фермента присутствует окончание – аза, которое прибавляется:
· к названию субстрата (сахараза, амилаза);
· к виду связи, на которую действует фермент (пептидаза, гликозидаза);
· к типу реакции, процесса (синтетаза, гидролаза).
3) У каждого фермента есть классификационное название, в котором отражается тип реакции, вид субстрата и кофермента. Например: ЛДГ – L лактат-НАД+ - оксидоредуктаза.
Классификация ферментов
Классификация ферментов разработана в 1961 году. Согласно классификации каждый фермент расположен в определённом классе, подклассе, подподклассе и имеет порядковый номер. В связи с этим каждый фермент имеет цифровой шифр, в котором первая цифра обозначает класс, вторая – подкласс, третья – подподкласс, четвертая – порядковый номер (ЛДГ: 1.1.1.27.). Все ферменты классифицируются на 6 классов:
- Оксидоредуктазы.
- Трансферазы.
- Гидролазы.
- Лиазы.
- Изомеразы.
- Синтетазы (лигазы).
Оксидоредуктазы
Ферменты, катализирующие окислительно - востановительные процессы. Общий вид реакции: Аок + Ввос = Авост + Вок. Этот класс ферментов включает несколько подклассов:
1. Дегидрогиназы, катализируют реакции путём отщепления водорода от окисляемого вещества. Они могут быть аэробными (переносят водород на кислород) и анаэробными (переносят водород не на кислород, а на какое-то другое вещество).
2. Оксигеназы - ферменты катализирующие окисление путём присоединения кислорода к окисляемому веществу. Если присоединяется один атом кислорода, участвуют монооксигеназы, если два атома кислорода – диоксигеназы.
3. Пероксидазы – ферменты, катализирующие окисление веществ с участием пероксидов.
Трансферазы
Ферменты, осуществляющие внутримолекулярный и межмолекулярный перенос функциональных групп с одного вещества на другое по схеме: АВ + С = А + ВС. Подклассы трансфераз выделяют в зависимости от вида переносимых групп: аминотрансферазы, метилтрансферазы, сульфотрансферазы, ацилтрансферазы (переносят остатки жирных кислот), фосфотрансферазы (переносят остатки фосфорной кислоты).
Гидролазы
Ферменты данного класса катализируют разрыв химической связи с присоединением воды по месту разрыва, то есть реакции гидролиза по схеме: АВ + НОН = АН + ВОН. Подклассы гидролаз выделяют в зависимости от вида разрываемых связей: пептидазы расщепляют пептидные связи (пепсин), гликозидазы - гликозидные связи (амилаза), эстеразы – сложноэфирные связи (липаза).
Лиазы
Лиазы катализируют разрыв химической связи без присоединения воды по месту разрыва. При этом в субстратах образуются двойные связи по схеме: АВ = А + В. Подклассы лиаз зависят от того, между какими атомами разрывается связь и какие вещества образуются. Альдолазы катализируют разрыв связи между двумя атомами углерода (например, фруктоза 1,6-ди-фосфатальдолаза «разрезает» фруктозу на две фосфотриозы). К лиазам относят ферменты декарбоксилазы (отщепляют углекислый газ), дегидратазы («вырезают» молекулы воды).
Изомеразы
Изомеразы катализируют взаимопревращения различных изомеров. Например, фосфогексоизимераза переводит эфиры фруктозы в эфиры глюкозы. К подклассам изомераз относятся мутазы (фосфоглюкомутаза переводит глюкозо- 1- фосфат в глюкозо-6-фосфат), эпимеразы (например, переводят рибозу в ксилулозу), таутомеразы
Синтетазы (лигазы).
Ферменты данного класса катализируют реакции синтеза новых веществ за счёт энергии АТФ по схеме: А + В + АТФ = АВ. Например, глютаминсинтетаза катализирует взаимодействие глютаминовой кислоты с NH3, при участии АТФ с образованием глютамина.
Свойства ферментов
Ферменты, помимо общих свойств с неорганическими катализаторами имеют определённые отличия от неорганических катализаторов. К ним относятся: более высокая активность, более высокая специфичность, более мягкие условия для катализа, способность к регуляции активности.
