Объем и физико-химические свойства крови
Объем крови – общее количество крови в организме взрослого человека составляет в среднем 6 – 8% от массы тела, что соответствует 5 – 6 л. Повышение общего объема крови называют гиперволемией, уменьшение – гиповолемией.
Относительная плотность крови – 1,050 – 1.060 зависит в основном от количества эритроцитов. Относительная плотность плазмы крови – 1.025 – 1.034, определяется концентрацией белков.
Вязкость крови – 5 усл.ед., плазмы – 1,7 – 2,2 усл.ед., если вязкость воды принять за 1. Обусловлена наличием в крови эритроцитов и в меньшей степени белков плазмы.
Осмотическое давление крови – сила, с которой растворитель переходит через полунепроницаемую мембрану из менее в более концентрированный раствор. Осмотическое давление крови вычисляют криоскопическим методом путем определения точки замерзания крови (депрессии), которая для нее равна 0,56 – 0,58 С. Осмотическое давление крови в среднем составляет 7,6 атм. Оно обусловлено растворенными в ней осмотически активными веществами, главным образом неорганическими электролитами, в значительно меньшей степени – белками. Около 60% осмотического давления создается солями натрия (NаСl).
Осмотическое давление определяет распределение воды между тканями и клетками. Функции клеток организма могут осуществляться лишь при относительной стабильности осмотического давления. Если эритроциты поместить в солевой раствор, имеющий осмотическое давление, одинаковое с кровью, они не изменяют свой объем. Такой раствор называют изотоническим, или физиологическим. Это может быть 0,85% раствор хлористого натрия. В растворе, осмотическое давление которого выше осмотического давления крови, эритроциты сморщиваются, так как вода выходит из них в раствор. В растворе с более низким осмотическим давлением, чем давление крови, эритроциты набухают в результате перехода воды из раствора в клетку. Растворы с более высоким осмотическим давлением, чем давление крови, называются гипертоническими, а имеющие более низкое давление – гипотоническими.
Онкотическое давление крови – часть осмотического давления, создаваемого белками плазмы. Оно равно 0,03 – 0,04 атм, или 25 – 30 мм рт.ст. Онкотическое давление в основном обусловлено альбуминами. Вследствие малых размеров и высокой гидрофильности они обладают выраженной способностью притягивать к себе воду, за счет чего она удерживается в сосудистом русле, При снижении онкотического давления крови происходит выход воды из сосудов в интерстициальное пространство, что приводит к отеку тканей.
Кислотно-основное состояние крови (КОС). Активная реакция крови обусловлена соотношением водородных и гидроксильных ионов. Для определения активной реакции крови используют водородный показатель рН – концентрацию водородных ионов, которая выражается отрицательным десятичным логарифмом молярной концентрации ионов водорода. В норме рН – 7,36 (реакция слабоосновная); артериальной крови – 7,4; венозной – 7,35. При различных физиологических состояниях рН крови может изменяться от 7,3 до 7,5. Активная реакция крови является жесткой константой, обеспечивающей ферментативную деятельность. Крайние пределы рН крови, совместимые с жизнью, равны 7,0 – 7,8. Сдвиг реакции в кислую сторону называется ацидозом, который обусловливается увеличением в крови водородных ионов. Сдвиг реакции крови в щелочную сторону называется алкалозом. Это связано с увеличением концентрации гидроксильных ионов ОН и уменьшением концентрации водородных ионов.
В организме человека всегда имеются условия для сдвига активной реакции крови в сторону ацидоза или алкалоза, которые могут привести к изменению рН крови. В клетках тканей постоянно образуются кислые продукты. Накоплению кислых соединений способствует потребление белковой пищи. Напротив, при усиленном потреблении растительной пищи в кровь поступают основания. Поддержание постоянства рН крови является важной физиологической задачей и обеспечивается буферными системами крови. К буферным системам крови относятся гемоглобиновая, карбонатная, фосфатная и белковая.
Буферные системы нейтрализуют значительную часть поступающих в кровь кислот и щелочей, тем самым препятствуя сдвигу активной реакции крови. В организме в процессе метаболизма в большей степени образуется кислых продуктов. Поэтому запасы щелочных веществ в крови во много раз превышают запасы кислых, Их рассматривают как щелочной резерв крови.
Гемоглобиновая буферная система на 75% обеспечивает буферную емкость крови. Оксигемоглобин является более сильной кислотой, чем восстановленный гемоглобин. Оксигемоглобин обычно бывает в виде калиевой соли. В капиллярах тканей в кровь поступает большое количество кислых продуктов распада. Одновременно в тканевых капиллярах при диссоциации оксигемоглобина происходит отдача кислорода и появление большого количества щелочно реагирующих солей гемоглобина, Последние взаимодействуют с кислыми продуктами распада, например угольной кислотой. В результате образуются бикарбонаты и восстановленный гемоглобин, В легочных капиллярах гемоглобин, отдавая ионы водорода, присоединяет кислород и становится сильной кислотой, которая связывает ионы калия. Ионы водорода используются для образования угольной кислоты, в дальнейшем выделяющейся из легких в виде Н2О и СО2.
Карбонатная буферная система по своей мощности занимает второе место. Она представлена угольной кислотой (Н2СО3) и бикарбонатом натрия или калия (NaНСО3, КНСО3) в пропорции 1/20. Если в кровь поступает кислота, более сильная, чем угольная, то в реакцию вступает, например, бикарбонат натрия. Образуются нейтральная соль и слабодиссоциированная угольная кислота. Угольная кислота под действием карбоангидразы эритроцитов распадается на Н2О и СО2, последний выделяется легкими в окружающую среду. Если в кровь поступает основание, то в реакцию вступает угольная кислота, образуя гидрокарбонат натрия и воду. Избыток бикарбоната натрия удаляется через почки. Бикарбонатный буфер широко используется для коррекции нарушений кислотно-основного состояния организма.
Фосфатная буферная система состоит из натрия дигидрофосфата (NаН2РО4) и натрия гидрофосфата (Nа2НРО4). Первое соединение обладает свойствами слабой кислоты и взаимодействует с поступившими в кровь щелочными продуктами. Второе соединение имеет свойства слабой щелочи и вступает в реакцию с более сильными кислотами.
Белковая буферная система осуществляет роль нейтрализации кислот и щелочей благодаря амфотерным свойствам: в кислой среде белки плазмы ведут себя как основания, в основной – как кислоты.
Буферные системы имеются и в тканях, что способствует поддержанию рН тканей на относительно постоянном уровне. Главными буферами тканей являются белки и фосфаты.
Поддержание рН осуществляется также с помощью легких и почек. Через легкие удаляется избыток углекислоты. Почки при ацидозе выделяют больше кислого одноосновного фосфата натрия, а при алкалозе – больше щелочных солей: двухосновного фосфата натрия и бикарбоната натрия.
Эритропоэз
Образование эритроцитов, или эритропоэз, происходит в красном костном мозге. Эритроциты вместе с кроветворной тканью носят название “красного ростка крови”, или эритрона.
Для образования эритроцитов требуются железо и ряд витаминов.
Железо организм получает из гемоглобина разрушающихся эритроцитов и с пищей. Трехвалентное железо пищи с помощью вещества, находящегося в слизистой кишечника, превращается в двухвалентное железо. С помощью белка трансферрина железо, всосавшись, транспортируется плазмой в костный мозг, где оно включается в молекулу гемоглобина. Избыток железа депонируется в печени в виде соединения с белком – ферритина или с белком и липоидом – гемосидерина. При недостатке железа развивается железодефицитная анемия.
Для образования эритроцитов требуются витамин В12 (цианокобаламин) и фолиевая кислота. Витамин В12 поступает в организм с пищей и называется внешним фактором кроветворения. Для его всасывания необходимо вещество (гастромукопротеид), которое вырабатывается железами слизистой оболочки пилорического отдела желудка и носит название внутреннего фактора кроветворения Касла. При недостатке витамина В12 развивается В12-дефицитная анемия, Это может быть или при недостаточном его поступлении с пищей (печень, мясо, яйца, дрожжи, отруби), или при отсутствии внутреннего фактора (резекция нижней трети желудка). Считается, что витамин В12 способствует синтезу глобина, Витамин В12 и фолиевая кислота участвуют в синтезе ДНК в ядерных формах эритроцитов. Витамин В2 (рибофлавин) необходим для образования липидной стромы эритроцитов. Витамин В6 (пиридоксин) участвует в образовании гема. Витамин С стимулирует всасывание железа из кишечника, усиливает действие фолиевой кислоты. Витамин Е (a -токоферол) и витамин РР (пантотеновая кислота) укрепляют липидную оболочку эритроцитов, защищая их от гемолиза.
Для нормального эритропоэза необходимы микроэлементы. Медь помогает всасыванию железа в кишечнике и способствует включению железа в структуру гема. Никель и кобальт участвуют в синтезе гемоглобина и гемсодержащих молекул, утилизирующих железо. В организме 75% цинка находится в эритроцитах в составе фермента карбоангидразы. Недостаток цинка вызывает лейкопению. Селен, взаимодействуя с витамином Е, защищает мембрану эритроцита от повреждения свободными радикалами.
Физиологическими регуляторами эритропоэза являются эритропоэтины, образующиеся главным образом в почках, а также в печени, селезенке и в небольших количествах постоянно присутствующие в плазме крови здоровых людей. Эритропоэтины усиливают пролиферацию клеток-предшественников эритроидного ряда – КОЕ-Э (колониеобразующая единица эритроцитарная) и ускоряют синтез гемоглобина. Они стимулируют синтез информационной РНК, необходимой для образования энзимов, которые участвуют в формировании гема и глобина. Эритропоэтины увеличивают также кровоток в сосудах кроветворной ткани и увеличивают выход в кровь ретикулоцитов. Продукция эритропоэтинов стимулируется при гип 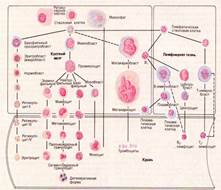 оксии различного происхождения: пребывание человека в горах, кровопотеря, анемия, заболевания сердца и легких. Эритропоэз активируется мужскими половыми гормонами, что обусловливает большее содержание эритроцитов в крови у мужчин, чем у женщин. Стимуляторами эритропоэза являются соматотропный гормон, тироксин, катехоламины, интерлейкины. Торможение эритропоэза вызывают особые вещества – ингибиторы эритропоэза, образующиеся при увеличении массы циркулирующих эритроцитов, например у спустившихся с гор людей. Тормозят эритропоэз женские половые гормоны (эстрогены), кейлоны. Симпатическая нервная система активирует эритропоэз, парасимпатическая – тормозит. Нервные и эндокринные влияния на эритропоэз осуществляются, по-видимому, через эритропоэтины.
оксии различного происхождения: пребывание человека в горах, кровопотеря, анемия, заболевания сердца и легких. Эритропоэз активируется мужскими половыми гормонами, что обусловливает большее содержание эритроцитов в крови у мужчин, чем у женщин. Стимуляторами эритропоэза являются соматотропный гормон, тироксин, катехоламины, интерлейкины. Торможение эритропоэза вызывают особые вещества – ингибиторы эритропоэза, образующиеся при увеличении массы циркулирующих эритроцитов, например у спустившихся с гор людей. Тормозят эритропоэз женские половые гормоны (эстрогены), кейлоны. Симпатическая нервная система активирует эритропоэз, парасимпатическая – тормозит. Нервные и эндокринные влияния на эритропоэз осуществляются, по-видимому, через эритропоэтины.
Об интенсивности эритропоэза судят по числу ретикулоцитов – предшественников эритроцитов. В норме их количество составляет 1 – 2%. Созревшие эритроциты циркулируют в крови в течение 100 – 120 дней.
Разрушение эритроцитов происходит в печени, селезенке, в костном мозге посредством клеток мононуклеарной фагоцитарной системы. Продукты распада эритроцитов также являются стимуляторами кроветворения.
Лейкопоэз
Все лейкоциты образуются в красном костном мозге из единой стволовой клетки. Предшественники лимфоцитов первыми ответвляются от общего древа стволовых клеток; формирование лимфоцитов происходит во вторичных лимфатических органах.
Лейкопоэз стимулируется специфическими ростовыми факторами, которые воздействуют на определенные предшественники гранулоцитарного и моноцитарного рядов. Продукция гранулоцитов стимулируется гранулоцитарным колониестимулирующим фактором (КСФ-Г), образующимся в моноцитах, макрофагах, Т-лимфоцитах, а угнетается – кейлонами и лактоферрином, секретируемыми зрелыми нейтрофилами; простагландинами Е. Моноцитопоэз стимулируется моноцитарным колониестимулирующим фактором (КСФ-М), катехоламинами. Простагландины Е, a - и b -интерфероны, лактоферрин тормозят продукцию моноцитов. Большие дозы гидрокортизона препятствуют выходу моноцитов из костного мозга. Важная роль в регуляции лейкопоэза принадлежит интерлейкинам. Одни из них усиливают рост и развитие базофилов (ИЛ-3) и эозинофилов (ИЛ-5), другие стимулируют рост и дифференцировку Т- и В-лимфоцитов (ИЛ-2,4,6,7). Лейкопоэз стимулируют продукты распада самих лейкоцитов и тканей, микроорганизмы и их токсины, некоторые гормоны гипофиза, нуклеиновые кислоты,
Жизненный цикл разных видов лейкоцитов различен, Одни живут часы, дни, недели, другие на протяжении всей жизни человека.
Лейкоциты разрушаются в слизистой оболочке пищеварительного тракта, а также в ретикулярной ткани.
Тромбоциты
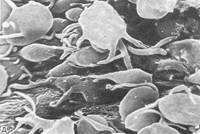 Тромбоциты, или кровяные пластинки – плоские клетки неправильной округлой формы диаметром 2 – 5 мкм. Тромбоциты человека не имеют ядер. Количество тромбоцитов в крови человека составляет 180 – 320х10'/л, или 180 000 – 320 000 в 1 мкл. Имеют место суточные колебания: днем тромбоцитов больше, чем ночью. Увеличение содержания тромбоцитов в периферической крови называется тромбоцитозом, уменьшение – тромбоцитопенией.
Тромбоциты, или кровяные пластинки – плоские клетки неправильной округлой формы диаметром 2 – 5 мкм. Тромбоциты человека не имеют ядер. Количество тромбоцитов в крови человека составляет 180 – 320х10'/л, или 180 000 – 320 000 в 1 мкл. Имеют место суточные колебания: днем тромбоцитов больше, чем ночью. Увеличение содержания тромбоцитов в периферической крови называется тромбоцитозом, уменьшение – тромбоцитопенией.
Рис 5. Тромбоциты, прилипшие к стенке аорты в зоне повреждения эндотелиального слоя.
Главной функцией тромбоцитов является участие в гемостазе. Тромбоциты способны прилипать к чужеродной поверхности (адгезия), а также склеиваться между собой ~агрегация) под влиянием разнообразных причин. Тромбоциты продуцируют и выделяют ряд биологически активных веществ: серотонин, адреналин, норадреналин, а также вещества, получившие название пластинчатых факторов свертывания крови. Тромбоциты способны выделять из клеточных мембран арахидоновую кислоту и превращать ее в тромбоксаны, которые, в свою очередь, повышают агрегационную активность тромбоцитов. Эти реакции происходят под действием фермента циклооксигеназы. Тромбоциты способны к передвижению за счет образования псевдоподий и фагоцитозу инородных тел, вирусов, иммунных комплексов, тем самым, выполняя защитную функцию. Тромбоциты содержат большое количество серотонина и гистамина, которые влияют на величину просвета и проницаемость капилляров, определяя тем самым состояние гистогематических барьеров.
Тромбоциты образуются в красном костном мозге из гигантских клеток мегакариоцитов. Продукция тромбоцитов регулируется тромбоцитопоэтинами. Тромбоцитопоэтины образуются в костном мозге, селезенке, печени. Различают тромбоцитопоэтины кратковременного и длительного действия. Первые усиливают отщепление тромбоцитов от мегакариоцитов и ускоряют их поступление в кровь. Вторые способствуют дифференцировке и созреванию мегакариоцитов.
Активность тромбоцитопоэтинов регулируется интерлейкинами (ИЛ-6 и ИЛ-11). Количество тромбоцитопоэтинов повышается при воспалении, необратимой агрегации тромбоцитов, Продолжительность жизни тромбоцитов составляет от 5 до 11 дней. Разрушаются кровяные пластинки в клетках системы макрофагов.
