Трепетание и фибрилляция желудочков.
Это беспорядочные неэффективные сокращения отдельных пучков волокон миокарда с высокой частотой.
Трепетание – регулярные волны – «пила», нет изолинии, 180-250-в мин., желудочковые комплексы не дифференцируются.
Фибрилляция – высокая частота желудочковых сокращений, более 300 в мин., абсолютно разные волны, разной продолжительности и амплитуды, отсутствие дифференцированных элементов ЭКГ.
III. Нарушение функции проводимости(синоатриальные, внутрипредсердные, атриовентрикулярные, внутрижелудочковые блокады).
Замедление или полное прекращение проведения электрического импульса по какому-либо отделу проводящей системы получило название блокады сердца.
Синоатриальная блокада – это нарушение проведения электрического импульса от синусового узла к предсердиям.
ЭКГ. 1 и 3 степень блокады этим методом не могут быть установлены. Блокада 1 степени распознается только специальными электрофизиологическими методами. При блокаде 2 степени периодически выпадают отдельные сердечные циклы (з.Р и QRS). В момент таких выпадений на ЭКГ регистрируется длинная пауза, превышающая обычные интервалы в –R –R в 2-3-4 раза, если выпадают 2-3 или 4 цикла подряд.
Атриовентрикулярные блокады: - это нарушение проведения импульса от предсердий к желудочкам на уровне A-V узла.
Различают 3 степени AV блокады:
АВ-блокада 1 степени–замедление предсердно-желудочковой проводимости, на ЭКГ- удлинение интервала РQ более 0,2 сек..
АВ-блокада 2 степени – некоторые импульсы не проводятся от предсердий к желудочкам и выпадает часть желудочковых комплексов.. Если перед выпадением комплекса QRS интервал РQ постепенно удлиняется такую блокаду называют АВ-блокадой 2 степени 1 типа с периодами Самойлова –Венкебаха, Мобитц 1). В других случаях периодически выпадает желудочковый комплекс, но интервал РQ стабилен-АВ-блокада 2 степени 2 типа (Мобитц 2).
АВ-блокада 3 степени –полная-импульс от предсердий не проводится к желудочкам, они функционируют независимо друг от друга – з.Р в своем ритме, более частом, чем комплексы QRS (частота желудочковых сокращений менее 60 в мин.). Предсердия возбуждаются из синусового узла, а желудочки из атриовентрикулярного узла или эктопических очагов автоматизма II или III порядка. Может развится выраженная брадикардия с неэффективной гемодинамикой. На ЭКГ наблюдается полная диссоциация между зубцами Р и комплексами QRS.
ЭКГ-диагностика ишемической болезни сердца (стенокардия и инфаркт миокарда).
Появляющиеся изменения ЭКГ неспецифичны для хронической ишемической болезни сердца и хронической коронарной недостаточности и наблюдаются также при различных заболеваниях.
Поэтому четкие объективные электрокардиографические критерии хронической ишемической болезни сердца в большинстве случаев отсутствуют и диагноз ставят на основании комплекса клинических и электрокардиографических данных с применением различных функциональных проб.
Следует учитывать, что у 30 – 85% больных с заведомо установленной хронической ишемической болезнью сердца ЭКГ может быть совершенно нормальной. Естественно, что диагнозу значительно помогают перенесенный в анамнезе инфаркт миокарда или очаговые изменения миокарда. Диагностика также облегчается при жалобах больного на типичные, особенно частые приступы стенокардии.Во время ишемии миокарда на ЭКГ фиксируются изменения конечной части желудочкового комплекса — сегмента ST и зубца Т.
Типы смещения сегмента ST, наблюдаемые при хронической ишемической болезни сердца. А – горизонтальное; Б – косое нисходящее; Б – с дугой, обращенной выпуклостью кверху; Г – косое восходящее; Д – корытообразное; Е – подъем сегмента ST.

Для хронической ишемической болезни сердца наиболее специфичны первые два типа смещения сегмента ST, т.е. горизонтальное и косое нисходящее. Изменения сегмента ST, характерные для ишемической болезни сердца, чаще наблюдаются в грудных отведениях V4 –V6, а также в отведениях II, III, aVF, I и aVL.
Пробы с физической нагрузкой.
Во время пробы с ФН пациент выполняет возрастающую нагрузку на тредмиле или велоэргометре, при этом постоянно регистрируются ЧСС и ЭКГ, через регулярные промежутки времени (1-3 мин) контролируется АД.
Основные показания к проведению нагрузочных проб:
· дифференциальная диагностика ИБС и отдельных ее форм;
· определение индивидуальной толерантности к ФН у больных с установленным диагнозом ИБС и уточнение ФК стенокардии;
· оценка эффективности лечебных, в т.ч. хирургических и реабилитационных мероприятий;
· экспертиза трудоспособности больных ССЗ;
· оценка прогноза;
· оценка эффективности антиангинальных препаратов.
Абсолютными противопоказаниями к проведению теста с ФН являются острая стадия ИМ (в течение 2-7 дней от начала), нестабильная стенокардия, нарушение мозгового кровообращения, острый тромбофлебит, тромбоэмболия легочной артерии, СН III-IV ФК согласно классификации Нью-йоркской ассоциации сердца (NYHA), выраженная легочная недостаточность, лихорадка. Нецелесообразно выполнять диагностический тест при тахиаритмиях, полной блокаде левой ножки пучка Гиса, высоких степенях синоатриальной и атриовенокулярной блокад.
Проба с ФН выполняется до развития приступа стенокардии, появления признаков ишемии миокарда на ЭКГ, достижения целевой ЧСС, развития выраженного утомления, делающего невозможным продление ФН, и отказа пациента от проведения пробы. Тест с ФН следует прекратить при:
· развитии типичного приступа стенокардии;
· появлении угрожающих жизни нарушений сердечного ритма: частая, или политопная, или залповая желудочковая экстрасистолия, пароксизмальная тахикардия или пароксизмальная мерцательная аритмия;
· возникновении выраженной одышки (число дыханий более 30 в минуту) или приступа удушья;
· развитии нарушений проводимости – блокада ножек пучка Гиса, атриовентрикулярная блокада 2 степени и более;
· ишемическом смещении сегмента ST вверх > 1 мм в любом из отведений за исключением V1–2, где подъемом считают 2 мм и более, или вниз от изоэлектрической линии > 1 мм и длящемся 80 мс от точки J, медленное косовосходящее снижение сегмента ST в точке J+80 мс > 2 мм (быстрое косовосходящее снижение ST за ишемическое не принимается);
· подъеме САД > 220 мм рт.ст., ДАД > 110 мм рт.ст., снижении САД на 20 мм рт.ст.;
· появлении неврологической симптоматики – головокружение, нарушение координации движений, сильная головная боль;
· возникновении интенсивной боли в ногах;
· развитии резкого утомления больного, его отказе от дальнейшего выполнения пробы;
· как мере предосторожности по решению врача;
· достижении 75% максимальной возрастной ЧСС.
При соблюдении вышеприведенных критериев чувствительность пробы с ФН для обнаружения пациентов с анатомически значимым поражением коронарных артерий, т.е. сужением > 50%, составляет 65-80%, а специфичность – 65-75%. У пациентов с положительными результатами теста чаще бывает тяжелое поражение нескольких коронарных артерий. Проба с ФН считается положительной в плане диагностики ИБС, если при ней воспроизводятся типичные для пациента боль или стеснение в груди и возникают характерные для ишемии изменения на ЭКГ. Не всегда боль сопровождает снижение сегмента ST, проба считается положительной, если снижение появится без боли, либо если типичный приступ стенокардии развивается без снижения сегмента ST.
Учитывая большую важность тестовой информации, необходимо во всех случаях (при отсутствии противопоказаний) стремиться к выполнению нагрузочных проб у больных СС.
ЭКГ-диагностика ИМ.
Достоверные электрокардиографические критерии инфаркта миокарда:
-появление новых зубцов Q шириной более 30 мс и глубиной более 2 мм не менее чем в двух отведениях из следующих: а) отведениях II, III или aVF; б) отведениях V1 - V6; в) в отведениях I и aVL.
-Вновь появившийся подъем или депрессия сегмента ST более 1 мм через 20мс после точки J* в двух смежных отведениях.
-Полная блокада левой ножки пучка Гиса при наличии соответствующей клинической картины.
ЭКГ - важнейший метод диагностики ИМ, позволяющий:
1) выявить ИМ
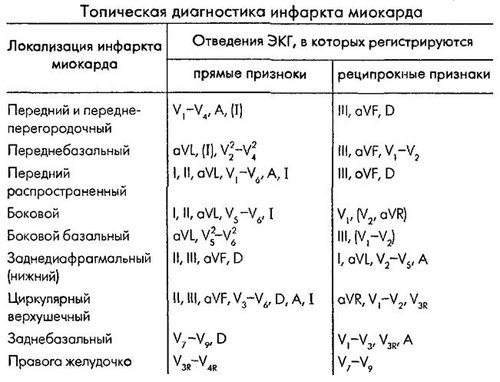
2) установить локализацию ИМ, его глубину и распространенность
3) диагностировать осложнения ИМ (аритмии, формирование аневризмы сердца и др.п)
Согласно Bayley, ЭКГ при ИМ формируется под влиянием трех зон, образующихся в области инфаркта:1. зона некроза.2.зона выраженной дистрофии, которая в ЭКГ называется зоной повреждения.3. зона ишемии.
Ишемия развивается прежде всего в субэндокардиальных отделах миокарда, которые снабжаются кровью хуже, чем субэпикардиальные, т.к.сосуды эндокарда испытывают большее давление со стороны крови, содержащейся в желудочках, поэтому ишемия раньше развивается в субэндокардиальных слоях.
ЭКГ-проявлением субэндокардиальной ишемии будет высокий, заостренный з.Т в грудных отведениях или отведениях от конечностей – это острейшая стадия ИМ.
Ишемия обычно не может продолжаться долго (мах.30 мин.-1 час): или обмен веществ в миокарде восстанавливается или очаг ишемии начинает распространяться и доходит до субэпикарда, что проявляется отрицательным з.Т на ЭКГ.
Следующая стадия- это субэндокардиальное повреждение, в основе его гистологические изменения клеток миокарда, проявляется депрессией ST. Все эти изменения миокарда м.б.обратимы. При субэпикардиальном или трансмуральном повреждении на ЭКГ регистрируем подъем ST.
При инфаркте миокарда происходит гибель миокардиоцитов, внутриклеточные ионы калия выходят из погибшей клетки, накапливаются под эпикардом, образуя в зоне некроза "электрические токи повреждения», вектор которых направлен кнаружи. Эти токи повреждения существенно изменяют процессы реполяризации (S-T и T) в зоне некроза, что отображается на ЭКГ ленте. Регистрирующие электроды, расположенные как над областью инфаркта, так и противоположной, записывают эти токи повреждения, но каждый по-своему.
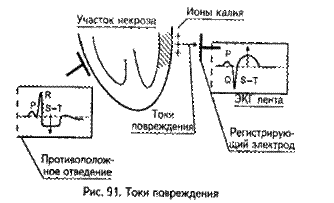
При продолжающемся нарушении коронарного кровообращения мышечные волокна погибают и развивается некроз мышечных волокон. .Поврежденная зона не возбуждается , т.к. не продуцирует электричества, вследствие этого з.R < или исчезает, вместо него образуется широкий и глубокий з.Q или Q-S. Чем больше по глубине некроз, тем шире патологический з.Q. Патологическим зубцом Q мы называем такой зубец Q, ширина которого превышает 0,03 с. Генез нормального зубца Q – это возбуждение межжелудочковой перегородки, а время ее возбуждения не превышает 0,03".

Таким образом, имеем 3 основных ЭКГ-признака ИМ: патологический з.Q, смещение S-T кверху от изолинии и отрицательный з.Т. На противоложных стенках –реципрокные изменения- (дискордантное смещение сегмента S-T ниже изолинии в отведениях, противоположных области инфаркта).
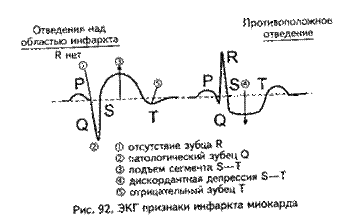
ИМ без зубца Q, чаще мелкоочаговый:
1.Интрамуральный (зона некроза в толще сердечной мышцы,) - в острой стадии короткое время (несколько часов, реже-суток) S-T смещен вверх от изолинии, во второй половине 1 суток появляется отр. Т, который нередко является единственным признаком ИМ на первой ЭКГ Комплекс QRS не изменен- нет з.Q и снижения з.R. В дальнейшее происходит обычная для ИМ динамика з.Т. Отрицательный з.Т регистрируется на эКГ более 2 недель (4-6) , нередко остается (-) и в рубцовой стадии.
2. Субэндокардиальный ИМ, как правило, это распространенный процесс, субэндокардиальный некроз может пронизывать половину миокарда. Основное изменение ЭКГ- депрессия сегмента ST на 2 и более мм в 2 и более отведениях, в конце 1-2 суток присоединяется (-) Т. В течение 1-2 недель сегмент ST приближается к изолинии, сохраняется глубокий отр. з.Т. QRS не изменен, нет патологического з.Q.
ЭКГ при некоторых заболеваниях сердца (миокардиты, пороки сердца, легочное сердце, дисметаболические процессы в миокарде).
Миокардиты вызывают следующие изменения ЭКГ (одно или несколько):
- различные нарушения проводимости, включая удлинение электрической систолы желудочков (QT), атриовентрикулярные блокады I или II степени, нарушения внутрижелудочковой проводимости и блокады ножек пучка Гиса;
- разнообразные нарушения ритма сердца, такие, как синусовая тахикардия, эктопические ритмы, мерцательная аритмия, экстрасистолия и др.;
- изменения ЭКГ, наблюдаемые при остром фибринозном или экссудативном перикардите.
При миокардитах любой этиологии могут выявляться изменения конечной части желудочкового комплекса смещение книзу интервала ST и появление сниженного, сглаженного или отрицательного зубца Т. Эти изменения определяются в грудных или (и) в стандартных отведениях.
Возможно снижение вольтажа зубцов комплекса QRS, зазубренность его. Иногда наблюдаются блокады ножек пучка Гиса и ветвей левой ножки, а также различные их сочетания. При ревматическом миокардите чаще раньше всего появляются различные нарушения атриовентрикулярной проводимости.
При эмболии легочной артерииобычно появляются следующие электрокардиографические признаки остро возникшей перегрузки правых отделов сердца:
1. Наблюдается отклонение электрической оси сердца вправо или тенденция к такому расположению электрической оси сердца. Например, до острой ситуации электрическая ось сердца была расположена горизонтально. При развитии эмболии легочной артерии электрическая ось может стать нормальной или вертикальной.
2. Появляется «Ppulmonale», указывающий на развитие перегрузки правого предсердия с высокими остроконечными зубцами РII, III, aVF.
3. Увеличивается амплитуда зубцов R во II, III и aVF отведениях.
4. Определяется электрическая ось сердца типа SI–SII–SIII.
Выявляются признаки гипертрофии или перегрузки правого желудочка в грудных отведениях:
- увеличение амплитуды или появление высокого зубца R в правых грудных отведениях V1, V2, V3R. ЭКГ в отведениях V1, V2, V3. R может иметь вид R, Rs, qR, а иногда даже QR. В редких случаях в этих отведениях регистрируется комплекс QS. Это заставляет иногда проводить дифференциальный диагноз с инфарктом миокарда переднесептальной области;
- регистрация выраженного зубца SV5, V6;
- развитие признаков полной или неполной блокады правой ножки пучка Гиса с регистрацией ЭКГ типа rsR в V1, V2 и с появлением уширенного зубца SV5, V6;
- снижение амплитуды зубца Rv5, v6 c уменьшением соотношения R/S в отведениях V4–V6;
- увеличение времени активации правого желудочка в отведениях V1, V2;
- подъем или снижение сегмента ST в V1- V2. Подъем сегмента STV1, V2 отмечается чаще при массивной эмболии сосудов малого круга, выпуклость сегмента ST обращена кверху. Депрессия сегмента ST обычно наблюдается при умеренном повышении давления в системе легочной артерии;
- снижение сегмента ST в V4-V6;
- появление отрицательного зубца Т в отведениях V1–V3. Иногда при эмболии легочной артерии отмечается отрицательный зубец Т не только в отведениях V1–V3, а с V1 по. V6, что обусловлено ухудшением питания левого желудочка;
- регистрация позднего зубца R в отведении aVR;
- увеличение амплитуды зубца Р в отведениях V1 – V5;
- смещение переходной зоны влево;
- развитие синусовой тахикардии, а иногда и других нарушений ритма: мерцания и трепетания предсердий, пароксизмальной тахикардии, эктопического ритма из атриовентрикулярного соединения, нарушений атриовентрикулярной проводимости и др.
Указанные изменения ЭКГ встречаются всего в 15 – 40% случаев и чаще наблюдаются при закупорке просвета легочной артерии наполовину или более.
Электрокардиография может помочь в диагностике приобретенных пороков сердца [Маколкин В. И., 1978]. Электрокардиографический диагноз пороков сердца основывается на определении положения электрической оси сердца, выявлении признаков гипертрофии и перегрузки различных отделов сердца. Сведения о характере и топике нарушений ритма, получаемые при электрокардиографическом исследовании, также могут быть использованы при решении вопроса о поражении клапанного аппарата сердца.
Следует учитывать, что вертикальное расположение электрической оси сердца или отклонение ее вправо в сочетании с электрокардиографическими признаками гипертрофии правого желудочка наиболее часто имеют место при митральных пороках с преобладанием стеноза левого венозного отверстия или при митральнотрикуспидальных пороках, реже – при комбинированных митральноаортальных пороках.
Горизонтальное расположение электрической оси сердца или отклонение ее влево в сочетании с электрокардиографическими признаками гипертрофии левого желудочка характерны для аортальных пороков, митральной недостаточности, а также для сочетанных митральных пороков с преобладанием недостаточности митрального клапана. Такая электрокардиографическая картина может отмечаться и при комбинированных митральноаортальных пороках сердца. При митральных пороках частой электрокардиографической находкой является гипертрофия левого предсердия.
Электрокардиографические признаки гипертрофии обоих желудочков при пороках сердца обычно обусловлены сочетанным митральным пороком или комбинированным поражением митрального и аортального клапанов.
Мерцательная аритмия наиболее специфична для митрального стеноза. Крупноволнистая форма мерцания отличает его от мерцательной аритмии другой этиологии.
Для недостаточности клапанов аорты очень характерна электрокардиографическая картина диастолической перегрузки левого желудочка с глубоким qV5,V6. При стенозе устья аорты часто отмечаются электрокардиографические признаки систолической перегрузки левого желудочка с малым qV5, V6. Блокада левой ножки пучка Гиса чаще указывает на стеноз устья аорты, реже – на недостаточность клапанов аорты и не встречается при изолированном митральном пороке сердца.
Дисметаболические нарушения миокарда
Во время климакса или в предклимактерическом периоде, а также при различных гормональных нарушениях у женщин нередко наблюдаются такие же изменения ЭКГ, как при хронической ишемической болезни сердца [Воробьев А. И. и др., 1980]. Эти изменения касаются конечной части желудочкового комплекса – сегмента ST и зубца Т.
Значительно чаще при этом наблюдается патология со стороны зубца Т: высокий положительный, сниженный, сглаженный, двухфазный или отрицательный зубец Т в одном или чаще в нескольких отведениях. Изменения зубца Т наблюдаются в основном в грудных отведениях, больше в правых.
Они могут возникать остро – в пред или менструальный период. Появление их не связано с болевым синдромом в области сердца. Патологические изменения ЭКГ не сопровождаются динамикой биохимических и общих показателей крови и повышением температуры тела, характерных для острого нарушения коронарного кровообращения с развитием очаговых изменений в миокарде.
Патологические изменения ЭКГ могут возникать также на фоне выраженного климакса и характеризоваться стабильностью, не изменяясь в динамике. Для климактерической или дисгормональной кардиопатии специфично улучшение ЭКГ при проведении функциональной пробы с калием и обзиданом.
Суточное мониторирование ЭКГ и АД
Суточное (холтеровское) мониторирование ЭКГ- это метод, с помощью которого осуществляется суточное наблюдение за работой сердца.
Для этого используется носимый портативный регистратор, который производит круглосуточную запись электрокардиограммы и передачу информации о работе сердца за сутки в компьютер.
Обобщив двадцатипятилетний опыт исследований в области регистрации электрических явлений и возможности передачи по радио электроэнцефалограмм, Norman J. Holterсоздал и представил в 1961 году новый метод регистрации ЭКГ.
В течение следующих лет мы стали свидетелями усовершенствования этого метода исследования, который, в отличие от стандартного метода ЭКГ, называется суточным, амбулаторным или холтеровским.
За эти годы 40-килограммовый радиопередающий регистратор, который закреплялся на спине больного, был заменен на регистратор с магнитной лентой, весивший вначале около 2 кг, а сейчас менее 0,5 кг.
Техническое усовершенствование привело к улучшению качества записи, свело до минимума артефакты, связанные с физической активностью пациента. Появилась возможность регистрации 12 отведений, автоматического анализа.
Усовершенствование аппаратуры позволило увеличить число регистрируемых и анализируемых параметров. В настоящее время, наряду с анализом нарушений ритма сердца, появилась возможность количественного определения смещения сегмента ST, оценки функции электрокардиостимулятора (ЭКС) и циклической изменяемости ритма сердца, определяемой автоматически в виде различных временных и спектральных параметров, регистрация усредненных сигналов ЭКГ при большом усилении и автоматическое измерение продолжительности интервала QT.
Как правило, в современных аппартах ХМ используется регистрация ЭКГ в 1-12 модифицированных грудных отведениях, имитирующих (но не идентичных!) грудным отведениям V1 (CM1) – V5 (CM5).
Всем больным при ХМ рекомендуется вести дневник активности с записью возникающей в процессе исследования симптоматики
n Физические и эмоциональные нагрузки
n Прием лекарств
n Прием пищи
n Поездка на транспорте/за рулем
n Отдых
n Сон
n Неприятные ощущения (сердцебиения, «перебои» в работе сердца, боли в грудной клетке и т.д.)
n
n Показания к проведению суточного мониторирования ЭКГ
n Анализ наличия и характера нарушений сердечного ритма и проводимости
n Оценка эффективности антиаритмической терапии
n Выявление ишемических эпизодов
n Оценка работы кардиостимулятора
n Оценка вариабельности сердечного ритма
Суточное мониторирование артериального давления (СМАД).
Однократное определение АД даёт информацию лишь на отдельно взятый момент времени и не всегда отражает реальную клиническую картину. С 70-х годов 20 века широко применяется суточное мониторирование артериального давления (СМАД), предоставляющее дополнительную информацию об уровне АД вне врачебного кабинета (в максимально естественных условиях). В исследовании PAMELA [2010] частота гипертонии белого халата составила 9–12% в общей популяции, а среди пациентов с АГ I степени – 36%, если в качестве ее критерия использовали уровень среднего дневного АД<135/85 мм рт. ст. Автоматические носимые приборы для СМАД воспроизводят алгоритм аускультативного или осциллометрического методов измерения. Большинство приборов измеряют АД по осциллометрическому методу. Однако аускультативный метод предпочтителен при проведении мониторирования у пациентов с повышенной двигательной активностью.
Показатели суточного профиля АД согласно данным СМАД
1. Нормальная степень ночного снижения АД «дипперы» - снижение ночного АД 10-20%
2. Недостаточная степень снижения АД «нондипперы» - снижение ночного АД 0-10%
3. Повышенная степень ночного снижения АД «овердипперы» - более 20%
4. Устойчивое повышение ночного АД «найтпикеры» - давление не снижается.
Методика проведения СМАД
- Установка прибора;
-Обязательное проведение контрольных измерений;
-Устный инструктаж пациента;
-Ввод в компьютер полученных данных с последующей их обработкой
с помощью статистических и графических методов;
-Анализ результатов.
Эхокардиография и допплерография.
Эхокардиогра́фия— метод ультразвуковой диагностики, направленный на исследование морфологических и функциональных изменений сердца и его клапанного аппарата. Основан на улавливании отражённых от структур сердца ультразвуковых сигналов.
Датчик, содержащий пьезоэлектрический керамический кристалл, способный трансформировать электрическую энергию в механическую (звук) и обратно, выступает одновременно и в качестве источника звука, и приемника отраженных волн. Существует три типа эхокардиографических исследований: М-эхокардиография, двухмерная эхокардиография и допплеровское исследование. При М-эхокардиографии один датчик излучает звук с частотой 100Ф—2000 импульсов в 1 с вдоль одной какой-либо оси. Этот тип эхокардиографии позволяет получить качественное изображение во времени. Изменяя направление луча, можно сканировать сердце от желудочков до аорты и левого предсердия. При двухмерной эхокардиографии, направляя ультразвуковой луч по дуге в 90°с частотой около 30 раз в 1 с, получают изображение в двух плоскостях. Используя различные точки расположения датчика, можно получить качественное пространственное изображение, позволяющее анализировать движения структур сердца в реальном времени.
С помощью допплеровской эхокардиографии можно определять скорость кровотока и его турбулентность. Когда звук сталкивается с движущимися эритроцитами, частота отраженного сигнала изменяется. Величина этого изменения (допплеровский сдвиг) указывает на скорость кровотока (V), которую можно рассчитать, учитывая следующие характеристики звукового луча:
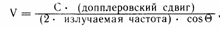
где С — скорость звука в тканях, Q — угол между допплеровским лучом и средней осью кровотока.
Направление сдвига вверх (увеличение частоты отраженного звука) указывает на то, что ток крови направлен к датчику; направление сдвига вниз — от датчика. При прохождении крови через стенозированные отверстия клапанов ее скорость увеличивается, что также может быть зарегистрировано с помощью допплеровской эхокардиографии. Используя затем модифицированное уравнение Бернулли, можно рассчитать чресклапанный градиент давлений (P):P=4V2. Регистрация сигналов в отдельных небольших областях позволяет определить пространственную локализацию турбулентности, характерную для стеноза, недостаточности клапанов или шунтирования крови. Сочетание допплеровского исследования с методами получения изображения позволяет рассчитать сердечный выброс. К сожалению, не у всех больных эхокардиография может быть выполнена успешно. Проникновение звука в ткани может затрудняться у многих лиц пожилого возраста, страдающих ожирением и эмфиземой.
Нормальные величины размеров отдельных структур на М-эхокардиограмме
| Измеряемый параметр | Размер, см | |
| пределы колебаний | среднее значение | |
| Полость правого желудочка в конце диастолы | 0,9—2,6 | 1,7 |
| Полость левого предсердия (в период систолы желудочков) | 1,9—4 | 2,9 |
| Полость левого желудочка в конце диастолы | 3,5—5,7 | 4,7 |
| Толщина задней стенки желудочка в конце диастолы | 0,6—1,1 | 0,9 |
| Амплитуда систолического движения задней стенки левого желудочка | 0,9—1,4 | 1,2 |
| Толщина межжелудочковой перегородки в конце диастолы | 0,6—1,1 | 0,9 |
| Амплитуда систолического движения межжелудочковой перегородки на уровне средней трети | 0,3—0,8 | 0,5 |
| на уровне верхушки сердца | 0,5—1,2 | 0,7 |
| Диаметр устья аорты | 2,0—3,7 | 2,7 |
| Сепарация створок аортального клапана | 1,5—2,5 | 1,9 |
Оценка сократительной функции миокарда левого желудочка с помощью эхокардиографии основывается, главным образом, на измерении ударного объема сердца по разнице между конечным диастолическим и конечным систолическим объемами желудочка (они вычисляются по специальным формулам из результатов измерения полости желудочка), определении фракции выброса (отношение ударного объема к конечному диастолическому объему желудочка) и скорости циркулярного укорочения волокон миокарда. Последний показатель наиболее близко характеризует собственно сократимость миокарда. Интерпретировать показатели центральной гемодинамики, получаемые по данным эхокардиографии , следует с большой осторожностью у больных со следующими заболеваниями: острый инфаркт миокарда, постинфарктный кардиосклероз, врожденные пороки сердца, сопровождающиеся шунтами справа налево и слева направо, приобретенные пороки сердца, особенно митральные и аортальные.
Важную характеристику сократительной функции миокарда дает исследование движений межжелудочковой перегородки и стенок желудочков; повышение функции проявляется гиперкинезией, а снижение — асинергией сокращения и гипокинезией стенок различной распространенности, в т.ч. на отдельных участках изучаемого миокарда.
Фракция выброса — это отношение УО к КДО. В большинстве случаев ее вычисляют по формуле: ФВ = (КДО - КСО)/КДО х 100 (%), где ФВ — фракция выброса, КДО — конечный диастолический объем, КСО — конечный систолический объем. Нормальное значение ФВ ЛЖ — 55-75% .

Двухмерная эхокардиограмма из верхушечного доступа: Видны полости всех четырех камер сердца в поперечном сечении.
Рентгенографическое исследование сердца.
Сердце чаще всего исследуют в прямой (фронтальной) проекции, в первом (правом) и втором (левом) косых положениях и в боковых проекциях. Прямая проекция дает возможность определить контур сердца. Слева он состоит из 4 дуг: самой верхней является дуга аорты, затем — легочной артерии, ушка левого предсердия и левого желудочка. Справа контур сердца образован дугой аорты и правого предсердия.
Исследование сердца во фронтальной проекции позволяет определять его три положения: косое расположение, при котором угол наклона сердца равен 43—48°, поперечное (лежачее сердце) с углом наклона 49—56° и срединное (вертикальное) с углом наклона в 35—42°.
В первом косом положении, т. е. при положении больного правым плечом вперед, хорошо проецируется ретрокардиальное пространство, т. е. пространство между тенью сердца и сосудов с одной стороны, и позвоночным столбом — с другой. В этом положении при заболеваниях может выявляться расширение восходящего отдела аорты и увеличение левого предсердия.
В левом косом положении (левым плечом вперед) видны все отделы аорты и так называемое аортальное окно. Здесь хорошо видны изменения дуги и нисходящего отдела аорты, а также увеличения правого и левого желудочка сердца. Форма сердца значительно изменяется при различных его заболеваниях и поражениях крупных сосудов. Особенно большие изменения наблюдаются при пороках сердца.
Нормальная картина сердца и больших сосудов в рентгеновском изображении
Контуры сосудисто-сердечной тени в переднем положении обрисовываются в виде своеобразной фигуры, верхне-правый контур которой в области тени сосудистого пучка соответствует верхней полой вене, прилегающей к восходящей аорте; нижняя же правая дуга соответствует контуру правого предсердия; далее кнутри расположен правый желудочек, который при данной проекции лучей не участвует в рисунке контура сердца; изредка обнаруживается в виде небольшой тени в углу между правым контуром сердечной тени и диафрагмой нижняя полая вена. Слева образуются три изгиба контура: верхний соответствует дуге аорты и ее нисходящей части, следующий - главным образом легочной артерии и отчасти левому предсердию (ушку) и нижний - левому желудочку. Некоторые авторы выделяют четыре изгиба или дуги слева, соответствующие аорте, легочной артерии, ушку левого предсердия и левому желудочку.
Тень сердца дает очень отчетливое изображение, но нижний ее контур только в редких случаях удается дифференцировать от густой тени печени. При глубоком вдохе нижняя граница видна на несколько большем протяжении благодаря опусканию диафрагмы, а с нею и печени.
Сердечная тень изображается в виде неправильно-эллиптической фигуры, напоминающей больше всего куриное яйцо, (поставленное так, что его узкий конец обращен влево и вниз и продольный диаметр с горизонтальной линией составляет угол, приблизительно равный 35-45°. При высоком стоянии диафрагмы, что часто наблюдается у гиперстеников, указанный угол уменьшается до 25-30°, и сердце принимает более поперечное положение, т. е. его продольный диаметр приближается к горизонтальной линии. Наоборот, у астеников диафрагма стоит относительно низко, и верхушка сердца занимает соответственно более низкое положение, отчего угол наклонения сердца достигает 60° и более. У выраженных астеников сердце, будучи по своим размерам относительно малым («малое сердце»), как бы висит на сосудах («висячее сердце», «капельное сердце») и отличается значительной подвижностью при переменах положения тела («подвижное сердце»).
Инструментальное исследование сосудов
1. Ультразвуковое исследование артерий
Ультразвуковые технологии, являясь высокоинформативными и общедоступными, представляют врачу широкий спектр информации о ранних доклинических проявлениях атеросклероза артерий. Ультразвуковая допплерография \УЗДГ\ – позволяет определить наличие пульсации, сегментарное АД, объемный минутный кровоток, скорость кровотока, оценивает состояние сосудистой стенки, зоны коллатерального и магистрального кровообращения на сегментах конечности.
Дуплексное ультразвуковое сканирование с допплерографией – существенно дополняет УЗДГ графическим изображением зон окклюзии или стеноза с оценкой характеристик изменения проходимости сосудистого русла, измерением протяженности окклюзирующего субстрата с оценкой его плотности, оценкой диаметров и состояния сосудистой стенки. При наличии свищей - позволяет оценить его размеры и объемы перетоков.. УЗИ сосудов позволяет определить зоны окклюзии и стеноза магистральных артерий.
В клинической и научной практике наиболее востребованы методы определения толщины комплекса интима-медиа сонных артерии (ТИМ), выявления атеросклеротических бляшек (АСБ) в сонных артериях и определения лодыжечного индекса давления (ЛИД).
