Учение о растворах. Основные типы химических равновесий и процессов в жизнедеятельности
1. А) Свойства растворов, зависящие от концентрации кинетически самостоятельных единиц и независящие от их природы, называют коллигативными.
К таким коллигативным свойствам относятся:
· Скорость диффузии
· Осмотическое давление
· Давление насыщенного пара растворителя над раствором
· Температура кипения растворов
· Температура замерзания растворов
Б) Коллигативные свойства растворов электролитов зависят от степени ионизации веществ и взаимодействия ионов и молекул в растворе, а в растворах неэлектролитов этим можно пренебречь.
2. А) Самопроизвольный процесс переноса вещества, в результате которого устанавливается равновесие и распределение концентраций вследствие беспорядочного теплового движения молекул, атомов, ионов в газах, жидкостях или твердых телах, называется диффузией.
Диффузия играет важнейшую роль в поглощении питания и насыщении кислородом крови, в поступлении воды и минеральных веществ из почвы в корни, стебли и листья растений.
Б) Всякая живая клетка окружена мембраной, которая служит для защиты и регуляции внутриклеточной среды. Вещества проходят через мембраны по двум основным механизмам: путем обычной диффузии, не связанной с затратой химической энергии -пассивный транспорт и за счет энергетически активированного переноса на основе гидролиза АТФ или переноса электронов по дыхательной цепи митохондрий, что подразумевает активный транспорт.
В) Закон Фика: скорость диффузии вещества пропорциональна поверхности мембраны, через которую переносится вещество, и градиенту концентрации вещества. Для описания диффузии веществ через клеточные мембраны пользуются не математическим выражением закона Фика: An/At = -DS• (Ас/Ах), а более простым уравнением (т. к. концентрационный градиент (Ас/Ах) клеточной мембраны определить трудно):
Am/At = -PS(CrC2), [1] где С и С2 - концентрации по разные стороны мембраны; Р - коэффициент проницаемости, зависящий от свойств мембраны.
Г) В пассивном транспорте различают: а) простую диффузию; б) перенос через поры, каналы; в) транспорт с помощью переносчиков - на основе диффузии переносчика вместе с веществом в мембране, т. е. эстафетной передаче (временная цепочка поперек мембраны).
3. А) Изоосмия -, относительное постоянство осмотического давления в жидких средах и тканях организма, обусловленное поддержанием на данном уровне концентраций содержащихся в них веществ.
Эндоосмос – движение растворителя в осмотическую ячейку (клетку) из окружающей среды.
При этом концентрация в-ва в окр.среде должна быть меньше конц.в-ва в клетке, осмотическое давление в окр.среде так же меньше, чем в клетке.

Экзоосмос – движение растворителя из осмотической ячейки в окружающую среду.
Конц.в-ва и осмотическое давление в окр.среде (межклет.жидкости) должны быть больше, чем в клетке.

4) Гемо́лиз — разрушение эритроцитов крови с выделением в окружающую среду гемоглобина. Гемолиз наступает при попадании эритроцита в среду, где его внутриклеточное содержимое будет гипертоничным по отношению к контактирующему раствору.
Плазмолиз – сжатие и сморщивание оболочки клетки в результате экзоосмоса.

5) А) Изотонические растворы – р-ры, с одинаковым осмотичским давлением.
Гипертонический раствор — раствор, осмотическое давление которого выше нормального.
Гипотонический раствор - раствор, осмотическое давление которого ниже нормального.
Осмотический шок - нарушения в клетке, возникающие при переносе ее в гипертонический или гипотонический раствор
Растворы лекарственных препаратов, вводимые подкожно или внутривенно во избежание осмотического конфликта, должны быть изотоничны биосредам. Все растворы, использующиеся в качестве плазмозамещающих при острых кровопотерях, шоке различного происхождения, нарушениях микроциркуляции, интоксикациях и других процессах, связанных с изменением гемодинамики, должны быть изотоничны крови.
Б) В медицинской практике для очищения ран от гноя применяют гипертонические растворы (3-5-10%) NaCl) в виде марлевых повязок. Ток жидкости в таких марлевых повязках направлен в сторону большего осмотического давления - наружу марли. Для усиления мочевыделения при острых отравлениях, аллергических реакциях, глаукоме, при острой почечной недостаточности, при различных отеках используют осмотические диуретики: натрия ацетат, ман-нит, мочевину.
С изменением осмотического давления связано действие солевых слабительных средств (карловарской соли, натрия сульфата, магния сульфата).
6) А) Осмос – самопроизвольная диффузия молекул растворителя сквозь мембрану с избирательной проницаемостью из раствора с меньшей концентрацией в раствор с большей концентрацией.
Осмос является одной из причин, обусловливающих поступление воды и растворенных в ней веществ из почвы по стеблю или стволу растения к листьям. Осмос обеспечивает распределение воды и веществ в клетках живых организмов.
Б) Закон Вант-Гоффа гласит: "Осмотическое давление разбавленного раствора равно давлению, которое проявляло бы растворенное вещество, если бы оно было газообразным и занимало объем, равный объему раствора". Уравнение для описания осмотического давления для растворов неэлектролитов можно записать так:
p = (m/MV)-RT = C-RT, [2]
где р - осмотическое давление, кПа;
С - молярная концентрация, моль/л;
R - универсальная газовая постоянная, равная 8,31 (кПа-л)/(моль-К); Т - абсолютная температура, К.
Концентрация кинетически самостоятельных частиц в растворах электролитов всегда больше, чем это следует из аналитической концентрации. С тем, чтобы свойства растворов электролитов удовлетворительно описывались уравнениями, выражающими следствие из закона Рауля, Вант-Гоффом был введен поправочный эмпирический коэффициент, называемый сейчас изотоническим или коэффициентом Вант-Гоффа (i):
p=iCRT
7) Концентрация кинетически самостоятельных частиц в растворах электролитов всегда больше, чем это следует из аналитической концентрации. С тем, чтобы свойства растворов электролитов удовлетворительно описывались уравнениями, выражающими следствие из закона Рауля, Вант-Гоффом был введен поправочный эмпирический коэффициент, называемый сейчас изотоническим или коэффициентом Вант-Гоффа (i)
Изотонический коэффициент (также фактор Вант-Гоффа; обозначается i) — безразмерный параметр, характеризующий поведение вещества в растворе. Он численно равен отношению значения некоторого коллигативного свойства раствора данного вещества и значения того же коллигативного свойства неэлектролита той же концентрации при неизменных прочих параметрах системы:

где solut. — данный раствор, nel. solut. — раствор неэлектролита той же концентрации, Tbp — температура кипения, а Tmp — температура плавления (замерзания).
Коэффициент Вант-Гоффа учитывает ионизацию веществ и взаимодействие ионов и молекул в растворе. Значение i для раствора данного электролита увеличивается по мере разбавления, стремясь в пределе к целому значению, равному числу ионов, возникающих при диссоциации структурной единицы электролита.
8) В растворах, содержащих смесь электролитов, расчет числа кинетически самостоятельных частиц затруднен. В связи с этим в прикладных областях химии, в частности в медицине, в последнее время широко применяются понятия осмолярность и осмоляльность.
Под осмолярностью (осмоляльностью) понимают активную концентрацию частиц, не проникающих через идеальную полупроницаемую мембрану. Единицы измерения в системе СИ: осмолярности - моль/л, осмоляльности - моль/кг. Для разбавленных растворов численные значения осмоляльности и осмолярности совпадают. Последнее время чаще применяется такая единица измерения, как осмоль.
Учет этих величин особенно важен в тех случаях, когда применение лекарственных средств сопряжено с протеканием процессов, связанных с осмотическим давлением. Так, при введении лекарственных растворов в кровь, необходимо, чтобы осмолярная концентрация раствора для инъекции совпадала с осмолярной концентрацией плазмы крови (~0,3 осмоль/л). Это значит, что растворы изотоничны. Часто под изоосмией понимают способность организма поддерживать постоянство осмолярности биологических жидкостей.
9) А) Явление преимущественно одностороннего проникновения растворителя (диффузию) через полупроницаемую мембрану из растворителя в раствор или из раствора с меньшей концентрацией в раствор с большей концентрацией называется осмосом.
Осмотическое давление -давление на раствор, отделенный от чистого растворителя мембраной, проницаемой только для молекул растворителя (полупроницаемая мембрана), при котором прекращается осмос. Для электролитов рассчитывается по формуле:
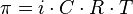
где i — изотонический коэффициент раствора; C — молярная концентрация раствора, выраженная через комбинацию основных единиц СИ, то есть, в моль/м3, а не в привычных моль/л; R — универсальная газовая постоянная; T — термодинамическая температура раствора.
Для неэлектролитов:
p = (m/MV)-RT = CRT
Онкотическое давление – это осмотическое давление, создаваемое за счет наличия белков в биожидкостях организма.
10) А) Первый закон Рауля:
При постоянной температуре относительное понижение давления насыщенного пара растворителя над идеальным раствором нелетучего вещества равно молярной доле растворенного вещества:
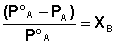
Б) Насы́щенный пар — это пар, находящийся в термодинамическом равновесии с жидкостью или твёрдым телом того же состава.
В) Растворение нелетучего вещества будет затруднять испарение растворителя, вследствие:
· Уменьшения подвижности молекул растворителя за счет взаимодействия его молекул с растворенным веществом
· Уменьшения поверхности испарения, т.к. часть её будет занята молекулами нелетучего вещества
· Уменьшения концентрации молекул растворителя в растворе
11) А) Температура кипения –это температура, при которой давление насыщенного пара над жидкостью становится равным внешнему давлению.
Температура замерзания –это температура, при которой давление насыщенного пара над жидкостью становится равным давлению насыщенного пара над кристаллами этой жидкости.
Б) Второй закон Рауля:
Повышение температуры кипения или понижение температуры замерзания идеальных растворов нелетучих веществ прямо пропорционально моляльной концентрации раствора:
Δtкип = Ккип·Сm, Δtкp = Ккр·Сm.
Здесь Сm -моляльная концентрация раствора (моль/кг); Ккип - эбуллиоскопическая константа или константа кипения растворителя; Ккр - криоскопическая константа или константа кристаллизации растворителя.
В) Растворение нелетучего вещества в растворителе приводит к расширению температурного диапазона существования жилкой фазы: раствор замерзает при более низкой температуре, а кипит при более высокой температуре по сравнению с растворителем, т.к. моляльная концентрация раствора повышается.

12) А) Электролиты – вещества, расплавы и растворы которых содержат подвижные ионы и проводят электрический ток.
Электролитическая диссоциация –процесс распада вещества на ионы вследствие взаимодействия его молекул с полярными молекулами растворителя.
Степень электролитической диссоциации (ионизации) –отношение количества электролита, распавшегося на ионы к общему количеству растворенного электролита.
Б) На степень электролитической диссоциации влияют след.факторы:
· Полярность и поляризуемость хим.связи в соединении. Увеличение полярности хим.связи (напр.CH3COOH и HNO3) и особенно её поляризуемости (HI и HF) увеличивает степень диссоциации.
· Свойства среды. Среда с большим значением диэлектрической проницаемости ослабляет связь между ионами и затрудняет их диссоциацию
· Степень электролитической диссоциации возрастает с уменьшением концентрации раствора, т.к. это способствует диссоциации электролита и затрудняет процесс ассоциации его ионов
· Процесс электролитической диссоциации обычно эндотермический, поэтому степень диссоциации увеличивается с повышением температуры
В) Все электролиты по величине степени диссоциации (а) делятся на сильные и слабые.
Сильные электролиты - α>0,7, являются кислоты, щелочи, большинство солей (H2SO4, HCl, HNO3, KOH, NaOH, Ba(OH)2, NaCl, KNO3)
Слабые электролиты - α<0,1 являются слабые кислоты и слабые основания (CH3COOH, HCN, H2CO3, HF, HNO2, NH2*H2O)
13) А) Константа диссоциации — количественное выражение электролитического равновесия в растворах слабых электролитов.


Б) Kd зависит от:
· Природы вещества
· Природы растворителя (с увеличением диэлектрической проницаемости Kd увеличивается)
· Температуры (при повышении температуры Kd возрастает)
В) 
14) А) В 1923 году Дебай и Хюккель выдвинули теорию, согласно которой
· В растворах сильных электролитов каждый ион окружен со всех сторон ионами противоположенного знака, вследствие чего движение ионов ограничено.
· Ионы сильного электролита в растворе взаимодействуют между собой благодаря наличию значительных электростатических сил, в результате чего ионы одного знака образуют вокруг иона другого знака так называемую ионную атмосферу. Необходимо также учитывать сольватацию ионов.
· Ионная атмосфера и сольватная оболочка замедляют движение ионов в растворе и являются причиной кажущейся неполной ионизации.
· Кроме того, в растворах сильных электролитов при высоких концентрациях может происходить ассоциация ионов.
· Для учета этих влияний состав растворов электролитов следует характеризовать не аналитической концентрацией, а эффективной концентрацией, называемой активностью (Льюис, 1907).
Б) Активность иона (а) –эффективная концентрация иона, соответственно которой он участвует во взаимодействиях, протекающих в растворах сильных электролитов.
Коэффициент активности иона (f) – показывает во сколько раз активность иона отличается от его истинной концентрации в растворе сильного элеткролита.
В) Между активностью и аналитической концентрацией ионов существует связь:
a = f-C, [6]
где f - коэффициент активности, зависящий от концентрации (обычно f < 1); а - активность, моль/л; С - концентрация электролита, моль/л.
В разбавленных растворах сильных электролитов f = 1, тогда а = с.
15) А) Ионная сила раствора (I) –величина, характеризующая интенсивность электростатического поля всех ионов в растворе, которая равна полу-сумме произведений молярной концентрации (с) каждого иона на квадрат его заряда (z):

В биологических системах широко распространены межионные взаимодействия, которые сильно зависят от ионной силы растворов, что прежде всего сказывается на значениях констант диссоциации ионогенных групп биологических субстратов, так как они определяются активностями ионов, а не их концентрациями. Незначительное увеличение ионной силы раствора вызывает изменение степени ионизованности белков или нуклеиновых кислот, вследствие чего меняется их конформация, а следовательно, и биологические функции. Поэтому при использовании растворов электролитов в биологических экспериментах крайне необходимо, чтобы их ионная сила была равна ионной силе соответствующей биологической системы. Так, ионная сила плазмы крови человека равна 0,15 М, поэтому физиологический раствор -простейший заменитель плазмы крови - должен иметь соответствующую концентрацию NaCl (0,15 М, или 0,9 %).
Б) Электролиты являются составной частью жидкостей и тканей живых организмов. Для нормального протекания физиологических и биохимических процессов необходимы катионы натрия, калия, кальция, магния, водорода, анионы хлора, сульфат-ионы, гидрокарбонат-ионы, гидроксид-ионы и др. Концентрации этих ионов в организме человека различны. Так, например, концентрации ионов натрия и хлора весьма значительны и ежедневно пополняются. Концентрации ионов водорода и гидроксид-ионов очень малы, но играют большую роль в жизненных процессах, способствуя нормальному функционированию ферментов, обмену веществ, перевариванию пищи и т.д.
