Ключевая реакция синтеза жирных кислот. Как осуществляется регуляция.
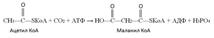
Фермент - ацетил-КоА-карбоксилаза, определяет скорость всех последующих реакций синтеза жирных кислот.
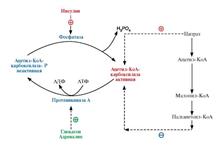
Активность ацетил-КоА-карбоксилазы регулируется несколькоми механизмами: после еды в абсорбтивный период под действием гормона инсулина активируется фермент фосфатаза, который переводит ацетил-КоАкарбоксилазу в дефосфорилированную активную форму. Цитрат активирует ассоциацию дефосфорилированных протомеров, и фермент становится активным;
В абсорбтивный период инсулин стимулирует дефосфорилирование ацетил-КоАкарбоксилазы, цитрат активирует объединение протомеров и фермент становится активным. При голодании (под действием глюкагона) и при физической работе (под действием адреналина) фермент фосфорилируется и становится неактивным
инсулин не только активирует регуляторный фермент ацетил-КоАкарбоксилазу, но и индуцирует его синтез и синтез ряда других ферментов,участвующих в превращении продуктов катаболизма глюкозы в жирные кислоты. Поэтому длительное избыточное потребление углеводов активирует синтез жирных кислот и жиров, что ведет к ожирению;
• при голодании или физической работе гормоны глюкагон или адреналин, активируя аденилатциклазную систему, переводят ацетил-КоАкарбоксилазу в фосфорилированную неактивную форму. ПальмитоилКоА - конечный продукт синтеза - стимулирует диссоциацию протомеров, ускоряя инактивацию фермента.
Таким образом, в результате гормональной регуляции синтез жирных кислот активируется в абсорбтивный период (после еды) и ингибируется при голодании и физической работе, причем это происходит не только за счет изменения активности ферментов, но и путем индукции или репрессии ферментов, участвующих в синтезе жирных кислот из углеводов - индуцируемый фермент) При длительном избыточном потреблении углеводов под действием гормона инсулина происходит индукция синтеза ферментов, участвующих как в образовании субстратов синтеза жирных кислот, так и непосредственно в их синтезе: 1 - глюкозо- 6-фосфат-дегидрогеназа, 2 - малик-фермент, 3 - ацетил-КоА-карбоксилаза, 4 - синтаза жирных кислот, 5 - цитратлиаза
3.Что способствует развитию гиперкетонемии? Как и почему изменяется кетогенез при сахарном диабете и углеводном голодании?
Гиперкетонемия – повышенное содержание кетоновых тел в организме. Кетонемия может наступить в результате усиленного, но недостаточно полного окисления жирных кислот, что в большинстве случаев связано с уменьшением в организме запасов углеводов. Кетоз сопровождает такие заболевания, как сахарный диабет, инсулиновая гипогликемия. К кетозу могут привести также гипоксия, интоксикации, инфекции, вызывающие жировую инфильтрацию печени, избыточное введение глюкокортикоидов при инсулиновой недостаточности.
В норме концентрация кетоновых тел в крови составляет 1-3 мг/дл, но при голодании значительно увеличивается. Увеличение концентрации кетоновых тел в крови называют кетонемией. Накопление кетоновых тел в организме приводит к кетоацидозу: уменьшению щелочного резерва (компенсированному ацидозу), а в тяжёлых случаях - к сдвигу рН (некомпенсированному ацидозу), так как кетоновые тела (кроме ацетона) являются водорастворимыми органическими кислотами (рК~3,5), способными к диссоциации: СН3-СО-СН2-СООН ↔ СН3-СО-СН2-СОО- + Н+. Ацидоз достигает опасных величин при сахарном диабете. Тяжёлая форма ацидоза - одна из основных причин смерти при сахарном диабете. Накопление протонов в крови нарушает связывание кислорода гемоглобином, влияет на ионизацию функциональных групп белков, нарушая их кон-формацию и функцию.
4.Какие ферменты генерируют НАДФ*Н2? Его роль в липидном обмене?
В клетке существует 2 основных источника НАДФ*Н2для синтеза жирных кислот:
а) ГМФ-путь распада углеводов.
б) В реакции окисления малата

Эта реакция протекает в цитоплазме и катализируется ферментом МАЛАТДЕГИДРОГЕНАЗОЙ ДЕКАРБОКСИЛИРУЮЩЕЙ, тривиальное название которого – ЯБЛОЧНЫЙ ФЕРМЕНТ.
НАДФ*Н2 является восстановителем при синтезе жирных кислот.
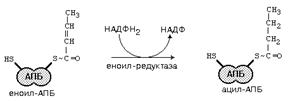
РЕАКЦИИ СИНТЕЗА ЖИРНЫХ КИСЛОТ.
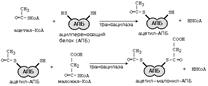


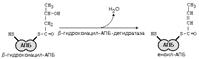
5. Какими реакциями синтезируется мевалоновая кислота? Ключевой фермент в биосинтезе холестерола. Где он локализован? Как осуществляется автономная саморегуляция?
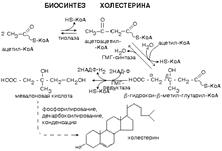
Ключевой фермент - ГМГ-КоА- редуктаза, который обнаруживается в эндоплазматическом ретикулуме всех клеток, обладающих способностью синтезировать холестерин . К ним относятся клетки печени , тонкого кишечника , надпочечников , половых желез .
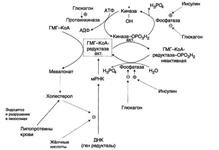
Регуляция происходит разными способами:
1.Фосфорилирование/дефосфорилирование ГМГ-КоА-редуктазы. При увеличении соотношения инеулин/глюкагон этот фермент дефосфорилируется и переходит в активное состояние. Действие инсулина осуществляется через 2 фермента:
А)фосфатазу киназы ГМГ-КоА-редуктазы, которая превращает киназу в неактивное дефосфорилированное состояние;
Б)фосфатазу ГМГ-КоА-редуктазы путём превращения её в дефосфорилированное активное состояние. Результатом этих реакций служит образование дефосфорилированной активной формы ГМГ-КоА-редуктазы.
2. Ингибирование синтеза ГМГ-КоА-редуктазы.
Конечный продукт метаболического пути (холестерол) снижает скорость транскрипции гена ГМГ-КоА-редуктазы, подавляя таким образом собственный синтез. В печени активно идёт синтез жёлчных кислот из холестерола, поэтому и жёлчные кислоты (как конечные продукты синтеза) подавляют активность гена ГМГ-КоА-редуктазы. Так как молекула ГМГ-КоА-редуктазы существует около 3 ч после синтеза, то ингибирование синтеза этого фермента конечным продуктом метаболического пути (холестеролом) является эффективной регуляцией.
Билет 8 = 23
