Электронные и электронно-графические формулы атомов элементов. Правило Хунда
Электронные формулы фиксируют занятые электронами уровни и подуровни и количество электронов на них. В электронных формулах используется обозначение уровней и подуровней, т.е. первым, цифровым символом обозначают уровень (номер), а вторым буквенным символом (s, p, d, f) обозначают подуровни. Число электронов на подуровне обозначают верхним первым индексом.
Например: 1Н 1S , для азота N 7 1S2 2S2 2p3
Электронно-графические формулы изображают атом в виде совокупности орбиталей, которые называют квантовыми ячейками. Например, для азота 1S2 2S2 2p3
 S-подуровень
S-подуровень
 n =1, l=0, m=0
n =1, l=0, m=0
S
S= -1/2 S = +1/2
 |
n =2
P-подуровень, l=1 m=-1,m=0,m=+1
Заполнение орбиталей – ячеек электронами осуществляется в соответствии с принципом Паули, минимизация энергии и правилами Хунда
При данном значении l электроны в атоме располагаются так, что суммарное спиновое число их максимально.
∑S = 1/2+ 1/2+1/2 =3/2
Если заполнили так, т.е. s = +1/2 s = - 1/2, спаренные электроны
∑s= 1/2 + (-1/2) + 1/2 =1/2
Химические свойства атомов определяются в основном строением наружных электронных уровней, которые называются валентными.
Заполненные энергетические подуровни, соответствующие электронным структурам атомов благородных газов, называют электронным остовом. Например: для натрия, имеющего электронную формулу 1S 22S2 2p6 благородного газа неона. Сокращенно электронную формулу благородного газа обозначают его химическим символом в квадратных скобках, например: 1S2 2S2 2p6 = [Ne]
Это позволяет упростить запись электронных формул, например для калия вместо 1S 22S2 2p6 3S2 3p6 4S1 можно написать [Ar] 4S1. Одновременно эта запись наглядно выделяет валентные электроны, определяющие химические свойства атомов элемента.
В электронно-графических (структурных) формулах в отличие от электронных изображают не только заполненные, но и вакантные орбитали валентных подуровней. Это позволяет предсказать изменение валентности элемента в результате перехода его атома в возбужденное состояние, что обозначают символом соответствующего элемента со звездочкой.


 Например: 15P * [Ne] 3S2 3P3 n=3 ↓↑ S ↓↓↓ P
Например: 15P * [Ne] 3S2 3P3 n=3 ↓↑ S ↓↓↓ P
В невозбужденном состоянии атом фосфора имеет три неспаренных электрона на p-подуровне. При переходе атома в возбужденное состояние электронная пара s-подуровня может разделиться, и один из электронов с S- подуровня может переходить на d-подуровень. Валентность фосфора при этом меняется с трех в основном состоянии до пяти в возбужденном состоянии.
Контрольные вопросы
1 Какие элементарные частицы входят в состав атома?
2 Что такое электрон, протон, нейтрон?
3 Объясните, почему у многих элементов при одном и том же заряде ядра атома могут быть разные массовые числа. Почему у ряда элементов, например у хлора, нецелочисленные атомные массы?
4 Дайте характеристику квантовым числам. Почему в атоме не могут быть два электрона с одинаковыми квантовыми числами? Принцип Паули.
5 Объясните физический смысл графических изображений

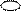
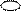
 S и р-орбиталей: S p
S и р-орбиталей: S p
6 Изобразите электронно-структурные формулы атомов углерода, азота и кислорода. Подсчитайте суммы спиновых квантовых чисел электронов в этих атомах. Как изменяются эти суммы при нарушении правила Хунда.
7 Напишите электронную и электронно-структурную формулу атома бора. Какую дополнительную информацию содержит электронно-структурная формула по сравнению с электронной.
8 Правило Клечковского. Какой энергетический уровень и подуровень заполняется вперед 4S или 3d, 5S или 4p, 4f или 6p?
9 Какое основное отличие р-орбиталей от d-орбиталей?
10 Какое число электронов может находиться в энергетических состояниях 2S, 3p, 3d, 5f?
11 Опишите форму орбитали, характеризующейся квантовыми числами: а) n=3, 1=0, m=0 ; б) n=3, 1=1, m=0+1-1; в) n=3, 1=2, m=0+1-1+2-2 Приведите символы орбиталей
12 Охарактеризуйте набором квантовых чисел каждую из следующих орбиталей: 1S, 2p, 3d.
13 Сформулируйте правила, которыми определяется число орбиталей и электронов данного электронного слоя. Например 1=0,1,2 n=1,2,3
14 Какова максимальная емкость электронных слоев К, М, L, N?
15 Зависит ли число орбиталей с данным значением 1 от номера энергетического уровня? Приведите буквенные обозначения орбиталей с указанными значениями 1.
Рекомендуемая литература
Основная
1 Хомченко Г.П., Цитович И.К. Неорганическая химия. М.: Высшая школа, 1998, глава 2, стр 53-75
2 Князев Д.А., Смарыгин С.Н. Неоганическая химия. М.: Высшая школа, 1990, глава 10, стр 102 -112
Дополнительная
3 Глинка Н.Л. Общая химия.(Под ред. А.И.Ермакова, - 28-е изд., перераб. и доп. – М.; Интеграл-Пресс, 2000 – 728с.)
4 Глинка Н.Л. Задачи и упражнения по общей химии. М.;1988.
5 Павлов Н.Н Теоретические основы общей химии. М.,Высшая химия 1978.
