Факторы, влияющие на кислотность и основность органических соединений. Влияние заместителей
Большинство органических соединений можно рассматривать как кислоты, т.к. в их молекулах имеются связи атомов водорода с атомами С, О, N, S. Органические соединения классифицируют по кислотным центрам на С–Н, О–Н, N–H, S–H кислоты.
Кислотный центр – это элемент и связанный с ним атом водорода. На кислотные свойства органических соединений оказывает влияние стабильность аниона, образующегося при отдаче протона Н+. На стабильность аниона оказывают влияние следующие факторы:
Органические кислоты — слабые электролиты, и процесс диссоциации идет до установления обратимого равновесия,которое характеризуется константой диссоциации (К).
Чем меньше рКа, тем больше кислотность по Бренстеду.
Качественной характеристикой кислотных свойств может служить стабильность образующегося аниона. Стабильность аниона, определяется характером распределения отрицательного заряда аниона и зависит
от ряда факторов:
1) природы атома в кислотном центре (электроотрицательности и поляризуемости элемента);
2) характера связанного с кислотным центром органического радикала (электроноакцепторного или электронодонорного);
3) сольватационныхэффектов.
Электроотрицательность имеет значение, когда сравнивается кислотность соединений, имеющих одинаковые радикалы и элементы кислотного центра, относящиеся к одному и тому же периоду периодической системы Д.И. Менделеева (т.е. когда практически не
изменяется поляризуемость)
Поляризуемость атома характеризует меру смещения (рассредоточения) валентных электронов под действием внешнего электрического поля.
Электроноакцепторные заместители способствуют делокализации отрицательного заряда, стабилизируют анион и увеличивают кислотность. Так, введение ОН группы в молекулу пропановой кислоты (рКа =4,9) приводит к увеличению кислотности на порядок:
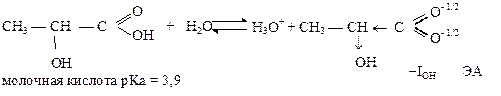
Электронодонорные заместители, наоборот, препятствуют делокализации отрицательного заряда и понижают кислотность.
Растворители оказывают существенное влияние на стабилизацию аниона (эффектсольватации). Как правило, лучше гидратируются небольшие по размеру ионы с низкой степенью делокализации заряда.
Факторы, влияющие на основность
1. Природа гетероатома в основном центре
Н3С - NH2 > Н3С - OH Н3С - OH > Н3С – SH
Сила оснований зависит от электроотрицательности гетероатома в основном центре. Чем больше ЭО атома, тем слабее основные свойства, поэтому спирты и простые эфиры являются более слабыми основаниями по сравнению с аминами.
2. Строение радикала, связанного с основным центром.
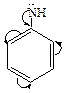 анилин Н3С → СН2 → NH2 этиламин
анилин Н3С → СН2 → NH2 этиламин
Алифатические амины проявляют более выраженные основные свойства, чем ароматические, так как электронная плотность от углеводородного радикала смещается к NH2, а чем больше электронной плотности на основном центре, тем лучше присоединяется Н+. в ароматических аминах NH2 входит в общее сопряжение с бензольным кольцом и отдает электронную плотность на кольцо, поэтому Н+ присоединяется труднее, основные свойства слабее.
3. Влияние заместителей. Электронодонорые заместители усиливают основные свойства, а электроноакцепторные – уменьшают, например:
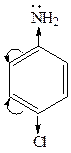 4-хлоранилин
4-хлоранилин 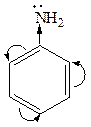 анилин
анилин 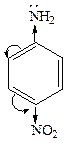 4-нитроанилин
4-нитроанилин
РКВН+ 5,1 4,6 1,0

уменьшение основности
4. Влияние растворителя
В водной среде важную роль играет уменьшение пространственных препятствий для гидратации, поэтому вторичные амины лучше гидратируются, чем третичные, которые пространственно труднодоступны.
 H3C - NH – CH3 > H3C – NH2 > H3C - N – CH3
H3C - NH – CH3 > H3C – NH2 > H3C - N – CH3
CH3
 |
основность уменьшается
В газовой среде основность возрастает с увеличением углеводородных радикалов, так как усиливается их стабилизирующее действие за счет +I-эффекта на катион сопряженной кислоты, поэтому третичные амины проявляют более сильные основные свойства по сравнению с другими аминами.
 H3C - N – CH3 > H3C - NH – CH3 > H3C – NH2
H3C - N – CH3 > H3C - NH – CH3 > H3C – NH2
CH3
 основность уменьшается
основность уменьшается
