Глава 19 патофизиология почек
ГЛАВА 19 ПАТОФИЗИОЛОГИЯ ПОЧЕК
Почки относятся к жизненно важным органам. Основное назначение почек - сохранение постоянства внутренней среды (гомеостаза) организма:
1) поддержание на постоянном уровне объема внеклеточной жидкости и ее осмолярности путем влияния на размер экскреции воды и натрия;
2) регуляция содержания во внеклеточной жидкости калия, магния, кальция, фосфора, хлора и других электролитов;
3) участие в поддержании на нормальном уровне рН крови путем задержки в организме, удаления и продукции кислых и щелочных субстанций;
4) удаление из плазмы крови токсических и конечных продуктов обмена, избытка глюкозы, аминокислот, пептидов и полипептидов, в том числе различных гормонов, а также чужеродных веществ (лекарственные препараты, яды и пр.);
5) участие в регуляции кровяного давления и эритропоэза.
Значительная часть перечисленных функций связана с экскреторной деятельностью почек, суммарным результатом которой является образование мочи.
ПОКАЗАТЕЛИ ЭКСКРЕТОРНОЙ ФУНКЦИИ ПОЧЕК В НОРМЕ
Суточный объем мочи при обычной водной нагрузке равен 0,8-1,5 л. Относительная плотность ее колеблется в зависимости от объема поступившей в организм жидкости в пределах от 1002 до 1035. Реакция мочи кислая, рН колеблется от 5,0 до 7,0. В составе мочи могут присутствовать единичные эритроциты и лейкоциты, клетки плоского эпителия, иногда гиалиновые цилиндры, кристаллы солей.
НЕЭКСКРЕТОРНЫЕ ФУНКЦИИ ПОЧЕК
Почки играют важную роль в регуляции системного кровяного давления, эритропоэза, в катаболизме гормонов и других биологически активных веществ.
Общеизвестно, что в юкстагломерулярном аппарате почек образуется ренин, являющийся пусковым звеном ренин-ангиотензинальдостероновой системы (РААС), которая играет важнейшую роль в регуляции сосудистого тонуса.
В почках образуется гормон эритропоэтин, который регулирует процессы дифференцировки, размножения и созревания клеток, участвующих в эритропоэзе.
В первичную мочу поступают из плазмы крови различные пептиды и полипептиды, в том числе гормоны полипептидной природы, такие, как гастрин, инсулин, глюкагон, вазопрессин, аденокортикотропный гормон (АКТГ), паратгормон, пролактин, а также ангиотензин-II и брадикинин. В щеточной кайме эпителия проксимальных канальцев имеются пептидазы, которые расщепляют поступившие в первичную мочу пептиды и полипептиды до аминокислот. При почечной недостаточности удаление этих веществ почками снижается, а содержание их в плазме крови возрастает, что сопровождается различными эндокринными расстройствами. В проксимальных канальцах синтезируется активная форма витамина D - 1,25 (ОН)2 D3 (кальцитриол), которая необходима для транспорта кальция через стенку кишечника и эпителий канальцев.
НАРУШЕНИЕ ФУНКЦИИ КАНАЛЬЦЕВ
Нарушение процессов реабсорбции, экскреции и секреции в канальцах может сопровождаться расстройствами водноэлектролитного обмена, кислотно-основного равновесия, обмена глюкозы и аминокислот, гормонов.
В основе этих нарушений может лежать изолированное повреждение ферментных систем, что имеет место при наследственных и приобретенных тубулопатиях. Кроме того, причиной нарушения функции канальцев могут быть дистрофические изменения канальцевого эпителия, структурные изменения в окружающем интерстиции и расстройства эндокринной регуляции.
Тубулопатии- это заболевания, обусловленные нарушением транспортных функций эпителия почечных канальцев в связи с отсутствием или качественными изменениями белков-переносчиков, тех или иных ферментов, рецепторов для гормонов или дистрофическими процессами в стенке канальцев.
По этиологии различают первичные(наследственные) и вторичные(приобретенные) тубулопатии.
Вторичные тубулопатии могут развиться под действием лекарственных препаратов (например, тетрациклина с истекшим сроком годности), при отравлении солями лития, висмута, ртути, свинца, кадмия; при обширных ожогах, гиперпаратиреозе, злокачественных опухолях различных органов, миеломе, пиелонефрите, интерстициальном нефрите.
В зависимости от локализации дефекта различают проксимальные и дистальные тубулопатии.
Проксимальные тубулопатии.Обусловлены нарушением функции проксимальных канальцев. К этой группе относятся фосфатурия, почечная глюкозурия, гипераминоацидурия и проксимальный почечный ацидоз.
Фосфатурия.Возникает вследствие нарушения реабсорбции фосфатов; она сопровождается гипофосфатемией, рахитоподобными изменениями в костях (гипофосфатемический витамин D-резистентный рахит). Полагают, что в механизме развития фосфатурии играют роль отсутствие транспортного белка для фосфатов, а также недостаток рецепторов для связывания кальцитриола.
Почечная глюкозурия.Реабсорбция глюкозы в кровь происходит в проксимальном канальце с помощью специального переносчика, который одновременно присоединяет и глюкозу, и Na+-ионы. Экскреция глюкозы с мочой происходит в том случае, если количество профильтровавшейся в клубочках глюкозы превышает реабсорбционную способность канальцев. Почечная глюкозурия характеризуется понижением почечного порога для глюкозы вследствие уменьшения максимальной способности канальцев ее реабсорбировать. Почечная глюкозурия может быть самостоятельным заболеванием наследственной природы или одним из симптомов других тубулопатий, например синдрома де Тони-Дебре-Фанкони.В отличие от сахарного диабета при почечной глюкозурии содержание глюкозы в крови нормально или понижено.
Почечная гипераминоацидурия.Обусловлена отсутствием одного или нескольких транспортных белков-переносчиков, участвующих в реабсорбции аминокислот. Примером ренальной гипераминоацидурии является цистинурия. Она возникает при изолированном выпадении специфической транспортной системы, необходимой для реабсорбции цистина. Заболевание наследуется по аутосомнорецессивному типу. Иногда нарушается реабсорбция не только цистина, но и лизина, аргинина, орнитина. Цистин плохо растворим в кислой моче и может выпадать в осадок, из которого образуются цистиновые камни. Щелочная реакция мочи способствует растворению цистина.
Следует иметь в виду, что наряду с ренальной формой гипераминоацидурии существует экстраренальная, обусловленная резким повышением содержания аминокислот в крови и относительной недостаточностью функции канальцевого эпителия.
Дистальные тубулопатии.К ним относится почечный водный диабет, который чаще является наследственным рецессивным, сцепленным с полом заболеванием. В основе его развития лежит отсутствие реакции почек на АДГ, что ведет к нарушению реабсорбции воды в дистальных канальцах и собирательных трубочках.
В результате развивается полиурия (до 30 л/сутки), сопровождающаяся полидипсией; почки утрачивают способность к концентрированию мочи, относительная плотность ее не превышает 1005, т.е. имеется гипостенурия. При этом содержание АДГ в крови нормально.
Разновидностями дистальных тубулопатий являются также псевдогипоальдостеронизм и дистальный почечный канальцевый ацидоз.
Наряду с повреждением изолированных транспортных систем существуют тубулопатии, характеризующиеся комбинированным дефектом процессов канальцевой реабсорбции. К их числу относится синдром де Тони-Дебре-Фанкони, проявляющийся нарушением реабсорбции глюкозы, различных аминокислот, фосфатов и бикарбонатов.
По этиологии различают наследственную и приобретенную формы этого синдрома. Основные клинические проявления - метаболический ацидоз, глюкозурия, рахитоподобные изменения в костях, остеопороз; при наследственной форме - задержка роста и развития.
Ренальные нарушения
Заболевания почек сопровождаются нарушениями образования и выделения мочи. Они могут выражаться в виде изменения количества мочи, ее относительной плотности и состава (мочевой синдром). Количество выделяемой за сутки мочи может быть повышенным (полиурия), пониженным (олигурия) или крайне низким (анурия).
Полиурия(polys - много, uron - моча) характеризуется увеличением объема суточного диуреза свыше 2000 мл независимо от объема выпитой жидкости. В механизме развития полиурии играют роль увеличение клубочковой фильтрации плазмы крови и (или) уменьшение реабсорбции жидкости в канальцах. Последнее имеет место на полиурической стадии острой и хронической почечной недостаточности, а также при прекращении секреции АДГ. У здорового человека может формироваться временная полиурия в результате повышенной водной нагрузки или поступления в кровь и затем в клубочковый фильтрат большого количества осмотически активных веществ (солей, глюкозы и др.). Полиурия может развиваться у новорожденных из-за неспособности эпителия канальцев осуществлять реабсорбцию воды в нормальном размере.
Олигурия(olygos - малый) характеризуется снижением суточного диуреза до 500-200 мл. Причинами этого могут являться уменьшение объема клубочкового фильтрата, усиление реабсорбции воды в канальцах почек или затруднение оттока мочи. У здорового человека олигурия возникает при ограничении принимаемой жидкости.
Анурия(an - отсутствие) характеризуется прекращением мочеотделения или выделением мочи в количестве менее 200 мл/ сутки. По механизму развития различают анурию преренальную, ренальную и постренальную. Примером преренальной анурииявляется прекращение мочеотделения в результате рефлекторного торможения функции почек при сильных болевых ощущениях. Травма, заболевание одной почки или сдавление одного мочеточника тормозят функцию второй почки и также могут вызвать анурию. В механизме развития рефлекторной анурии играют роль спазм приносящих артериол почечных клубочков и стимуляция секреции АДГ.
Ренальная ануриявозникает на определенной стадии острой почечной недостаточности в связи с резким снижением объема клубочковой фильтрации и закупоркой канальцев.
Постренальная анурияимеет место при наличии препятствия для оттока мочи на каком-либо уровне мочевого тракта, а также при параличе мочевого пузыря.
Наряду с объемом суточной мочи могут изменяться частота мочеиспускания и распределение выделения мочи в течение суток. При ряде заболеваний почек и некоторых нарушениях в мочевыводящих путях наблюдается превалирование ночного диуреза над дневным - никтурия(от nictos - ночь), тогда как у здорового человека объем дневного диуреза составляет 65-80% от общего объема суточной мочи.
Частота мочеиспускания может увеличиваться (поллакиурия,от греч. pollakis - часто) или снижаться (оллакизурия,от греч. ollakis - редко).
Относительная плотность мочи является показателем концентрационной способности почек. У здорового человека, как уже отмечалось, она колеблется от 1002 до 1035 в зависимости от количества поступившей в организм жидкости. В условиях патологии относительная плотность мочи может изменяться независимо от поступления в организм жидкости, она может увеличиваться (гиперстенурия), уменьшаться (гипостенурия) или соответствовать относительной плотности клубочкового фильтрата (изостенурия).
Гиперстенурия(hyper - много, sthenos - сила) характеризуется увеличением относительной плотности мочи более 1030 вследствие усиления процесса реабсорбции воды в дистальном отделе нефрона (при сухоядении, больших внепочечных потерях внеклеточной жидкости).
Гипостенурия(hypo - мало) означает снижение относительной плотности мочи (1002-1012); при пробе с сухоядением относительная плотность мочи не достигает 1026.
Изостенурия(isos - равный) - относительная плотность мочи очень мало колеблется в течение суток и соответствует относительной плотности клубочкового фильтрата (1010).
Гипо- и изостенурия свидетельствуют о нарушении концентрационной способности почек. Это происходит при ренальной форме острой почечной недостаточности, хронической почечной недостаточности, гипофункции надпочечников, отсутствии АДГ, а также при гиперкальциемии и дефиците калия, которые нарушают нормальное действие АДГ на клетки собирательных трубочек и дистальных извитых канальцев.
Изменения состава мочихарактеризуются появлением в ней белка (протеинурия), глюкозы (глюкозурия), аминокислот (аминоацидурия), крови (гематурия), лейкоцитов (лейкоцитурия), цилиндров (цилиндрурия), клеток эпителия почечных канальцев или мочевыводящих путей, кристаллов различных солей или аминокислот (кристаллурия), микроорганизмов (бактериурия).
Протеинурия.В норме проникновению белков плазмы крови в клубочковый фильтрат препятствуют гломерулярный фильтр (эндотелий, базальная мембрана, подоциты) и электростатический заряд этих структур, который отталкивает отрицательно заряженные молекулы, в том числе молекулы альбумина. Заряд клубочкового фильтра обусловлен присутствием в нем сиалогликопротеина и гликозаминогликанов.
У здорового человека в клубочках из плазмы крови фильтруется 0,5 г белка/сутки (преимущественно альбумина). Значительная часть поступившего в клубочковый фильтрат белка реабсорбируется в проксимальных канальцах посредством пиноцитоза. Некоторая часть поступающего в мочу белка образуется в эпителии петли Генле и дистальных канальцев - это уропротеин Тамма- Хорсфалля, являющийся сложным гликопротеином. Общее количество белка, выделяющегося с суточной мочой, в норме составляет около 50 мг и не обнаруживается обычными лабораторными
методами. Выделение с мочой более 150 мг белка/сутки называется протеинурией.
По механизму развития различают клубочковуюи канальцевуюпротеинурию. Первая связана с повышенной проницаемостью клубочкового фильтра, вторая - с нарушением реабсорбции белка в проксимальном канальце вследствие недостаточности функции эпителия или снижения оттока лимфы от ткани почек. В последнем случае белок накапливается в интерстициальной ткани и обусловливает отек почечной паренхимы.
Кроме этого выделяют функциональную и патологическую протеинурию. Функциональная протеинурияможет иметь место у людей со здоровыми почками. Существует несколько разновидностей функциональной протеинурии: ортостатическая, протеинурия напряжения, лихорадочная, застойная и идиопатическая. Ортостатическая протеинурия возникает у некоторых людей (чаще в молодом возрасте) при длительном стоянии или ходьбе; при смене положения тела на горизонтальное она исчезает. Протеинурия напряжения наблюдается примерно у 20% здоровых людей после тяжелой физической нагрузки. Лихорадочная протеинурия возникает чаще у детей и стариков; при нормализации температуры тела она исчезает. Застойная протеинурия наблюдается при застойной недостаточности кровообращения. Идиопатическая протеинурия обнаруживается иногда у здоровых людей при медицинском обследовании, она имеет преходящий характер. Следует также иметь в виду возможность развития протеинурии у здоровых женщин в конце беременности. Общей особенностью всех видов функциональной протеинурии являются ее небольшие размеры - обычно не более 1 г белка/сутки.
Патологическая протеинуриясвязана с различными заболеваниями. Она подразделяется на преренальную, ренальную и постренальную.
Преренальная протеинурия(или перегрузочная) устанавливается при повышенном содержании в плазме крови низкомолекулярных белков, таких, как легкие цепи иммуноглобулинов (белок БенсДжонса), миоглобин, гемоглобин, лизоцим. Эти белки легко проходят через клубочковый фильтр, но не полностью реабсорбируются канальцевым эпителием. Такой вид протеинурии развивается при миеломной болезни, моноцитарном лейкозе, рабдомиолизе, внутрисосудистом гемолизе и др. Размер преренальной протеинурии может достигать 20 г белка/сутки.
Ренальная протеинурияможет быть связана с поражением как клубочков, так и канальцев. Она развивается при гломерулонефритах, интерстициальном нефрите, пиелонефрите, амилоидозе, остром канальцевом некрозе, тубулопатиях и некоторых других заболеваниях. Выделение белка с мочой колеблется в пределах 1-3 г белка/сутки и выше. Если оно превышает 3 г белка/сутки, развивается нефротический синдром.
Постренальная протеинурия(внепочечная) регистрируется при заболеваниях мочевыводящих путей, она обусловлена поступлением в мочу экссудата.
Патологическая ренальная клубочковая протеинурия подразделяется на селективную и неселективную протеинурию. Развитие селективной протеинуриисвязано с утратой клубочковым фильтром способности отталкивать отрицательно заряженные молекулы белка и, таким образом, препятствовать их прохождению в ультрафильтрат. Поскольку диаметр пор фильтра (70 нм) превышает размер молекул альбумина и трансферрина, то эти белки свободно проходят через незаряженный фильтр, и развивается массивная протеинурия. Она наблюдается при нефротическом синдроме с минимальными изменениями, которые выражаются в потере тонких переплетающихся ножек отростков подоцитов.
Неселективная протеинуриявозникает при утрате гломерулярным фильтром способности регулировать прохождение молекул белка в зависимости от их размера. В связи с этим в ультрафильтрат поступают не только альбумины и трансферрин, но и крупнодисперсные белки плазмы, например иммуноглобулины G1, а2-макроглобулин и β-липопротеины.
Гематурия(от греч. haima - кровь) - присутствие крови в моче. Различают микро- и макрогематурию. Микрогематурия не изменяет цвета мочи, ее можно выявить только при микроскопии осадка или с помощью индикаторной полоски. Макрогематурия придает моче цвет мясных помоев. Причины развития гематурии разнообразны: 1) заболевания почек - гломерулонефрит, тубулоинтерстициальный нефрит, поликистоз, поражение почек при системной красной волчанке, пурпуре Шенлейна-Геноха, туберкулезе и др.; 2) повреждения мочевыводящих путей при почечно-каменной болезни, уролитиазе, травмах, развитии опухолей и др. Гематурия иногда обнаруживается при больших физических нагрузках.
Цилиндрурия- присутствие в осадке мочи плотных масс, подобных слепкам почечных канальцев, в которых они формируются.
В зависимости от состава различают цилиндры гиалиновые, зернистые, эпителиальные, жировые, восковидные, гемоглобиновые, эритроцитарные и лейкоцитарные. Матрицей цилиндров являются белки. Гиалиновые цилиндры состоят почти исключительно из белка Тамма-Хорсфалля, иногда они обнаруживаются в моче здоровых людей. В состав других цилиндров также входят белки почечного или плазменного происхождения. Присутствие цилиндров, как правило, свидетельствует о заболевании почек (гломерулонефриты, острый некроз почек, амилоидоз, пиелонефрит и др.).
Лейкоцитурия- присутствие в моче лейкоцитов в количестве более 5 в поле зрения микроскопа. Выявляется при остром и хроническом пиелонефрите и воспалительных процессах в мочевыводящих путях.
К изменениям состава мочи, не связанным с заболеваниями почек, относятся билирубинурия, гемоглобинурия, кетонурия; глюкозурия и аминоацидурия наблюдаются как при заболеваниях почек (тубулопатиях), так и при заболеваниях других органов (сахарный диабет, заболевания печени).
Нефротический синдром
Этим термином обозначается симптомокомплекс, характеризующийся массивной протеинурией(более 3 г белка/сутки), гипо- и диспротеинемией, гиперлипидемией, гиперхолестеринемией, распространенными отеками и водянкой серозных полостей.
По этиологииразличают первичный и вторичный нефротический синдром. Причиной развития первичного нефротического синдромаявляются первично возникающие заболевания почек, такие, как гломерулопатия с минимальными изменениями в виде слияния малых ножек подоцитов (липоидный нефроз), мембранозный гломерулонефрит, фокально-сегментарный гломерулосклероз, мембранозно-пролиферативный гломерулонефрит.
Вторичный нефротический синдромвозникает при многих заболеваниях, в основном системного характера, при которых почки поражаются вторично. К числу таких заболеваний относятся сахарный диабет (диабетическая нефропатия), амилоидоз, злокачественные опухоли, коллагенозы (системная красная волчанка, склеродермия, ревматизм, узелковый периартериит), хронические инфекционные процессы в организме, паразитарные заболевания
(токсоплазмоз, шистоматоз и др.), аллергические заболевания (сывороточная болезнь и др.). Кроме этого вторичный нефротический синдром возникает при интоксикациях (золото, ртуть, висмут, пенициламин, нестероидные противовоспалительные средства, яды насекомых и змей), нефропатии беременных, тромбозе почечных сосудов и др.
Этиология нефротического синдрома в значительной степени зависит от возраста. Наиболее частой причиной развития этого синдрома у детей является нефропатия с минимальными изменениями; у взрослых среди причин развития нефротического синдрома на первом месте стоит мембранозный гломерулонефрит; у людей старше 60 лет, наряду с мембранозным гломерулонефритом, развитие нефротического синдрома во многих случаях связано с диабетической нефропатией и другими системными заболеваниями, вторично нарушающими функцию почек.
Патогенез.Во всех случаях нефротического синдрома имеет место повышенная проницаемость базальной мембраны капилляров клубочков для белка. Протеинурияможет иметь как селективный, так и неселективный характер. При нефротическом синдроме с минимальными изменениями повышение клубочковой проницаемости связано с уменьшением постоянного электрического заряда стенки капиллярных петель, что обусловлено исчезновением из нее сиалопротеида, в норме тонким слоем покрывающего эндотелий и отростки подоцитов, лежащих на базальной мембране. При мембранозном гломерулонефрите главную роль играет потеря функции барьера, зависящего от размера пор в базальной мембране, которые в норме ограничивают прохождение плазменных белков с молекулярной массой более 150 кД.
Повышение проницаемости фильтрующих мембран клубочков связывают с повреждающим действием откладывающихся на них иммунных комплексов, а также лизосомальных ферментов и активных форм кислорода, выделяемых нейтрофилами и моноцитами. Кроме того, в плазме крови больных с нефротическим синдромом обнаружен фактор, предположительно образуемый лимфоцитами, который повышает проницаемость клубочкового барьера. При любом механизме повреждения происходит повышенное поступление белков плазмы крови, преимущественно альбуминов, в клубочковый фильтрат, и развивается резко выраженная протеинурия (более 3 г белка/сутки, в отдельных случаях - до 50 г белка/сутки). Следствием этого является гипопротеинемия(менее 60 г белка/л),
главным образом за счет снижения содержания альбуминов. Вызываемое гипопротеинемией падение коллоидно-осмотического давления сопровождается усиленным выходом жидкости из сосудов в межклеточное пространство и серозные полости тела и развитием гиповолемии, что, в свою очередь, вызывает повышение активности РААС и усиление продукции альдостерона; последний снижает экскрецию натрия с мочой и увеличивает его концентрацию в крови. При проведении ряда клинических и экспериментальных исследований было установлено, что, кроме описанного механизма, развитию гипернатриемии при нефротическом синдроме способствует снижение реакции почек на действие предсердного натрийдиуретического пептида, стимулирующего выведение натрия с мочой. Установлено, что пониженная реакция нефротической почки на предсердный натрийуретический пептид обусловлена пострецепторным дефектом в механизме действия этого фактора на уровне канальцевого эпителия. Возникающее при этом повышение осмотического давления стимулирует секрецию АДГ, который усиливает задержку в организме воды, что ведет к развитию отеков (рис. 19-2).
Стимуляция секреции АДГ под действием гипернатриемии сопровождается увеличением объема плазмы крови, но происходит ее разжижение, гипопротеинемия и гипоонкия возрастают. Вследствие этого избыточная вода не задерживается в кровеносном русле, а перемещается в ткани, что способствует дальнейшему нарастанию отеков, т.е. возникает «порочный круг».
Развитию гипопротеинемии при нефротическом синдроме, кроме протеинурии, способствуют повышенный выход белка в ткани в составе транссудата и потеря его через отечную слизистую кишечника. Гипопротеинемия сочетается с диспротеинемией,так как наряду с альбуминами нередко снижается содержание в крови γ-глобулинов, которые также могут поступать в мочу. Вместе с тем развивается гиперлипидемияза счет повышения содержания липопротеинов низкой и очень низкой плотности (ЛПОНП) при нормальном или пониженном уровне липопротеинов высокой плотности. В плазме крови повышается содержание холестерина и триацилглицеролов. За развитие гиперлипидемии ответственны два механизма: повышение продукции липопротеинов в печени и нарушение катаболизма хиломикронов и ЛПОНП. Предполагается, что пониженный катаболизм липопротеинов может быть обусловлен потерей с мочой некоторых субстанций (например, ли-
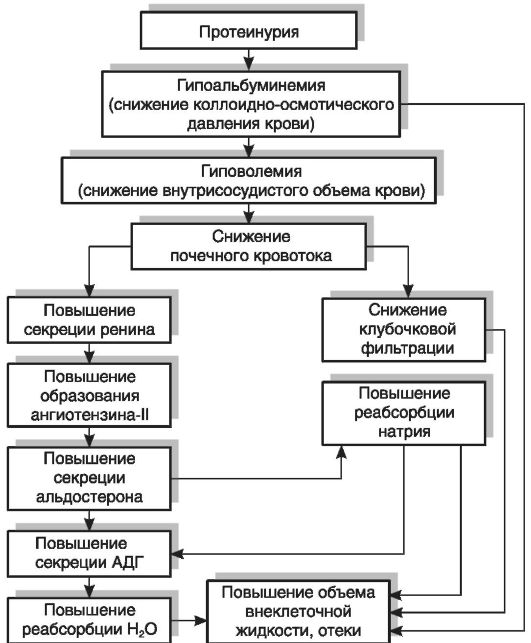 Рис. 19-2.Механизм развития отеков при нефротическом синдроме. АДГ - антидиуретический гормон
Рис. 19-2.Механизм развития отеков при нефротическом синдроме. АДГ - антидиуретический гормон
попротеиновой липазы). Однако ни один из компонентов, выделенных из мочи этих больных, полностью не устраняет нарушения обмена липопротеинов. Гиперхолестеринемия и гиперлипидемия повышают риск развития у таких пациентов сердечно-сосудистых нарушений.
При нефротическом синдроме многие транспортные белки, связывающие эндогенные и экзогенные субстанции, теряются с мочой. В связи с этим в плазме крови у больных с нефротическим синдромом понижен уровень ряда микроэлементов (Fe, Cu
и Zn), метаболитов витамина D, тареоидньгх и стероидных гормонов. Многие лекарства в плазме крови связаны с альбуминами, поэтому при гипоальбуминемии повышается количество свободно циркулирующих форм, что может повысить их токсичность.
Развитие обширных отеков(вплоть до отека легких и мозга) и накопление транссудата в серозных полостях могут сопровождаться тяжелыми нарушениями функции жизненно важных органов и стать причиной летального исхода. Наряду с этим при нефротическом синдроме возникает ряд осложнений, являющихся факторами риска для таких больных.
Главную опасность при нефротическом синдроме составляют тромбоэмболические осложнения.У больных мембранозным гломерулонефритом часто возникает тромбоз почечной вены (у 20-30% взрослых пациентов); нередко происходит тромбоз глубоких вен голени. Другим опасным осложнением является эмболия легочной артерии. Артериальные тромбозы менее часты, но они могут привести к нарушению коронарного кровообращения, что повышает риск развития инфаркта миокарда. Главными факторами, ответственными за состояние гиперкоагуляции при нефротическом синдроме, являются повышение содержания прокоагулянтов - фибриногена и плазменных факторов V и VIII, снижение содержания антикоагулянта антитромбина III, ослабление активности фибринолитической системы вследствие снижения содержания плазминогена и повышение активности а2-антиплазмина; кроме того, происходит увеличение количества тромбоцитов и повышается их способность к адгезии и агрегации, что способствует нарушению микроциркуляции в различных органах и тканях.
Другую опасность для больных с нефротическим синдромом представляют инфекционные осложнения. Ранее дети с этим синдромом умирали от бактериальной инфекции, в частности от пневмококкового перитонита. Повышенная чувствительность к бактериальной инфекции обусловлена снижением уровня иммуноглобулинов А и G вследствие потери их с мочой.
Нередко происходит развитие гипокалыщемии,что обусловлено потерей с мочой связанного с белком кальция и метаболитов витамина D и снижением продукции этого витамина в проксимальных канальцах нефронов. Следствием гипокальциемии является развитие гиперпаратиреоза и остеопороза.Из других осложнений следует указать на возможность развития острой почечной недостаточности в связи с резко выраженной гиповолемией.
Ренальные показатели при нефротическом синдроме в значительной степени зависят от заболевания, на фоне которого он развился. В наиболее чистом виде они выражены при нефропатии с минимальными изменениями. При этом состоянии развивается олигурия,относительная плотность мочи повышена (1030-1050); кроме массивной протеинурии, регистрируется липидурия;в осадке мочи обнаруживаются гиалиновые, восковидные и эпителиальные цилиндры с жировыми включениями. При других вариантах нефротического синдрома в осадке мочи могут присутствовать эритроциты и лейкоциты. Массивная протеинурия повреждает эпителий канальцев, и это может сопровождаться развитием глюкозурии, гипераминоацидурии, фосфатурии, почечного канальцевого ацидоза; возникает состояние, подобное синдрому де Тони- Дебре-Фанкони.
Считается, что прогноз нефротического синдрома благоприятен при нефропатии с минимальными изменениями (при условии своевременно начатого лечения). При нефротическом синдроме другой этиологии исход зависит от вида заболевания, возникших осложнений, возраста пациента, своевременности и правильности лечения.
Острая почечная недостаточность (ОПН) - это быстро возникающее, потенциально обратимое, резкое снижение функции почек, сопровождающееся появлением гиперазотемии и многих других нарушений гомеостаза и функций органов.
Различают три формы ОПН:
1) преренальную, характеризующуюся нарушением почечной гемодинамики без повреждения паренхимы почек;
2) ренальную, связанную с повреждением аппарата почечных канальцев;
3) постренальную, обусловленную остро возникающей окклюзией мочевыводящих путей.
Этиология ОПН
Преренальная ОПНвозникает при значительном снижении перфузии почечных сосудов, обусловленном острой системной гипотонией (шок, коллапс), снижением объема экстрацеллюлярной жидкости (кровопотеря, обезвоживание), уменьшением эффектив-
ного объема кровотока при обширных отеках и водянках (цирроз печени, сердечная недостаточность).
К этиологическим факторам реналыной формы ОПНотносятся такие воздействия, которые обусловливают не только снижение клубочковой фильтрации, но и резко выраженное нарушение функции канальцев вследствие развития в них дистрофических изменений вплоть до острого некроза. По этиологии различают два типа острого канальцевого некроза (ОКН) - ишемический и нефротоксический. Причинами первого из них может быть резкое снижение системного артериального давления, особенно в сочетании с ДВС-синдромом и сладжем, при тех же состояниях, которые играют роль в развитии преренальной ОПН, но более резко выраженных и длительно действующих; нередко такое состояние может развиться после обширных хирургических операций, особенно осложненных сепсисом.
Нефротоксический ОКН развивается при прямом повреждающем действии на эпителий канальцев промышленных ядов (соли ртути, меди, платины, висмута, хрома, серебра, урана, мышьяка), радиоконтрастных средств, лекарственных препаратов (аминогликозидные антибиотики, нестероидные противовоспалительные средства, цисплатин, сульфаниламиды! и др.), грибных и змеиных ядов, бактериальных токсинов (при сепсисе, анаэробной инфекции). Кроме того, к факторам, вызывающим ренальную ОПН, относят блокаду почечных канальцев миоглобином при рабдомиолизе (краш-синдром, чрезмерные физические нагрузки, приступы судорог и др.), гемоглобином (при резко выраженном гемолизе), легкими цепями иммуноглобулинов (при миеломе), уратами (при чрезмерно выраженном распаде нуклеопротеидов в связи с противоопухолевой терапией). Примерно в 15-25% случаев ренальная ОПН обусловлена воспалительными процессами в почечной паренхиме, такими, как острый гломерулонефрит и пиелонефрит, интерстициальный нефрит, васкулит и др.
Причинами развития постренальной ОПНмогут являться нарушение проходимости обоих мочеточников (закупорка камнями, кровяными сгустками и др.), рак мочевого пузыря, простаты и др.
Патогенез ОПН
Основными патогенетическими факторами при развитии ОПН являются резкое снижение клубочковой фильтрации и повреждение канальцевого эпителия в связи с ишемией или действием
нефротоксинов, что сопровождается нарушением процессов реабсорбции, секреции и экскреции (рис. 19-3). Снижение фильтрации может быть обусловлено спазмом почечных артериол в связи с падением системного артериального давления (централизация кровообращения); нарушением их проходимости из-за сладжа эритроцитов или образования микротромбов (ДВС-синдром), замедлением кровотока и снижением фильтрационного давления при обезвоживании. Констрикция почечных артериол может быть результатом внутрипочечной перестройки кровотока, проис-
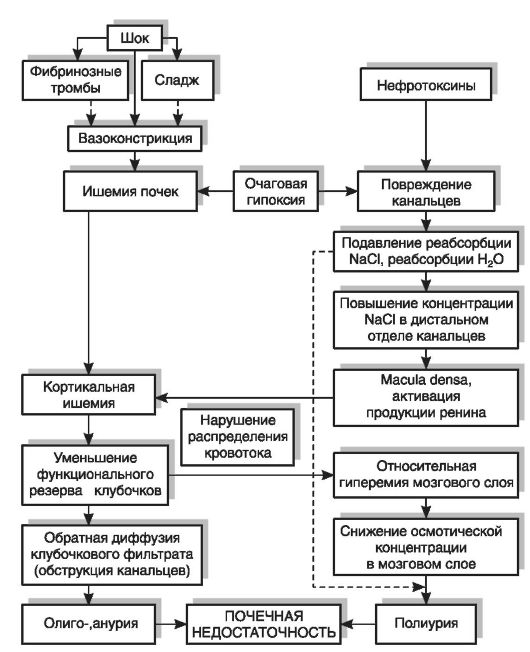 Рис. 19-3.Патогенез острой почечной недостаточности (по P.W. Wustenberg)
Рис. 19-3.Патогенез острой почечной недостаточности (по P.W. Wustenberg)
ходящей независимо от состояния системного кровообращения: вследствие пониженной реабсорбции натрия из-за повреждения эпителия канальцев повышается концентрация его в канальцевой жидкости. Это стимулирует через рецепторы, заложенные в macula densa, продукцию ренина и ангиотензина-II, который вызывает констрикцию афферентных артериол почечных клубочков, что сопровождается шунтированием крови на уровне кортикомедуллярной зоны. В патогенезе расстройств почечного кровообращения важную роль играет нарушение равновесия между NO, расширяющим сосуды, и эндотелином, вызывающим их спазм.
Различные нефротоксины в большинстве случаев оказывают прямое повреждающее действие на эпителий канальцев, вызывая нарушение ферментативно-обменных реакций, окислительных процессов, структуры и функции клеточных мембран. В повреждении и гибели канальцевого эпителия играет роль нарушение внутриклеточного гомеостаза кальция (содержание его в цитоплазме возрастает). Это сопровождается повреждением митохондрий, усилением перекисного окисления липидов (ПОЛ) и активацией фосфолипаз, в том числе фосфолипазы А2. Под действием последней высвобождается арахидоновая кислота. При ее расщеплении образуются тромбоксаны и лейкотриены, являющиеся хематтрактантами для нейтрофилов, повреждающих клетки своими лизосомальными ферментами и активными радикалами кислорода.
В патогенезе ОПН при остром гломерулонефрите играют роль нарушения кровообращения в клубочках и интерстициальной ткани, заполнение капсулы Боумена экссудатом и пролиферирующими клетками, отек интерстиция, повышение внутрипочечного давления, нарушение проходимости канальцев в результате обтурации кровяными сгустками. В механизме развития постренальной ОПН главную роль играет повышение внутрипочечного давления в связи с наличием препятствия для оттока мочи (см. раздел 19.1).
УРЕМИЯ
Уремия(мочекровие, от греч. uron - моча и haima - кровь) - клинический синдром прогрессирующей почечной недостаточност
