Факторы, влияющие на уровень доказательства.
Оглавление
1. Введение 4
2. Методология 4
3. Определение, терминология 6
4. Цели и показания к седации в ОРИТ 6
5. Основные принципы седации в ОРИТ 7
6. Седативные препараты 9
7. Алгоритмы седации 15
8. Седация при лечении постгипоксической энцефалопатии 16
9. Ключевые рекомендации 17
10. Список литературы 19
Приложение 1 21
Приложение 2 22
Список сокращений
ААС – алкогольный абстинентный синдром
ВЧГ – внутричерепная гипертензия
ВЧД – внутричерепное давление
ГАМК – гамма-аминомасляная кислота
ИВЛ – искусственная вентиляция легких
НИ – наблюдательные исследования
ОРИТ – отделение реанимации и интенсивной терапии
РКИ – рандомизированные контролируемые исследования
ЦНС – центральная нервная система
ЭЭГ - электроэнцефалография
- Введение.
Практически все пациенты в ОРИТ нуждаются в проведении адекватной седации в силу различных причин, среди которых необходимость выполнения инвазивных процедур, нарушение циркадных ритмов сна и бодрствования, тяжесть общего состояния, необходимость респираторной поддержки [1].Адекватная седация препятствует развитию стрессовой реакции, беспокойства, обеспечивает комфорт и повышает переносимость интубации трахеи и искусственной вентиляции легких, а также облегчает уход за больным [2].
Недостаточная седация приводит к посттравматическим стрессовым расстройствам, наблюдаемым у 15-27% пациентов палат реанимации [3, 4], существенно ухудшающим качество их жизни.
Ажитация (возбуждение) способствует асинхронии с аппаратом ИВЛ, повышенному потреблению кислорода, повышению продукции углекислоты и лактата, что ведет к угрожающему жизни респираторному и метаболическому ацидозу[5].
Избыточная седация, с другой стороны, может привести к неоправданно пролонгированной ИВЛ и связанным с ней осложнениям, в том числе пневмонии. Длительная ИВЛ, в свою очередь, обусловливает увеличение времени пребывания в ОРИТ, ухудшение прогноза, повышение риска летального исхода и возрастание затрат на лечение пациентов.
В настоящих клинических рекомендациях изложены вопросы седации в ОРИТ для взрослых пациентов. Диагностика и лечение делирия в данных рекомендациях не рассматриваются. Кроме того, данные клинические рекомендации не распространяются на пациентов с судорожным синдромом и внутричерепной гипертензией, так как седация в этих случаях имеет существенные особенности.
Область применения:
Настоящие рекомендации распространяются на осуществление медицинской помощи пациентам в процессе интенсивной терапии в условиях ОРИТ за исключением пациентов с органическими повреждениями головного мозга.
Цель разработки и внедрения:
Улучшение качества оказания медицинской помощи в условиях отделений анестезиологии-реанимации.
Задачи разработки и внедрения:
- Оптимизация и унификация технологии седации пациентов, находящихся в отделениях анестезиологии-реанимации.
-Обеспечение доступности оказания медицинской помощи населению в рамках Программы государственных гарантий оказания гражданам.
- Методология
Нами использована методология, предложенная в клинических рекомендациях по лечению боли, возбуждения и делирия Американской коллегией критической медицины [6]. Рекомендации классифицируются по своей силе и качеству доказательной базы. Уровень доказательства каждого утверждения и рекомендации оценивался как высокий (А), умеренный (В) или низкий/очень низкий (С). Различают « сильные» рекомендации (обозначены цифрой 1) и «слабые» (обозначены цифрой 2). Знаком «+» или «-» отмечено, направлена ли данная рекомендация за или против данного воздействия. Если это «сильная» рекомендация, то +1 или -1 означают, что большинство экспертов считают, что преимущества данного вмешательства значительно превышают риски или наоборот, риски значительно превышают преимущества. В этом случае у большинства пациентов они будут выполнены. В случае «слабых» рекомендаций +2 или -2 означают, что преимущества данного воздействия вероятно превышают риски, но эксперты не имеют согласованного мнения в связи с низким качеством доказательной базы или отсутствием баланса между преимуществами и рисками. В этой ситуации большинству пациентов будет назначено альтернативное лечение.
Таблица 1.
Определение, терминология.
Седация – комплекс медикаментозных и немедикаментозных средств, предназначенный обеспечить физический и психический комфорт пациента и облегчить технику ухода в ОРИТ [7].
Существует ряд более конкретных определений седации. Среди них: «контролируемый уровень медикаментозной депрессии сознания, при котором сохранены защитные рефлексы, обеспечивается адекватно дыхание, и есть ответы на физические стимулы или вербальные команды» [8].
По классификации Американской ассоциации анестезиологов (ASA) седация различается по уровню (глубине) [9]:
- минимальная седация (анксиолизис) – пациент находится в состоянии бодрствования, контактирует с врачом, но познавательная функция и координация могут быть нарушены;
- умеренная седация– депрессия сознания, при которой пациенты реагируют на словесный или легкий тактильный стимул, способны к сотрудничеству, не требуется поддержки проходимости дыхательных путей, адекватное спонтанное дыхание и функция сердечно-сосудистой системы сохранены;
- глубокая седация – пациенты не могут быть легко пробуждены, но реагируют на повторный или болезненный стимул, может потребоваться поддержка проходимости дыхательных путей, спонтанное дыхание может быть нарушено, функция сердечно-сосудистой системы сохранена.
По продолжительности различают:
- быструю (дискретную) седацию;
- кратковременную (менее 24 ч);
- средней длительности (24 – 72 ч);
- длительную (более 72 ч).
4. Цели и показания к седации.
Седация проводится у пациентов в ОРИТ с целью:
- улучшить комфорт и безопасность пациента и его окружения;
- обеспечить реализацию диагностических и лечебных действий в оптимальных комфортных и безопасных для больного условиях;
- улучшить состояние больного и устранить последствия, связанные с определенной патологией [10].
Показания к седации:
- устранение возбуждения и его отрицательных последствий;
- устранения и предупреждения делирия;
- синдром отмены алкоголя, наркотиков и сильнодействующих препаратов
- защита головного мозга (тяжелое повреждение, постгипоксическая энцефалопатия).
Большое значение имеет своевременная идентификация и правильное лечение основных причин возбуждения, таких, как боль, делирий, гипоксемия, гипогликемия, гипотензия, алкогольный или другой абстинентный синдром.
Перед применением седативных средств необходимо предпринять попытки снижения беспокойства и возбуждения с помощью обеспечения комфорта пациента, адекватного обезболивания, регулярной перемены положения и оптимизации окружающей обстановки для поддержания нормального сна [11].
Перед проведением седации необходимо определить:
а) тип седации (анксиолизис, т.е. купирование тревоги, или собственно седация)
б) глубину седации:
в) продолжительность седации:
Боль, страх и возбуждение могут иметь неблагоприятные психологические эффекты и вредные последствия. Боль ухудшает респираторную и циркуляторную функции, повышает частоту легочных осложнений и эндокринно-метаболических реакций. Страх может привести к отказу от ухода, прекращению сотрудничества с персоналом ОРИТ, росту агрессивности. Анальгезия и седация приводят к уменьшению эндокринно-метаболической реакции на стресс, повышают соотношение доставка/потребление кислорода, снижают частоту послеоперационных осложнений и смертность.
Многочисленные процедуры, выполняемые в ОРИТ у больных в сознании, являются болезненными и могут вызывать тревогу и страх. В связи с этим пациентам при выполнении инвазивных процедур может быть назначена выборочная, ограниченная по времени седация, интенсивность которой должна соответствовать процедуре. При этом необходимо оценивать потребности больного, учитывать побочное действие и контролировать эффективность седативной терапии.
При некоторых заболеваниях и состояниях может потребоваться глубокая седация:
- при внутричерепной гипертензии независимо от этиологии (с целью оптимизации перфузии и церебральной оксигенации, для борьбы с судорожным синдромом, нейровегетативными нарушениями, для предупреждения эпизодов гипертензии);
- при некоторых дыхательных расстройствах для профилактики баротравмы, обеспечения максимального соотношения вентиляция/перфузия и создания оптимальной оксигенации (например, при остром респираторном дистресс-синдроме, астматическом статусе).
- при постгипоксической энцефалопатии в течение первых 7 – 8 суток
В некоторых случаях необходимо дополнить седацию миорелаксацией. Показания к миорелаксациив настоящее время весьма ограничены и включают:
- острый респираторный дистресс синдром;
- астматический статус;
- злокачественную гипертермию, устойчивую к методам охлаждения.
Во всех перечисленных случаях состояние пациентов и показания к глубокой седации и миорелаксации должны подвергаться периодической переоценке.
Седативные препараты
Седативные препараты – это медикаментозные средства, которые успокаивают пациента, уменьшают возбуждение и обеспечивают сон. [12].
Отрицательные побочные эффекты седативных препаратов в ОРИТ:
- развитие толерантности к препаратам
-избыточный седативный эффект
-нарушение перистальтики желудочно-кишечного тракта
- появление симптомов отмены
- когнитивный дефицит.
Таблица 4
Клиническая фармакология седативных средств[6].
| Препарат | Время наступления действия | Время полувыведения | Активные метаболиты | Нагрузочная доза в/в | Поддерживающая доза , в/в | Побочные явления |
| Дексмедетомидин | 5-10 мин. | 1,8-3,1 ч | Нет | 1 мкг/кг в течение 10 мин. Не назначают при нестабильной гемодинамике | 0,2-0,7 мкг/кг в час, при нормальной переносимости можно повысить до 1,5 мкг/кг/час | Брадикардия, гипотензия; гипертензия при нагрузочной дозе; потеря рефлексов дыхательных путей |
| Пропофол | 1-2 мин. | Кратковременное применение 3-12 ч, длительное применение 50±18,6 ч | Нет | 5 мкг/кг/мин в течение 5 минут Вводят только пациентам, у которых маловероятная гипертензия | 5-50 мкг/кг/мин. | Угнетение дыхания, Боль при инъекциив периферические вены, гипотензия, гипертриглицеридемия, панкреатит, аллергические реакции, инфузионный синдром, связанный с пропофолом; после глубокой седации пропофолом пробуждение гораздо более длительное, чем после легкой седации |
| Ингаляционные анестетики | Несколько минут | 4 – 7 ч | Гипотензия, дозозависимое угнетение дыхания, брадикардия, тахикардия | |||
| Изофлуран | трифторацетат | 3 мл/ч | 2 – 7 мл/ч | |||
| Севофлуран | гексафторизопропанол | – 5 мл/ч | 4 – 10 мл/ч | |||
| Мидазолам | 2-5 мин. | 3-11 ч | Есть Продлевают седацию, особенно у больных с почечной недостаточностью | 0,01-0,05 мг/кг в течение нескольких минут | 0,02-0,1 мг/кг в час | Угнетение дыхания, гипотензия |
Дексмедетомидин
Является селективным агонистом α2 адренорецепторов, но не обладает селективностью к А, В и С подтипам α2 адренорецепторов. Препарат обладает седативным, обезболивающим и симпатолитическим эффектами, но без противосудорожного действия, позволяет снизить потребность в опиоидах. Седация при назначении дексмедетомидина имеет определенные особенности. Пациенты, получающие инфузию дексмедетомидина, легко просыпаются и способны к взаимодействию с персоналом, а признаки угнетения дыхания выражены минимально.
α2-агонисты вызывают активацию α2А-адренорецепторов в голубом пятне (locus coereleus) и стволе мозга. Это, в свою очередь, приводит к ингибированию выброса норадреналина и гиперполяризации возбудимых нейронов, что вызывает седативный эффект [13]. Поэтому седация, вызванная применением дексмедетомидина, близка к естественному сну[14].
Дексмедетомидин легко проникает через гематоэнцефалический барьер и обладает анальгетическим эффектом, особенно в сочетании с низкими дозами опиоидов или местных анестетиков [14 - 17].
Таким образом, симпатолитический эффект дексмедетомидина связан с уменьшением высвобождения норадреналина из симпатических нервных окончаний [18], а седативный эффект опосредован снижением возбуждения в голубом пятне, основном центре норадренергической иннервации ЦНС [19].
Дексмедетомидин потенцирует анальгетический эффект опиатов[20].
У взрослых на ИВЛ с факторами риска развития делирия использование для седации дексмедетомидина снижает выраженность делирия в сравнении с бензодиазепинамиии пропофолом. В сравнении с пропофолом, дексмедетомидин уменьшает частоту когнитивных расстройств в 1,6 раза [13]. Кроме того, дексмедетомидин сокращает время пребывания на ИВЛ и продолжительность пребывания в ОРИТ пациентов с делирием по сравнению с пациентами, для лечения которых применялся галоперидол [21].
Внутривенное введение дексмедетомидина обеспечивает эффективную седацию у пациентов на ИВЛ в ОРИТ и седацию во время кратковременных инвазивных вмешательств [14]. Обычно инфузия дексмедетомидина переносится хорошо и приводит к уменьшению потребности во внутривенном введении пропофола и мидазолама и снижает необходимость назначения опиатов.
Дексмедетомидин не вызывает депрессии дыхания. Препарат может применяться для седации самостоятельно дышащих неинтубированных пациентов и пациентов, которым проводят неинвазивную масочную вентиляцию легких. После прекращения введения дексмедетомидин не оказывает каких-либо остаточных влияний на систему дыхания. При использовании дексмедетомидина могут возникать гипотензия и брадикардия, но они проходят обычно самостоятельно, без дополнительного лечения. При седации дексмедетомидином возникает также побочный эффект в виде расслабления мышц ротоглотки [9].
Согласно российской инструкции,дексмедетомидин («Дексдор») показан для седации у взрослых пациентов, находящихся в отделении интенсивной терапии, необходимая глубина которой не превышает пробуждение в ответ на голосовую стимуляцию (соответствует диапазону от 0 до -3 баллов по шкале ажитации - седации Ричмонда (RASS).
Препарат противопоказан при:
- гиперчувствительности к компонентам препарата;
- атриовентрикулярной блокаде II – III степени (при отсутствии искусственного водителя ритма);
- неконтролируемой артериальной гипотензии;
- острой цереброваскулярной патологии;
- у детей до 18 лет.
Пациенты на ИВЛ могут быть переведены на инфузию дексмедетомидина с начальной скоростью 0,7 мкг/кг/ч с последующей постепенной коррекцией дозы в пределах 0,2 – 1,4 мкг/кг/ч с целью достижения необходимой глубины седации. Седация наступает в течение 5-10 минут, пик наблюдается через 1 час после начала в/в инфузии дексмедетомидина, длительность действия препарата после окончания инфузии составляет 30 минут. После коррекции скорости введения препарата необходимая глубина седации может не достигаться в течение одного часа. При этом не рекомендуется превышать максимальную дозу 1,4 мкг/кг/ч.
Для ослабленных пациентов начальная скорость инфузии дексмедетомидина может быть снижена до минимальных значений. У пожилых пациентов не требуется коррекции дозы.
Если нужно ускорить начало действия препарата, например, при выраженном возбуждении, рекомендовано проводить нагрузочную инфузию в дозе 0,5–1,0 мкг/кг массы тела в течение 20 мин, то есть начальную инфузию 1,5–3 мкг/кг/ч в течение 20 мин. После нагрузочной инфузии скорость введения препарата снижается до 0,4 мкг/кг/ч, в дальнейшем скорость инфузии можно корригировать.
Пациенты, у которых адекватный седативный эффект не достигнут на максимальной дозе препарата, должны быть переведены на альтернативное седативное средство. Введение насыщающей дозы препарата не рекомендуется, так как при этом повышается частота побочных реакций. До наступления клинического эффекта дексмедетомидина допускается введение пропофола или мидазолама. Опыт применения дексмедетомидина в течение более 14 дней отсутствует, при применении препарата более 14 дней необходимо регулярно оценивать состояние пациента.
Дексмедетомидин имеет ряд преимуществ по сравнению с другими седативными средствами, так как обладает одновременно седативным и анальгетическим действием, практически не влияет на внешнее дыхание и не вызывает кумулятивного эффекта. Успешное применение дексмедетомидина в условиях ОРИТ в России [22, 23] позволяет рекомендовать препарат в качестве одного из основных седативных средств как для пациентов на пролонгированной ИВЛ, так и на самостоятельном дыхании.
К агонистам α2 -адренорецепторов относится также клонидин который обладает влиянием на α1-адренорецепторы, оказывает анальгетическое и седативное действие. Существует ряд исследований, описывающих успешное применение клонидина в ОРИТ, в том числе при длительной седации и при отлучении от вентилятора [24 - 26]. Однако в российской инструкции к препарату клонидин седация к применению отсутствует в показаниях, в связи с чем клонидин не был включен в данные клинические рекомендации.
Пропофол.
Коротко действующий гипнотик. Механизм действия достаточно сложен и обусловлен воздействием на различные рецепторы ЦНС, в том числе рецепторы ГАМК, глицина, никотиновой кислоты и М1-мускариновые рецепторы. Препарат обладает седативным, снотворным, амнестическим, противорвотным и противосудорожным действием, но лишен обезболивающего эффекта [27]. Пропофол хорошо растворяется в липидах и проникает через гематоэнцефалический барьер, благодаря чему седативный эффект наступает быстро. При этом печеночный и внепеченочный клиренс пропофола высок, что обусловливает быстрое прекращение действия препарата. В связи с этим применение пропофола может быть рекомендовано для пациентов, которым требуется частое пробуждение для неврологической оценки или при дневном прерывании седации [28]. При длительном применении пропофола может произойти насыщение периферических тканей, что приведет к более длительному действию и более медленному выходу из седации [29]. Так же, как и бензодиазепины, пропофол вызывает угнетение дыхания и гипотензию, особенно у пациентов с уже имеющейся дыхательной недостаточностью или гемодинамической нестабильностью. Эти эффекты потенцируются одновременным назначением других седативных средств или опиоидов.
Доза введения пропофола в ОРИТ составляет 0,3 – 4,0 мг/кг/ч и не должна превышать 4 мг/кг/ч. Для пожилых пациентов скорость инфузии препарата должна быть снижена. Через 3 дня введения пропофола необходимо проверить уровень липидов крови. Длительность седации пропофолом не должна превышать 7 дней.
К побочным эффектам пропофола относятся гипертриглицеридемия, острый панкреатит и миоклонус [30 - 34]. Пропофол может также вызывать аллергические реакции у пациентов с аллергией на яичный лецитин и соевое масло (так как растворен в 10% эмульсии липидов, содержащей эти вещества). В редких случаях введение пропофола связано с развитием инфузионного синдрома.Симптомы пропофолового инфузионного синдрома варьируют, однако могут включать усиление метаболического ацидоза, гипертриглицеридемию, гипотензию с повышением потребности в сосудосуживающих препаратах и аритмии. Также описаны отдельные случаи повреждения почек, гиперкалиемии, рабдомиолиза и печеночной недостаточности при инфузионном синдроме [29, 30, 35, 36]. К возможным механизмам пропофолового инфузионного синдрома относятся дисфункция митохондрий, нарушение окисления жирных кислот, изменения метаболизма углеводов в жировые субстраты и накопление метаболита пропофола. Обычно инфузионный синдром развивается при длительном введении высоких доз пропофола (>70 г/кг в минуту), однако возможен и при инфузии низких доз [37, 38]. Частота инфузионного синдрома при инфузиях пропофола составляет примерно 1% [39].Смертность от инфузионного синдрома высокая (до 33%) и возможна даже после прекращения инфузии [32]. Разная картина, отсутствие специфичности диагноза и небольшая частота инфузионного синдрома осложняет выявление этого потенциально угрожающего жизни состояния. Раннее распознавание и отмена пропофола при подозрении на инфузионный синдром крайне важно. Лечение больных с инфузионным синдромом в основном симптоматическое.
Бензодиазепины
Механизм действия бензодиазепинов основан на взаимодействии с рецепторами гамма-аминомасляной кислоты (ГАМК) в головном мозге. Препараты обладают седативным, амнестическим, снотворным и противосудорожным эффектами, но не имеют обезболивающего действия. При этом мидазолам обладает более выраженным эффектом, чем диазепам. Отмечается повышенная чувствительность к бензодиазепинам у пожилых[40]. Бензодиазепины могут вызывать угнетение дыхания, а также вызывать артериальную гипотензию, особенно в сочетании с опиоидами [41]. При длительном применении развивается толерантность к препаратам данной фармакологической группы.
Все бензодиазепины метаболизируются в печени, поэтому их выведение замедлено у пациентов с печеночной недостаточностью, пожилых, а также при одновременном применении с препаратами, ингибирующими ферментную систему цитохромаP450 и конъюгацию глюкуронида в печени [42 – 44]. При почечной недостаточности могут накапливаться активные метаболиты мидазолама и диазепама[45].
При длительном применении бензодиазепинов возможно длительное восстановление сознания после окончания введения за счет насыщения периферических тканей, особенно при печеночной, почечной недостаточности и в пожилом возрасте. Особенно большой длительностью действия обладает диазепам [46]. При применении бензодиазепинов возможна повышенная частота развития делирия.
В настоящее время наиболее часто применяется мидазолам. Начальная доза препарата 2-2,5 мг, последующие дозы – 1 мг, общая доза – 3,5 – 7,5 мг. Для пожилых пациентов начальная доза должна быть снижена до 0,5-1 мг, последующие дозы: 0,5-1 мг, общая доза: <3,5мг, так как период полувыведения увеличивается в 2 раза.
Ингаляционные анестетики
В настоящее время в анестезиологии все большую популярность завоевывают ингаляционные анестетики (ИА). Важными преимуществами ИА являются возможность эффективного мониторинга их концентрации в конце выдоха и, как следствие, хорошая управляемость анестезией. Начало и конец действия ИА наступают очень быстро, так как они выводятся через легкие и мало кумулируются печенью и почками. Современные ИА (севофлуран, десфлуран в концентрации менее 1 MAC) не оказывают отрицательного влияния на центральную гемодинамику, что имеет особое значение для больных ОРИТ, находящихся в критическом состоянии. Кроме того, в ряде работ описан кардиопротекторный эффект севофлурана [47].
В ОРИТ используется устройство для ингаляционной седации «The Anaesthetic Conserving Device» (ACD) [48], в России зарегистрировано в 2013 г. ACD включает в себя модифицированный бактериальный фильтр с отражателем анестетика и пористый испаритель. Концентрация ИА в конце выдоха контролируется с помощью газового анализатора. В качестве ИА рекомендовано использование изофлурана или севофлурана.
В настоящее время эффективность и безопасность ACD подтверждена рядом исследований, в том числе рандомизированных [49 - 52]. Использование ингаляционных анестетиков в ОРИТ вошло в рекомендации по проведению седации в Германии [53].
ACD используется вместе с обычными аппаратами искусственной вентиляции лёгких и подключается между Y-образным коннектором и интубационной трубкой, так же, как бактериальный/вирусный фильтр. Помимо этого, данная система требует использования шприцевой помпы, монитора наркозного газа и системы выведения наркозного газа (возможно использование систем с адсорберами, например, «Контрфлурана»).
Применение севофлурана для продленной седации пациентов на ИВЛ позволяет снизить дозы опиатов и полностью отменить седативные препараты, вводимые внутривенно (IIC). У ряда пациентов с нестабильной гемодинамикой, выраженной гиповолемией возможно развитие артериальной гипотензии.
Рекомендуемая концентрация севофлурана на выдохе колеблется от 0,5% (при этом скорость инфузии севофлурана через шприцевую помпу составляет от 1,5 до 2,5 мл/ч) до 1% (скорость инфузии составляет 5 – 6 мл/ч). Для достижения уровня седации -2 – 3 балла по шкале RASS применяется скорость введения севофлурана 2,5 – 5,0 мл/ч, при этом концентрация анестетика в конце выдоха составляет около 0,75%. Скорость введения изофлурана несколько меньше и не превышает 3 мл/ч.
ACD – это одноразовое устройство. Производитель рекомендует менять ACD после 24-х часов использования. Возможно использование седации с помощью ACD как в течение нескольких часов в послеоперационном периоде до экстубации пациента, так и для длительной седации [53, 54].
Седативный эффект оценивается индивидуально у каждого пациента. Как только достигается намеченный уровень седативного эффекта (по шкале седации) необходимо выполнить другую настройку в течение первого часа после использования, применив для этого болюс (0.5 мл) или изменив скорость шприцевой помпы в соответствии с избыточным или недостаточным седативным эффектом. Обычно скорость введения анестетика постепенно снижается в течение нескольких часов до половины от исходных значений.
Седация ингаляционными анестетиками противопоказана в тех случаях, когда имеются противопоказания к соответствующему препарату для ингаляционного наркоза [55].
Противопоказания к седации галогенсодержащими ингаляционными анестетиками:
Подтвержденная или подозреваемая генетическая предрасположенность к развитию злокачественной гипертермии; повышенная чувствительность к севофлурану или другим галогенизированным препаратам.
Ограничения к применению:
С осторожностью применяют при нарушении функции почек, при нейрохирургических вмешательствах, если у больного имеется угроза повышения внутричерепного давления. Повышение концентрации ИА вызывает дозозависимое снижение АД; в таких случаях его можно повысить путем уменьшения концентрации подаваемого анестетика.
В качестве перспективного средства аналгоседации может обсуждаться инертный газ ксенон. В ряде научных работдоказано, что ксенон обладает аналгетическим, гипнотическим, нейро-, кардио- и ренопротективными эффектами, а также антигипоксическим, антиоксидантным и антистрессовым действием [56 - 58]. В настоящее время существуют единичные пилотные исследования, посвященные применению ксенона для седации в интенсивной терапии [59, 60]. В исследованиях использовались лечебные ингаляции ксенон-кислородных смесей по закрытому контуру с содержанием ксенона от 20 до 50% с сохранением спонтанного дыхания через маску, получен хороший обезболивающий и седативный эффект. Очевидно, необходимо проведение более крупных рандомизированных исследований для дальнейшего изучения возможностей применения ксенона для седации в ОРИТ.
Алгоритмы седации. 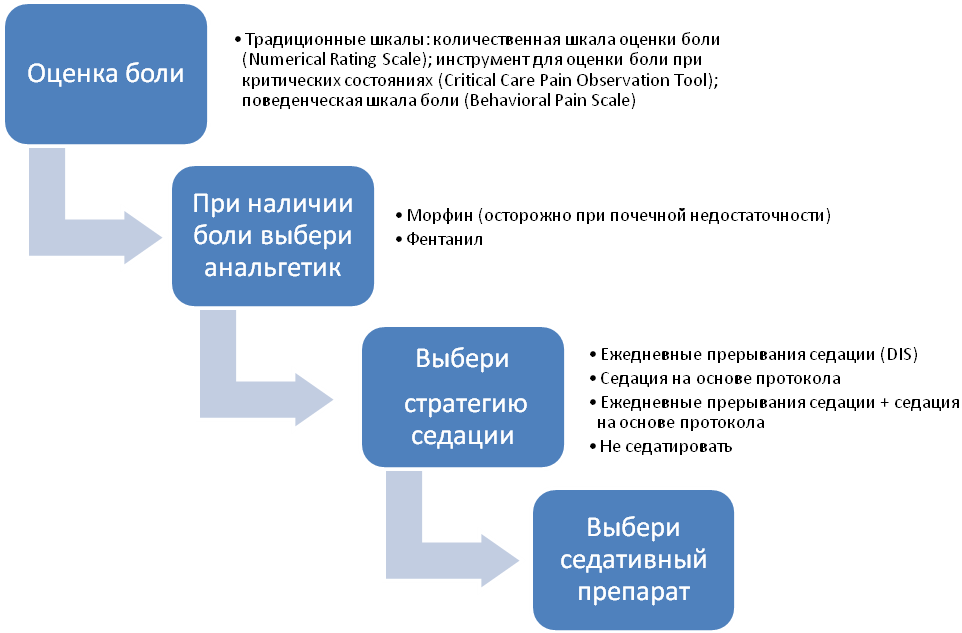
Примечание: данный алгоритм предложен с учетом концепции аналгоседации [47, 61].
Тактика седативной терапии:
Доза выбранного препарата титруется до достижения желаемого уровня седации.
1. Пропофол – при проведении постоянной инфузии доза постепенно снижается на 5 – 10 мкг/кг/мин каждые 10 минут до достижения целевой седации (учет данных оценочных шкал).
2. Бензодиазепины (мидазолам) – после достижения более глубокого уровня седации скорость введения снижается в 2 раза, а затем титруется.
3. Дексмедетомидин – нагрузочная доза не используется. В большинстве наблюдений для достижения эффекта достаточны дозировки 0,5-1,0 мкг/кг/час, а для поддержания – 0,2-0,7 мкг/кг/час [19].
4. Для седации пациентов, находящихся на ИВЛ, могут быть использованы ингаляционные анестетики (изофлуран, севофлуран). Введение начинается со скоростью 5 мл/ч для севофлурана и 3 мл/ч для изофлурана, в течение первого часа седации скорость введения корректируется (уменьшается, увеличивается или вводится болюс 0,5 мл) для достижения необходимого уровня седации по оценочным шкалам.
Такм образом, необходимо титровать дозы седативных препаратов, периодически снижая скорость введения или ежедневно прерывать седацию с целью минимизации пролонгированных седативных эффектов за исключением случаев, когда требуется глубокая седация.
При необходимости проведения аналгоседации предпочтительно использовать препараты, обладающие комбинированным (обезболивающим и седативным) эффектами, например, дексмедетомидин или ИА.
Отмена инфузии бензодиазепинов должна быть обсуждена у пациентов, получающих высокие дозы препаратов или постоянную инфузию в течение 7 дней. Пропофол в этих случаях должен быть отменен. Дозы должны снижаться систематически на 10 – 30% в день для предупреждения симптомов отмены.
Лечение избыточной седации бензодиазепинами:
- для лечения используется флумазенил (анексат) (для пациентов, получавших бензодиазепины 7 дней и более используются более низкие дозы)
- флумазенил назначается в дозе 0,2 мг (2 мл) в/в. Через 30 с состояние оценивается снова, при необходимости можно ввести дополнительно 0,3 мг (3мл) и через 30 с оценить состояние снова.
- дополнительные дозы 0,5 мг (5 мл) могут быть назначены через 30 секунд с интервалами в 1 минуту, если это необходимо. Максимальная суммарная доза – 3 мг.
Список литературы.
1. Fraser GL, Prato BS, Riker RR, Berthiaume D, Wilkins ML Evaluation of agitation in ICU patients: Incidence, severity, and treatment in the young versus the elderly. Pharmacotherapy, 2000, 20:75-82
2. Belda F.J.,Soro M., Meiser A. Sedation with Inhaled agents. Intensive Care Medicine. (Annual Update 2008).
3. Jones C, Griffiths R.D., Humphris G., Skirrow P.M. (2001). Memory, delusions, and the development of acute post-traumatic stress disorder-related symptoms after intensive care. Crit. Care Med 29:573-80
4. Scragg P., Jones A, Fauvel N. (2001) Psychological problems following ICU treatment. Anaesthesia 56: 9-14
5. Textbook of critical care. - 6th ed. [edited by jean-Louis Vincent et al.].– 1698 p.
6. Barr J., Fraser G.L., Puntillo K. et al. Clinical practice guidelines for the management of pain, agitation and delirium in adult patients in intensive care unit //Critical Care, 2013. – Vol.41, №, 1, p. 263 - 306.
7. Ann. Fr. Anesth. Réanim. 2000; 19: 98-105 Recommandations SFAR-SRLF. 1999.
8. Holzman R.S. Kullen D.J., Eichham J.H., Phillip J.H. Guidilines for sedation for non-anesthesiologists during diagnostic and therapeutic procedures. The Risk management Committee of the department of Anaesthesia of Harvard Medical School //J. Clin. Anesth. 1994. Vol.6 (4). P.265 – 276.
9. Козлов И.А. Современные подходы к седации в отделениях реанимации и интенсивной терапии //Медицинский алфавит. Неотложная медицина, 2013, №1, с. 22 – 31.
10. Cohen D., Horiuchi K., Kemper M., et al: Modulating effects of propofol on metabolic and cardiopulmonary responses to stressful intensive care unit procedures. CritCareMed1996; 24:612–617
11. The San Diego Patient Safety Council.ICU Sedation Guidelines of Care. 2009
12. Retrieved November, 2009 from wwwmemory disoder.org/glossary terms.htm
13. Jakob S.M., Ruokonen E., Grounds R.M.et al. Dexmedetomidin vs midozalam or propofol for sedation during prolonged mechanical ventilation. JAMA, 2012. – Vol. 307, №11. – P. 1151 – 1160.
14. Keating G.M., Sheritan M.H., Williamson K.A. Dexmedetomidin: a guide to its use for sedation in the US. Clin. Drug Investig. 2012; 32 (8): 561 – 567.
15. Brown E.N., Lydic R., Schiff N.D. General anaesthesia, sleep and coma //N.Engl.J.Med. 2010. Vol. 363 [27].P. 2638 – 2650.
16. Yuan X., Wu J., Wmoang Q., Xu M. The antinociceptive effect of systemic administration of a combination of low-dose tramadol and dexmedetomidine in a rat model of bone cancer pain. Eur. J. Anaesthesiol., 2014; 31: 30 – 34.
17. Brumett C.M., Hong E.K., Janda A.M. et al. Perineural dexmedetomidine added to roopivacaine for sciatic nerve block in rats prolongs the duration of analgesia by blocking the hyperpolarization-activated cation current. Anesthesiology, 2011; 115: 836 – 843.
18. Ugur F., Gilcu N., Boyaci A. Intrathecal infusion therapy with dexmedetomidine-supplemented morphine in cancer pain. Acta Anaeshesiol. Scand., 2007; 51: 388.
19. Dexdor: public assessment report. London: European Medicines Agency, 2011, Oct.4.
20. Hoy S.M., Keating J.M. Dexmedetomidine: a review of its use for sedation in mechanically ventilated patients in an intensive care setting and for procedural sedation. Drugs, 2011; 71 (11): 1481 – 1501.
21. Reede M.S., O’Sullivan K., Bates S. et al. Dexmedetomidin versus galoperidol in delirious, agitated, intubated patients: a randomized open-label trial //Crit. Care, 2009. Vol. 13(3). P. R75 – R84.
22. Никода В.Б., Бондаренко А.В., Дубов В.А., Алешин М.А., Маячкин Р.Б. Клиническое применение дексмедетомидина у больных после торакоабдоминальных хирургических вмешательств. Анестезиология и реаниматология, 2014, №5, с. 16 – 21.
23. Никода В.В., Грицан А.И., Еременко А.А., Заболотских И.Б., Киров М.Ю., Лебединский К.М., Левит А.Л. Эффективность и безопасность применения дексмедетомидина для седации больных при проведении продленной ИВЛ в отделениях реанимации и интенсивной терапии. Анестезиология и реаниматология, 2015, №5, с. 47 – 55.
24. Martin Jörg, Parsch Axel, Martin Franck et al. Practice of sedation and analgesia in German intensive care units: results of a national survey. Critical Care, 2005, vol.9, №2, R117 – 123.
25. Cormack J.R., Orme R.M., Costello T.G. The role of α2-agonists in neurosurgery. Journal of Clinical Science, 2005, vol. 12, issue 4, p. 375–378
26. Mirski M.A., Hemstreet M.K. Critical care sedation for neuroscience patients. Journal of the neurosurgical science, 2007, 261, p.16 – 34.
27. McKeage K., Perry C.M: Propofol: A review of its use in intensive care sedation of adults. CNS Drugs2003; 17:235–272
28. Carson S.S., Kress J.P., Rodgers J.E., et al: A randomized trial of intermittent lorazepam versus propofol with daily interruption in mechanically ventilated patients. Crit. Care Med2006; 34:1326–1332.
29. Barr J., Egan T.D., Sandoval N.F., et al: Propofol dosing regimens for ICU sedation based upon an integrated pharmacokinetic-pharmacodynamic model. Anesthesiology, 2001; 95:324–333
30. Riker R.R., Fraser G.L.: Adverse events associated with sedatives, analgesics, and other drugs that provide patient comfort in the intensive care unit. Pharmacotherapy, 2005; 25(5 Pt 2):8S–18S
31. Walder B., Tramèr M.R., Seeck M.: Seizure-like phenomena and propofol: A systematic review. Neurology, 2002; 58:1327–1332
32. Iyer V.N., Hoel R., Rabinstein A.A.: Propofol infusion syndrome in patients with refractory status epilepticus: An 11.-year clinical experience. Crit. Care Med, 2009; 37:3024–3030.
33. Parviainen I., Uusaro A., Kälviäinen R., et al: Propofol in the treatment of refractory status epilepticus. Intensive Care Med, 2006; 32:1075–1079
34. Voss L.J., Sleigh J.W., Barnard J.P., et al: The howling cortex: Seizures and general anesthetic drugs. Anesth. Analg., 2008; 107:1689–1703.
35. Fong J..J., Sylvia I., Barnard J.P. et al. Predictors of mortality in patients with suspected propofol infusion syndrome. Crit. Care Med. 2008; 36:2281 – 2287.
36. Didrich D.A., Brown D.R.: Analytic revewes: Propofol infusion syndrome in ICU. J. Intensive Care Med., 2011; 26: 59 - 72.
37. Merz T.M., Regli B., Roten H.U., et al. Propofol infusion syndrome: A fatal case at a low infusion rate. Anesth. Analg., 2006; 103: 1050.
38. Chukwuemeka A., Ko R., Ralf-Edwards A. Short-term low-dose propofol anaesthesia associated with severe metabolic acidosis. Anaesth. Intensive Care, 2006; 34: 651 – 655.
39. Roberts R.J., Barletta J.F, Fong J.J., et al: Incidence of propofol-related infusion syndrome in critically ill adults: A prospective, multicenter study. Crit. Care2009; 13:R169.
40. Barr J., Zomorodi K., Bertaccini E.J. et al: A double-blind, randomized comparison of i.v.lorazepam versus midazolam for sedation of ICU patients via a pharmacologic model. Anesthesiology2001; 95:286–298
41. Shafer A: Complications of sedation with midazolam in the intensive care unit and a comparison with other sedative regimens.Crit Care Med, 1998; 26:947–956
42. Swart E.L., Zuideveld K.P., de Jongh J, et al: Population pharmacodynamics modelling of lorazepam- and midazolam-induced sedation upon long-term continuous infusion in critically ill patients. Eur. J. Clin. Pharmacol., 2006; 62:185–194
43. Swart E.L., de Jongh J., Zuideveld K.P., et al: Population pharmacokinetics of lorazepam and midazolam and their metabolites in intensive care patients on continuous veno-venous hemofiltration. Am. J. Kidney Dis.2005; 45:360–371.
44. Swart EL, Zuideveld K.P., de Jongh J., et al: Comparative population pharmacokinetics of lorazepam and midazolam during long-term continuous infusion in critically ill patients. Br. J. Clin.Pharmacol, 2004; 57:135–145.
45. Swart E.L., Zuideveld K.P., de Jongh J., et al: Comparative population pharmacokinetics of lorazepam and midazolam during long-term continuous infusion in critically ill patients. Br. J. Clin.Pharmacol., 2004; 57:135–145
46. Ariano R.E. Kassum D.A., Aronson K.J.: Comparison of sedative recovery time after midazolam versus diazepam administration. Crit. Care Med, 1994; 22:1492–1496.
47. Shruti B. Patel and John P. Kress "Sedation and Analgesia in the Mechanically Ventilated Patient", American Journal of Respiratory and Critical Care Medicine, Vol. 185, No. 5 (2012), pp. 486-497.
48. De Hert S.G., Van der Linden P.J., Cromheecke S., et al (2004). Cardioprotective properties of sevoflurane in patients undergoing coronary surgery with cardiopulmonary bypass are related to the modalities of its administration. Anesthesiology, 101:299-310
49. Hellstrom J., Owall A., V. Sackey P.V. Cardiac outcome after sevoflurane versus propofol sedation following coronary bypass surgery: a pilot study. Acta Anaesthesiol. Scand., 2011; 55: 460 – 467.
50. Soro M., Gallego L., Silva V. et al. Sevoflurane and propofol during anaesthesia and the postoperative period in coronary bypass graft surgery: a double-blind randomised study. Eur J Anaesthesiol 2012; 29: 1 – 9.
51. Bellgardt M., Bomberg H., Herzog-Niescery J. et al. Survival after long-term isoflurane sedation as opposed to intravenous sedation in critically ill surgical patients. Eur J Anaesthesiol 2015; 32:1–8.
52. Mesnil M, Cap
