Аналитическая творческая работа
АНАЛИТИЧЕСКАЯ ТВОРЧЕСКАЯ РАБОТА
ПО СОЦИАЛЬНОЙ ПСИХОЛОГИИ
Болезнь Реклингхаузена
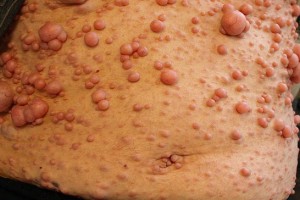 Болезнь Реклингхаузена, или нейрофиброматоз I типа – это заболевание с генетическими истоками, характеризующееся развитием множественных опухолей, поражением кожи в виде пятен цвета «кофе с молоком», веснушчатыми высыпаниями в нетипичных областях и рядом других симптомов. Болезнь довольно широко распространена среди населения планеты. Имеет прогрессирующий характер и неизлечима. Проводится только симптоматическое лечение. Специфическое лечение в настоящее время находится в стадии разработки. Из этой статьи Вы сможете узнать о причинах, симптомах, диагностике и методах лечения болезни Реклингхаузена.
Болезнь Реклингхаузена, или нейрофиброматоз I типа – это заболевание с генетическими истоками, характеризующееся развитием множественных опухолей, поражением кожи в виде пятен цвета «кофе с молоком», веснушчатыми высыпаниями в нетипичных областях и рядом других симптомов. Болезнь довольно широко распространена среди населения планеты. Имеет прогрессирующий характер и неизлечима. Проводится только симптоматическое лечение. Специфическое лечение в настоящее время находится в стадии разработки. Из этой статьи Вы сможете узнать о причинах, симптомах, диагностике и методах лечения болезни Реклингхаузена.
Заболевание имеет очень много синонимов: периферический нейрофиброматоз, нейрофибролипоматоз, классический нейрофиброматоз, глиофиброматоз, онтогенная дистрофия, врожденная нейроэктодермальная дисплазия Ван-Богарта, болезнь Ватсона. Историческое название «болезнь Реклингхаузена» корнями уходит в 1882 год, когда впервые были описаны симптомы нейрофиброматоза Фридрихом фон Реклингхаузеном.
РАСПРОСТРАНЕННОСТЬ ЗАБОЛЕВАНИЯ
 Болезнь Реклингхаузена считается весьма распространенным заболеванием. Частота встречаемости составляет 1 случай на 2500 – 7800 населения. Это очень высокий показатель. Это наиболее часто встречающееся заболевание с генетической природой. Причем, в связи с передачей по наследству, не наблюдается тенденции к уменьшению показателей распространенности.
Болезнь Реклингхаузена считается весьма распространенным заболеванием. Частота встречаемости составляет 1 случай на 2500 – 7800 населения. Это очень высокий показатель. Это наиболее часто встречающееся заболевание с генетической природой. Причем, в связи с передачей по наследству, не наблюдается тенденции к уменьшению показателей распространенности.
Болезни подвержены как мужчины, так и женщины. Расовая принадлежность не имеет значения. Нет зависимости от географического места проживания, особенностей питания и прочих факторов.
ПРИЧИНЫ БОЛЕЗНИ РЕКЛИНГХАУЗЕНА
В 90-е годы прошлого столетия была установлена точная генетическая причина заболевания: мутации в одном из генов 17-й хромосомы.
Ген ответственен за продукцию белков, подавляющих опухолевый рост в организме человека. То есть в норме, когда в организме возникает опухолевая клетка, она распознается иммунной системой и уничтожается. При болезни Реклингхаузена такая опухолевая клетка остается жить и развиваться, размножаясь и превращаясь в большую опухоль. Обычно возникают доброкачественные новообразования. Однако в 3-15% возможно озлокачествление и образование раковых клеток. В целом, риск появления злокачественных опухолей у больных с нейрофиброматозом I типа выше, чем в популяции в 200-500 раз.
Ген имеет огромные размеры по сравнению с другими. Эта особенность становится причиной высокой частоты новых мутаций. Около 50% всех случаев болезни Реклингхаузена являются наследственными (то есть мутация возникла в одном из поколений ранее и просто передавалась потомкам), вторая половина – результат новых спонтанных мутаций.
Особенностью болезни Реклингхаузена является то, что возникшая мутация имеет высокую степень клинического проявления (пенетрантность), то есть дает о себе знать практически в 100% случаев. Она не может остаться незаметной всю жизнь человека, носителя данной мутации.
Заболевание передается по наследству по аутосомно-доминантному типу, в том числе и вновь возникшие мутации. Такой тип передачи означает отсутствие связи с полом и реализацию эффекта даже при наличии только одного дефектного гена (все гены человека парные). Второй нормальный ген в данном случае не в состоянии «победить» дефектный.
СИМПТОМЫ БОЛЕЗНИ РЕКЛИНГХАУЗЕНА
Болезнь Реклингхаузена характеризуется широтой и разнообразием клинических проявлений. Среди них принято выделять опухолевые разрастания, кожные нарушения, патологию опорно-двигательного аппарата и нервной системы.
КОЖНЫЕ НАРУШЕНИЯ
Специфичным признаком нейрофиброматоза I типа являются пигментированные пятна на коже цвета «кофе с молоком». Они могут обнаруживаться уже при рождении, а могут появиться в детском возрасте. Представляют собой плоские безболезненные участки кожи от светло-бежевого до темно-коричневого и даже серо-синего цвета различной локализации и размера. Чаще они располагаются на коже туловища и конечностей. На ощупь кожа в таких участках не отличается от нормальной. Пятна постоянны, не имеют тенденции к обесцвечиванию или исчезновению. Но ведь почти у каждого человека есть родимое пятно или даже несколько, что не означает наличие нейрофиброматоза. Для болезни Реклингхаузена играет роль количество таких пятен: у взрослого их должно быть не менее 6 размером 15 мм и более. Только в таком случае это служит диагностическим критерием данного заболевания.
Еще одним кожным проявлением являются веснушчатые высыпания в виде «гроздьев». Они располагаются в нетипичных местах: в подмышечных впадинах, паховых областях, подколенных ямках. Они, также как и пятна цвета «кофе с молоком», появляются в течение жизни. Обычно их возникновение сопряжено с провоцирующим фактором: трением одежды, микротравмой, опрелостью. Веснушки на лице не считаются проявлением заболевания.
Еще одним типичным для болезни Реклингхаузена пигментным проявлением являются узелки Лиша (гамартромы). Это пигментные пятна белесого цвета на радужке глаза. Они не видны невооруженным глазом, а выявляются при осмотре в щелевой лампе. Сами по себе узелки Лиша не доставляют беспокойства. После 20-летнего возраста они обнаруживаются более, чем у 95% больных, поэтому считаются специфичным признаком нейрофиброматоза I типа. Именно узелки Лиша становятся достоверным доказательством болезни Реклингхаузена при проведении дифференциальной диагностики с другими видами нейрофиброматоза.
ОПУХОЛЕВЫЕ РАЗРАСТАНИЯ
При болезни Реклингхаузена образуется большое количество опухолевых разрастаний — нейрофибром. Они представляют собой размножившиеся клетки оболочек периферических нервов.Выглядят нейрофибромы как узелки (узлы – в зависимости от размера), могут расти на ножке или на широком основании. Узелки могут не отличаться по цвету от остальных кожных покровов, а могут иметь красновато-фиолетовый цвет. На верхушке некоторых из них могут расти волосы.
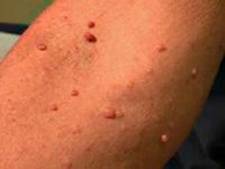 Количество нейрофибром зависит от возраста больного: в детском возрасте их очень мало, с наступлением периода полового созревания они растут, словно грибы после дождя. Численность нейрофибром у каждого больного различна. Они могут, в буквальном смысле слова, покрывать все тело, а могут быть единичными. После 30 лет нейрофибромы обнаруживаются у 94% больных.
Количество нейрофибром зависит от возраста больного: в детском возрасте их очень мало, с наступлением периода полового созревания они растут, словно грибы после дождя. Численность нейрофибром у каждого больного различна. Они могут, в буквальном смысле слова, покрывать все тело, а могут быть единичными. После 30 лет нейрофибромы обнаруживаются у 94% больных.
Размеры нейрофибром также вариабельны: от нескольких миллиметров до метра в диаметре. В связи с этим они могут обезображивать конечности и отдельные части тела, вызывая уродства. Нейрофибромы могут становиться причиной аномального увеличения конечностей, что называют слоновостью. При расположении внутри организма они сдавливают внутренние органы, нарушая их функцию, поэтому симптомы проявления таких нейрофибром весьма разнообразны, так как опухоли могут располагаться в любой части организма. Это кашель и одышка при росте нейрофибромы в зоне трахеобронхиального дерева, это нарушение пищеварения при локализации в области желудочно-кишечного тракта и так далее.
Среди нейрофибром выделяют следующие разновидности;
- кожные: не спаяны с подлежащими тканями, смещаются относительно подлежащих тканей;
- подкожные: более плотные и неподвижные образования;
- плексиформные: развиваются на крупных нервах, нередко достигают гигантских размеров.
При вовлечении в опухолевый процесс нервных корешков, нейрофибромы сопровождаются неврологической симптоматикой: болями, нарушением чувствительности, мышечной слабостью в соответствующих нерву участках.
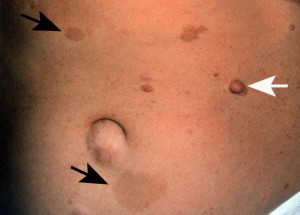 Нейрофибромы являются доброкачественными новообразованиями, но в 3-15% случаев могут трансформироваться в злокачественные.
Нейрофибромы являются доброкачественными новообразованиями, но в 3-15% случаев могут трансформироваться в злокачественные.
Кроме нейрофибром, у больных с болезнью Реклингхаузена выше, чем в популяции частота возникновения других опухолей (особенно нервной системы): астроцитом, менингиом, эпендимом, глиом зрительного нерва. Развиваясь внутри черепа, они становятся причиной повышения внутричерепного давления, мышечной слабости (парезов), утраты чувствительности, нарушений речи, зрения, слуха, психических расстройств. Довольно частой находкой при болезни Реклингхаузена является феохромоцитома – опухоль надпочечников, вызывающая неконтролируемое повышение артериального давления.
Глиома зрительного нерва обнаруживается у 15% больных. Опухоль вначале не дает никаких проявлений, а по мере своего роста может вызывать снижение зрения, боли и выпячивание глазного яблока, опущение века. Особенностью глиом зрительного нерва является склонность к рецидивированию, даже после полного, казалось бы, хирургического удаления.
ИЗМЕНЕНИЯ СО СТОРОНЫ НЕРВНОЙ СИСТЕМЫ
Неврологические расстройства при болезни Реклингхаузена (кроме симптомов, вызванных сдавлением мозга нейрофибромами и другими опухолями в нервной системе) представлены умственными нарушениями различной степени выраженности. Небольшое снижение интеллектуальных способностей, затруднения в освоении точных наук, приобретении навыков письма и чтения – это перечень наиболее часто встречаемых проблем при нейрофиброматозе I типа.
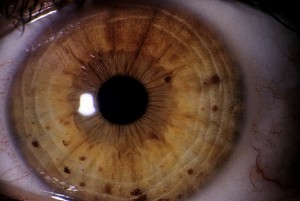
Узелки Лиша
Довольно частыми при болезни Реклингхаузена являются эпилептические припадки, депрессии и сопутствующие им симптомы. Иногда психологические расстройства связаны с косметическими дефектами, возникающими из-за большого количества нейрофибром. Больные стесняются своего внешнего вида, замыкаются в себе, что и становится причиной нарушений психики и поведения.
НАРУШЕНИЯ ОПОРНО-ДВИГАТЕЛЬНОГО АППАРАТА
Заболевание характеризуется наличием неправильного строения некоторых костей тела. Среди наиболее часто встречающихся аномалий костной системы стоит отметить следующие:
-
 недоразвитие крыла клиновидной кости;
недоразвитие крыла клиновидной кости; - кифосколиотическая деформация позвоночника;
- дефекты по краям тел позвонков, нижних краев ребер;
- незаращение дужек позвонков;
- расширение межпозвоночных отверстий;
- спондилолистез (смещение выше лежащего позвонка по отношению к ниже лежащему);
- деформация грудной клетки;
- асимметрия черепа, большой череп (макроцефалия);
- краниовертебральные аномалии (например, базилярная импрессия);
- псевдоартрозы (как результат частых переломов);
- кисты трубчатых костей;деформация трубчатых костей (например, костей голени).
В некоторых случаях аномалии позвоночника сочетаются с менингоцеле – грыжевым выпячиванием оболочек мозга.
ДРУГИЕ СИМПТОМЫ
Существует еще ряд изменений со стороны организма, регистрируемых при болезни Реклингхаузена. Они встречаются реже выше описанных симптомов, тем не менее, представляют собой диагностически ценные признаки. Это следующие изменения:
- нарушение роста;
- эндокринные нарушения полового созревания (преждевременное половое созревание, гинекомастия);
- сужение почечной и/или легочной артерий;
- легочные кисты;
- сирингомиелия.
ДИАГНОСТИКА
Существуют диагностические критерии Международного комитета экспертов по нейрофиброматозу. Для достоверного диагноза «болезнь Реклингхаузена» у пациента должно быть как минимум 2 признака из ниже перечисленных:
- 5 и более пятен цвета «кофе с молоком» больше 5 мм в диаметре до подросткового возраста и 6 и более таких пятен диаметром более 15 мм после периода полового созревания;
-
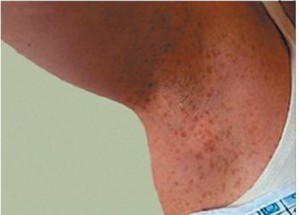 две любые нейрофибромы (или одна плексиформная);
две любые нейрофибромы (или одна плексиформная); - наличие веснушек в подмышечных и паховых складках;
- недоразвитие крыла клиновидной кости или истончение кортикального слоя трубчатых костей с образованием псевдоартроза или без него;
- глиома зрительного нерва;
- минимум два узелка Лиша;
- аналогичные изменения у одного из родственников первой линии родства (родители, дети, родные сестры и братья).
Для постановки точного диагноза необходима консультация узких специалистов: окулиста, дерматолога, невролога, хирурга (если необходимо — онколога), генетика, травматолога-ортопеда, нейрохирурга. Перечень дополнительных методов исследования, применяемых для диагностики болезни Реклингхаузена, довольно широк. Выбор метода зависит от локализации патологических изменений.
При выявлении пациента с таким диагнозом следует тщательным образом обследовать родственников, ввиду особенностей наследственной передачи заболевания (около 50% родственников, вероятнее всего, окажутся также больными). Следует учитывать, что процесс появления различных симптомов при болезни Реклингхаузена довольно динамичный. Это означает, что отсутствие многих симптомов в настоящее время не гарантирует их отсутствия в будущем. Поэтому рекомендуются периодические осмотры для исключения этой патологии.
ЛЕЧЕНИЕ
Болезнь Реклингхаузена является пока неизлечимым заболеванием. Все методы помощи относят к разряду симптоматических, которые помогают устранить ряд признаков и патологических изменений.
Основным методом лечения считается хирургическое удаление нейрофибром. Его проводят в случаях больших опухолей, которые сдавливают отдельные структуры и приводят к нарушению их функций (например, препятствие нормальному передвижению при наличии опухоли на нижней конечности, вызвавшей слоновость). В ряде случаев сдавление нервов узлами нейрофибром приводит к выраженному болевому синдрому, формированию парезов и нарушений чувствительности. Такая ситуация тоже является показанием к хирургическому вмешательству. Также оперативное лечение применяют в косметических целях, когда нейрофибромы становятся причиной обезображивания. Хирургическое лечение возможно только в случаях небольшого количества опухолей. Множественные нейрофибромы, расположенные на небольшом участке, невозможно радикально удалить.
В случаях, когда у больного выявляется злокачественная опухоль, лечение проводится с помощью всех существующих методов в онкологии. Проводится химиотерапия, лучевая терапия в комбинации с хирургическим удалением опухоли. Особенности лечения будут зависеть от разновидности опухоли.
В стадии клинического изучения в настоящее время находятся такие препараты, как Типифарниб и Пирфенидон. Но пока испытания не завершены полностью, препараты нельзя рекомендовать для лечения болезни Реклингхаузена.
Влияние на лёгкие
Болезнь Марфана является одним из факторов риска для спонтанного возникновения пневмоторакса, при котором воздух выходит из легких и занимает плевральную полость между грудной клеткой и легкими, в результате чего легкие сжимаются. Больной пневмотораксом испытывает резкую боль в груди, дышит часто и поверхностно, наблюдается выраженная отдышка. Часто проявляется бледность или синюшность кожных покровов, в частности лица (цианоз). Если заболевание не лечить, оно может привести к смерти больного.
Кроме этого, синдром Марфана может быть связан с такими заболеваниями легких как апноэ во сне (это прекращение вентиляции легких во время сна, более чем на 10 секунд) и другими идиопатическими (с неустановленной причиной) обструктивными болезнями легких.
Влияние на центральную нервную систему
Одним из последствий болезни Марфана, который может негативно повлиять на качест 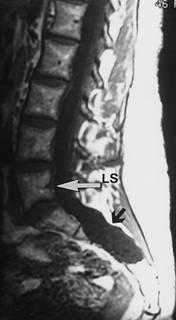 во жизни человека (хотя он не представляет угрозы жизни) является дуральная ектазия. Это ослабление и растяжение твердой оболочки мозга, а точнее соединительной ткани дурального мешка - мембраны, которая окутывает спинной мозг.
во жизни человека (хотя он не представляет угрозы жизни) является дуральная ектазия. Это ослабление и растяжение твердой оболочки мозга, а точнее соединительной ткани дурального мешка - мембраны, которая окутывает спинной мозг.
В течение длительного времени симптомы дуальной ектазии (боль в пояснице, в ногах, в области живота и таза, другие неврологические симптомы в нижних конечностях или головная боль) могут не проявляться. Или же резко исчезают, когда человек лежит на плоской ровной поверхности, на спине. При болях такого типа врачи обычно назначают рентген поясничного отдела позвоночника, хотя, как правило, дуральную ектазию невозможно заметить с помощью рентгена на ранних стадиях. Именно поэтому, ухудшение симптомов и отсутствие, какой либо другой причины боли создает необходимость проведения исследования с помощью магнитно резонансной томографии (МРТ) поясничного и крестцового отделов позвоночника. Дуральную ектазию, которая вызывает такие симптомы, будет хорошо видно на вертикальном изображении МРТ. Она будет иметь вид расширенных отростков, которые направлены к поясничным позвонкам. Другие неврологические проблемы, связанные с синдромом Марфана - это дегенеративные заболевания междупозвоночных дисков и костей спины. Также синдром Марфана является важным фактором вызывающим развитие дисфункции автономной нервной системы.
Патогенез заболевания
Синдром Марфана вызывается мутациями в гене FBN1 (15 хромосома), который кодирует гликопротеин фибрилин-1, являющийся компонентом внеклеточного матрикса. Белок фибрилин-1 имеет важное значение для правильного формирования внеклеточного матрикса, играет определенную роль при биогенезе и влияет на функционирование эластичных волокон. Кроме того, внеклеточный матрикс обеспечивает структурную целостность соединительной ткани, и играет роль резервуара для факторов роста (класс небольших природных пептидов и белков), главной целью которых является стимулирование роста клеток. Эластиновых волокон очень много во всем организме человека, но сконцентрированы они в основном в аорте, связках, в частности в цинновой связке (особая связка, с помощью которой хрусталик прикрепляется к цилиарному телу), именно поэтому эти части организма повреждаются при болезни Марфана больше всего. Для изучения механизма развития болезни Марфана была взята так называемая трансгенная мышь в организме которой в единственном экземпляре находился мутированный фибрилин-1 (мутации были аналогичны тем, которые происходят при изменении гена, кодирующего этот гликопротеин), который, как известно, является причиной развития синдрома Марфана. Этот вид мышей позволит изучить патогенез синдрома Марфана, ведь их черты болезни аналогичны человеческим. У мышей снижение нормального уровня фибрилина-1 приводит к развитию расстройств, связанных с болезнью Марфана.
Синдром Марфана существенно влияет на трансформирующий фактор роста бета (TGF-β). Ведь фибрилин-1, косвенно связывает неактивную форму TGF-β, будто поглощая ее, что в свою очередь приводит к снижению биологической активности этого фактора. Согласно простейшей схеме развития болезни Марфана, можно предположить, что снижение уровня фибрилина-1 приводит к увеличению количества TGF-β- из-за недостаточного его поглощения. И, хотя не доказано, что повышение уровня TGF-β приводит к возникновению патологий, связанных с синдромом Марфана, но, как известно, вследствие воспалительной реакции освобождения протеаз происходит постепенное ухудшение функциональности эластиновых волокон и других компонентов внеклеточного матрикса.
Достоверность данной гипотезы было подтверждена после открытия подобного синдрома с названием Синдром Лойса-Дитца (Syndrome Loeys-Dietz), который развивается при участии гена TGF-βR2 (3 хромосома), кодирующего рецептор к TGF-β. Через схожие клинические признаки эти два заболевания часто путают между собой.
Диагностика
Критерии, согласно которым диагностируют болезнь Марфана, были согласованы на международном уровне в 1996 году. Диагностика синдрома Марфана базируется на историях семей и на сочетании основных и второстепенных признаков болезни, которые в совокупности редко встречаются среди населения, но в единичном варианте могут проявляться в отдельной личности. Например - четыре нарушения со стороны опорно-двигательного аппарата сочетаются с патологиями других органов (органов системы зрения или сердечно-сосудистой системы) у одного человека - что может быть вероятным признаком синдрома Марфана.
Ниже перечисленные признаки могут быть вызваны болезнью Марфана, или могут возникнуть у людей, в которых любые нарушения отсутствуют:
• аневризма аорты или ее расширения;
• арахнодактилия;
• гастроэзофагеальная рефлюксная болезнь (ГЭРБ);
• двустворчатый аортальный клапан;
• кисты;
• кистозный медиальный некроз;
• дефекты перегородок сердца;
• дуальная ектазия;
• ранняя катаракта;
• ранняя глаукома;
• ранний остеоартрит;
• вывих хрусталика;
• эмфизема легких;
• колобома радужной оболочки;
• плоскостопие;
• рост - выше среднего;
• учащенное сердцебиение;
• грыжа;
• дисплазия суставов;
• кифоз (искривление верхнего отдела позвоночника.
• пролабирование клапанов сердца;
• неправильный прикус;
• микрогнатия (маленькая нижняя челюсть).
• пролапс митрального клапана;
• миопия (близорукость);
• обструктивные болезни легких;
• остеопения (пониженная плотность костной ткани);
• воронкообразное или килевидное искривление грудной клетки;
• пневмоторакс (коллапс легких);
• отслоения сетчатки;
• сколиоз;
• синдром апноэ;
• появление растяжек без причины (не от беременности, синдрома Кушинга или ожирения);
• нарушение роста зубов;
• узкое, худое лицо;
• артроз нижнечелюстного сустава.
Лечение
На сегодня лекарства от болезни Марфана не существует, однако за последние десятилетия продолжительность жизни с этим заболеванием значительно возросла, а клинические испытания, которые проводятся направленные на получение новых методов лечения и, на сегодня, довольно многообещающие. Синдром Марфана лечится по мере развития болезни, но особенно важным является профилактика заболевания, даже для маленьких детей, которая должна быть направлена на замедление развития аневризмы аорты.
Регулярные обзоры у кардиолога необходимые для контроля за состоянием здоровья сердечных клапанов и аорты. Цель лечения заключается в замедлении процессов прогрессирования аневризмы аорты и повреждение сердечных клапанов путем фармакологического устранения аритмий, уменьшение частоты сердечных сокращений (для чего могут быть использованы, например бета блокаторы) и снижения кровяного давления. Для его минимизации без снижения частоты сердечных сокращений, используют ингибиторы АПФ и антагонисты рецепторов ангиотензина II (также известные под названием блокаторы рецепторов ангионтензина или Сартана). Если диаметр расширение аорты становится существенным и развивается аневризма аорты, то это может стать причиной расслоения или разрыва аорты, или же приводит к недостаточности аортального или иного клапана. В таком случае необходимо проводить операцию (возможным, является трансплантация аортального клапана или проведения процедур для сохранения функциональности существующего клапана). Хотя хирургическая пересадка аорты, как и любая операция на сосудах достаточно серьезная задача, однако большинство из них можно считать успешными, если пациент добровольно и вовремя соглашается на сделку.
Операция в ситуации острого расслоения аорты или ее разрыва значительно опаснее и сложнее. Своевременным считается проведения операции на аорте, если диаметр ее корня составляет 50 мм, но каждый случай уникален и требует детальной оценки квалифицированного кардиолога.
На сегодняшний день все более распространенными становятся операции, с помощью которых осуществляется лечение клапанов. Также все более распространенными становятся методы лечения других сердечнососудистых заболеваний (нисходящей аневризмы грудной аорты и аневризмы других кровеносных сосудов). Именно поэтому, больные синдромом Марфана сегодня живут дольше, чем раньше.
Нарушение деятельности скелетной системы и системы зрения вследствие влияния болезни Марфана также серьезные, хотя и не опасны для жизни. Эти симптомы лечатся в обычном режиме, с помощью различных видов болеутоляющих средств или миорелаксантов. Очень важной в этом случае является работа физиотерапевта, который применяет TENS терапию (лечение током), ультразвук и различные способы улучшения деятельности скелетной системы, оказывает влияние на рост, длину рук и продолжительность жизни.
Физиотерапевт может также помочь улучшить функциональность опорно двигательной системы и уменьшить травматизм у лиц с болезнью Марфана. Для коррекции килевидного или воронкообразного искривления грудной клетки на западе применяются так называемые «Nuss»-процедуры. Так как очень часто болезнь Марфана приводит к патологиям позвоночника, то любое хирургическое вмешательство при осуществлении операции пациента с синдромом Марфана требует тщательного планирования и детальной визуальной диагностики различных отклонений современными методами.
Лечение спонтанного пневмоторакса, зависит от объема воздуха в плевральной полости и является уникальным для каждого больного. Если пневмоторакс незначительный, то его можно вылечить без активного вмешательства в течение одной-двух недель. Если же пневмоторакс постоянно повторяется, то больному может быть необходимо хирургическое вмешательство на грудной клетке. Для лечения пневмоторакса среднего размера нужно поставить грудной дренаж на несколько дней, конечно лечение должно осуществляться квалифицированным врачом. Если же пневмоторакс большой, то, вероятно, будет предоставлена быстрая медицинская помощь, в виде неотложной декомпрессии.
После исследования проведенного на мышах в лабораторных условиях было предположено, что антагонист рецепторов ангиотензина II лозартан, который, вероятно, блокирует активность TGF-бета, может замедлить или остановить развитие аневризмы аорты у больных с синдромом Марфана. Для сравнения эффекта действия лозартана и атенолола на аорту больных синдромом Марфана в 2007 году началось масштабное клиническое испытание под эгидой Национального института здоровья (США; деятельность которого координируется Университетом Джона Хопкинса
Также для помощи людям с синдромом Марфана и членам их семей действуют специализированные клиники и медицинские центры, проводятся генетические консультации.
Эпидемиология
Синдромом Марфана болеют как мужчины, так и женщины, при этом нет никаких этнических или географических особенностей данного заболевания. Согласно оценкам ученых один человек из 3000-5000 человек болеет синдромом Марфана. Через аутосомно-доминантный характер заболевания каждый из родителей может передать дефектные гены ребенку с вероятностью 50%. Большинство людей с синдромом Марфана имеют кого то в семье, кто уже поражен этим заболеванием, а 15-30% всех случаев связаны с новыми генетическими мутациями, которые возникают у одного ребенка на 20000 новорожденных. Синдром Марфана - это пример доминирующей негативной мутации и гаплонедостаточности. Вызванной переменной экспрессивностью, тогда как неполная пенетрантность на сегодня не является хорошо задокументированной.
Синдром Элерса - Данлоса
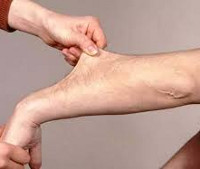
Синдром Элерса-Данлоса (несовершенный десмогенез, гиперэластическая кожа), наряду с несовершенным остеогенезом, синдромом Марфана и другими заболеваниями, относится к наследственным коллагенопатиям. Синдром Элерса-Данлоса неоднороден и включает в себя гетерогенную группу наследственных поражений соединительной ткани (соединительнотканных дисплазий), связанных с нарушением биосинтеза белка коллагена. Проявления синдрома Элерса-Данлоса носят системный характер и затрагивают опорно-двигательный аппарат, кожу, сердечно-сосудистую, зрительную, зубочелюстную и другие системы. Поэтому синдром Элерса-Данлоса представляет практический интерес не только для генетики, но и травматологии и ортопедии, дерматологии, кардиологии, офтальмологии, стоматологии.
Сложность верификации и наличие легких форм затрудняет получение точных сведений об истинной распространенности синдрома Элерса-Данлоса; частота диагностированных среднетяжелых случаев составляет 1:5 000 новорожденным, тяжелых форм - 1:100 000.
Причины синдрома Элерса-Данлоса
Различные варианты синдрома Элерса-Данлоса различаются по типу наследования, первичным молекулярным и биохимическим дефектам. Однако в основе всех клинических форм лежат мутации генов, обусловливающие количественную или структурную патологию коллагена. На сегодняшний день молекулярные механизмы синдрома Элерса-Данлоса установлены не для всех форм заболевания.
Так, известно, что I тип синдрома характеризуется снижением активности фибробластов, усилением синтеза протеогликанов, отсутствием ферментов, отвечающих за нормальный биосинтез коллагена. Синдром Элерса-Данлоса IV типа связан с недостаточностью продукции коллагена III типа; при VI типе заболевания имеет место недостаточность фермента лизилгидроксилазы, участвующего в гидроксилировании лизина в молекулах проколлагена. VII тип обусловлен нарушением превращения проколлагена I типа в коллаген; X тип - патологией плазменного фибронектина, участвующего в организации межклеточного матрикса и т. п.
Патоморфологическая картина при различных типах синдрома Элерса-Данлоса характеризуется истончением дермы, нарушением ориентации и потерей компактности коллагеновых волокон, разрастанием эластических волокон, увеличением числа сосудов и расширением их просвета.
Классификация синдрома Элерса-Данлоса
Всего выделяют 10 типов синдрома Элерса-Данлоса, различающихся по генетическому дефекту, характеру наследования и клиническим проявлениям. Рассмотрим основные из них:
I тип синдрома Элерса-Данлоса (классический тяжелого течения) – наиболее частый вариант заболевания (43% случаев) с аутосомно-доминантным типом наследования. Ведущим симптомом является гиперэластичность кожи, растяжимость которой по сравнению с нормой увеличена в 2-2,5 раза. Характерна гипермобильность суставов, носящая генерализованный характер, деформации скелета, повышенная ранимость кожи, склонность кнаружным кровотечениям, образованию рубцов, плохому заживлению ран. У части больных выявляется наличие моллюскоподобных псевдоопухолей и варикозного расширения вен нижних конечностей. Беременность у женщин с I типом синдрома Элерса-Данлоса часто осложняется преждевременными родами.
II тип синдрома Элерса-Данлоса (классический мягкого течения) – характеризуется вышеописанными признаками, но выраженными в меньшей степени. Растяжимость кожи превосходит нормальную лишь на 30%; гипермобильность отмечается преимущественно в суставах стоп и кистей; кровоточивость и наклонность к рубцеванию незначительны.
III тип синдрома Элерса-Данлоса – имеет аутосомно-доминантное наследование, доброкачественное течение. Клинические проявления включают генерализованную повышенную подвижность суставов, скелетно-мышечные деформации. Остальные проявления (гиперэластичность и рубцевание кожи, геморрагии) минимальны.
IV тип синдрома Элерса-Данлоса – встречается редко, протекает тяжело; может наследоваться различными путями (доминантно или рецессивно). Гиперэластичность кожи незначительна, отмечается повышенная подвижность только суставов пальцев рук. Ведущим проявлением данного типа заболевания является геморрагический синдром: склонность к образованию экхимозов, спонтанных гематом (в т. ч. во внутренних органах), разрывам полых органов и сосудов (в т. ч. аорты). Сопровождается высокой летальностью.
V тип синдрома Элерса-Данлоса – имеет Х-сцепленное рецессивное наследование. Характеризуется повышенной растяжимостью кожи, умеренно выраженными гипермобильностью суставов, кровоточивостью и ранимостью кожи.
VI тип синдрома Элерса-Данлоса - наследуется по аутосомно-рецессивному типу. Кроме гиперэластичности кожи, наклонности к кровотечениям, повышенной подвижности суставов, имеются мышечная гипотония, тяжелыйкифосколиоз, косолапость. Характерной чертой синдрома Элерса-Данлоса VI типа является глазной синдром, проявляющийся близорукостью, кератоконусом, косоглазием, глаукомой, отслойкой сетчатки и т. д.
VII тип синдрома Элерса-Данлоса (артроклазия) - наследуется как аутосомно-доминантно, так и аутосомно-рецессивно. Клиническую картину определяет низкий рост пациентов и гиперподвижность суставов, приводящая к частым привычным вывихам.
VIII тип синдрома Элерса-Данлоса – преимущественно наследуется аутосомно-доминантно. Ведущую роль в клинике играет хрупкость кожи, выраженный периодонтит, приводящий к ранней потере зубов.
X тип синдрома Элерса-Данлоса – характеризуется аутосомно-рецессивным наследованием; умеренной гиперэластичностью кожи и гипермобильностью суставов, стриями (полосовидной атрофией кожи), нарушением агрегации тромбоцитов.
XI тип синдрома Элерса-Данлоса – имеет аутосомно-доминантный тип наследования. У больных отмечаются рецидивирующие вывихи плечевых суставов, вывихи надколенника, встречается врожденный вывих бедра.
IX тип (Х-спепленный вариант вялой кожи) в настоящее время исключен из классификации синдрома Элерса-Данлоса. В современном варианте классификации синдрома Элерса-Данлоса рассматривается 7 основных типов заболевания:
· классический (типы I и II)
· гипермобильный (тип III)
· сосудистый (тип IV)
· кифосколиоз (тип VI)
· артроклазия (тип VIIB)
· дермоспараксис (тип VIIC)
· недостаток тенасцина-X
Симптомы синдрома Элерса-Данлоса
Ввиду того, что подробная характеристика различных типов синдрома Элерса-Данлоса дана выше, в настоящем разделе обобщим основные проявления заболевания. Поскольку соединительная ткань присутствует практически во всех органах, проявления синдрома Элерса-Данлоса носят системный, генерализованный характер.
Ведущим в клинической картине является кожный синдром: гиперэластичность кожи, которая легко собирается в складку и оттягивается. На ощупь кожа бархатистая, нежная, слабо фиксированная с подлежащими тканями, морщинистая на ладонных и подошвенных поверхностях. Гиперэластичность кожи при синдроме Элерса-Данлоса отмечается с рождения или дошкольного возраста, с годами имеет тенденцию к снижению.
Кроме, гиперрастяжимости, характерна повышенная ранимость, хрупкость кожи, обнаруживающаяся в возрасте старше 2-3-х лет. Минимальная травматизация приводит к образованию длительно не заживающих ран, на месте которых спустя время формируются атрофичные или келоидные рубцы, псевдоопухоли.
Суставные проявления синдрома Элерса-Данлоса представлены гипермобильностью (разболтанностью) суставов, которая может носить локальный (например, переразгибание межфаланговых суставов) или генерализованный характер. Суставной синдром проявляется с началом ходьбы ребенка, что приводит к повторным подвывихам и вывихам. С возрастом гипермобильность суставов обычно уменьшается.
Со стороны сердечно-сосудистой системы у детей с синдромом Элерса-Данлоса нередко выявляютсяврожденные пороки сердца, пролапс митрального клапана, аневризмы сосудов головного мозга, варикоз. Отмечается склонность к кровотечениям - экхимозам, гематомам различной локализации, носовым, десневым,маточным, желудочно-кишечным кровотечениям.
Глазные проявления синдрома Элерса-Данлоса могут включать гиперэластичность кожи век, миопию, птоз, косоглазие, разрывы роговицы и глазного яблока при минимальных механических повреждениях, спонтанную отслойку сетчатки.
Изменения скелета при синдроме Элерса-Данлоса характеризуются воронкообразной или килевиднойдеформацией грудной клетки, сколиозом, кифозом, косолапостью, неправильным прикусом, частичной адентией. Висцеральные нарушения предст
