Глава 6. лимфоциты и их роль при патологических процессах. лимфоцитоз и лимфопения.
ЛИМФОЦИТЫ И ИХ РОЛЬ ПРИ ПАТОЛОГИЧЕСКИХ ПРОЦЕССАХ. Общая характеристика лимфоцитов и их роль при патологических процессах.
Лимфоциты (Лф) заметно различаются между собой по размерам, однако, большинство представлено лейкоцитами наименьшего диаметра (8-10 мкм), которые лишь слегка больше типичных эритроцитов. Как правило, Лф округлы или овальны по форме, с круглым или эллиптическим ядром, которое может быть слегка вдавлено, образуя цитоплазматический "дворик" (рис. 24 на переднем форзаце, вид 16). Цитоплазма по площади очень невелика, но у больших лимфоцитов может быть выраженной, с отдельными розовыми гранулами. Цитоплазма красится по Романовскому-Гимза в различные оттенки голубого цвета. Хотя среди лимфоцитов различают Т-клетки , В - клетки, нулевые лимфоциты, коммитирование которых в одну из двух первых групп ещё не произошло, и большие гранулярные лимфоциты (HK-клетки) - при обычной технике окрашивания мазка крови, не используя иммунологические и гистохимические маркеры, различить их невозможно. У взрослого человека в норме относительное общее содержание лимфоцитов составляет 18-40% (Гольдберг, Гольдберг; 1976), а абсолютное - 720-3600 клеток/мкл. Плазматические клетки, важные производные B-лимфоцитов, секретирующие антитела, в норме в крови не обнаруживаются. Разнообразие, биология и функции различных Лф, а также связанные с ними нарушения подробно описаны в курсе иммунопатологии (см. т. 1, гл. 14 -17). В данном разделе повторены или добавлены лишь существенные для патофизиологических основ гематологии и онкологии детали. У эмбрирона и плода лимфопоэз идёт в желточном мешке, печени и селезёнке, а в постнатальном периоде у человека - в костном мозге и тимусе. Это - центральные лимфоидные органы, где осуществляется антигеннезависимое размножение и дифференцировка Лф. Периферические лимфоидные органы и ткани, где Лф оказываются, пройдя через кровь - арена конечных, антигензависимых стадий их созревания и клонального размножения. К ним относятся лимфоузлы, селезёнка, лимфоглоточное эпителиальное кольцо, рассеянная неинкапсулированная лимфоидная ткань ЖКТ и дыхательных путей.
Лимфоциты - нефагоцитирующие лейкоциты. В связи с этим, ни они, ни их прекурсоры не располагают ферментативно-рецепторным аппаратом фагоцитоза, что используется для дифференцировки лимфоидных и миелоидных клеток-предшественниц, например, в диагностике лейкозов (см. ниже). Зрелые Лф осуществляют высокоспецифические иммунные ответы в целях поддержания постоянства антигенного гомеостаза, а также аутоиммунные ответы, предназначенные для регуляции роста и функций собственных клеток. Для осуществления этих функций, различные клоны Лф способны к синтезу уникальных белковых распознающих молекул наборной структуры, которые находятся на их поверхности, как Т-клеточный антигенный рецептор (ТКР), либо секретируются и циркулируют в биологических жидкостях организма, как продукты плазматических клеток - иммуноглобулины (Ig). Лф могут покидать кровеносное русло, в основном - через посткапиллярные высокоэндотелиальные венулы, но, в отличие от Мф и Нф, они эмигрируют обратимо, возвращаясь по лимфоносным путям. Таким образом, лимфоциты рециркулируют между центральными и периферическими лимфоидными органами и тканями тела, осуществляя имунный надзор. Важная особенность Лф - их способность к эмпериополезу, проникновению в цитоплазму живых клеток, используемая как при эмиграции, так и при иммунном надзоре (см. т.1, с.297, 468). Лимфоциты отвечают хемотаксисом на особые хемокины, не активные в отношении других лейкоцитов. Ведущее положение среди них занимает лимфотактин, макрофагальный хемокин, пептид с молекулярной массой 12-18 кД, имеющий не менее 93-х аминокислотных остатков. Он принадлежит к С-семейству g-хемокинов и кодируется в первой хромосоме. НК -клетки и Т-лимфоциты высокочувствительны к этому хемокину и имеют распознающий его рецептор XCR1. Полустволовые клетки-предшественницы лимфопоэза служат общими предками всех Лф . Множество цитокинов стимулируют рост и созревание лимфоидных клеток .
В - лимфоциты у человека созревают в костном мозге, не проходят тимическую селекцию и в норме представлены большим количеством разнообразных клонов, каждый из которых способен синтезировать иммуноглобулиновый поверхностный рецептор, узнающий ограниченное число эпитопов. Не более 5% этих клонов соответствуют по специфичности зародышевой линии, остальные имеют иммуноглобулиновые рецепторы, являющиеся результатом соматического мутирования генов и рекомбинирования их транскриптов. Среди В-клонов всегда широко представлены аутореактивные, однако их активность сдерживается в норме механизмами относительной аутотолерантности. Рост и созревание В-клеток зависят от сигналов таких цитокинов, как фактор стволовых клеток и ИЛ-7, позднее в этих процессах участвуют ИЛ-6, ИЛ-3 и ИЛ-4, на заключительных этапах пролиферация В-клеток и их плазматизация стимулируются через клональный антигенный рецептор соответствующими антигенами, при пермиссивной роли ИЛ-6, ГМ-КСФ, ИЛ-2, ИЛ-4, ИЛ-5 и других цитокинов.
Ранние стадии дифференцировки В-Лф (пре-В-клетки) отличаются экспрессией фермента терминальной дезоксинуклеотид-трансферазы (ТДТ).
Значение этого энзима - как для иммунной системы, так и для дифференциальной диагностики в практической гематологии - трудно переоценить. ТДТ спонтанно встраивает различное произвольное число нуклеотидов в участки рекомбинации транскриптов генов иммуноглобулинов (в Т-клетках - в участки рекомбинации транскриптов генов ТКР), при этом не требуя, в отличие от классической ДНК-полимеразы, матрицы. Этот процесс значительно умножает молекулярную гетерогенность иммуноглобулинов (или ТКР), при конечном и ограниченном числе генов их цепей (т.1, с. 403).
Миелоидные (нелимфоидные) клетки не располагают ТДТ, что делает этот энзим важной отличительной особенностью лимфоидных бластов при гемобластозах. Пре-В-клетки имеют маркер CD10 (он же CALLA - или общий антиген острого лейкоза). Затем, при дозревании до стадии ранних В-клеток, экспрессируются CD19 и CD20 , а также цитоплазматические m-цепи иммуноглобулинов. Зрелые В-клетки имеют молекулы Ig на плазматической мембране (антиген sIg). Они находятся в зародышевых центрах коры лимфоузлов и в белой пульпе селезёнки. В крови их не более 20%. Их потомки, получаемые при антигензависимом этапе созревания, плазматические клетки, отличающиеся крайне развитым ЭПР и комплексом Гольджи, базофильной цитоплазмой, светлой перинуклеарной зоной, увеличенным диаметром и эксцентричным ядром - экспрессируют антигены CD38 и СD56, а молекулы Ig у них присутствуют в цитоплазме и выделяются ими в кровь. В ходе иммунного ответа возможно последовательное или альтернативное изотипическое переключение клона В-клеток на синтез антител одной специфичности, но разных классов (М, G, A, D или Е) - см. т. 1, с. 410.
В-лимфоциты необходимы для осуществления всех видов гиперчувствительности немедленного типа, являются важными организаторами всех антителоопосредованных форм иммунитета - от нейтрализации токсинов и вирусов, до опсонизации при фагоцитозе и адаптерных функций при антителозависимой К-клеточной цитотоксичности. В-лимфоциты распознают свободные антигены в растворе и могут даже презентовать те эпитопы, к которым клонально специфичны.
Они опосредуют физиологические аутоиммунные и патологические аутоаллергические реакции, способность к которым передаётся сывороткой сенсибилизированного донора. Более того, по современным представлениям, антиидиотипический механизм позволяет В-лимфоцитам изготавливать гомотела - иммуногические копии экзогенных и эндогенных биологически активных соединений, например - гормонов (Линденманн, 1979). Таким образом, по выражению Фидлера (1980), "В-лимфоцит - не только иммуноцит!." Т-лимфоциты образуются из полустволовых лимфоидных клеток костного мозга, проходя тимическую позитивную и негативную селекцию - на способность взаимодействовать с собственными белками ГКГС и отсутствие аутореактивных потенций. Таким образом, большинство аутореактивных Т-клонов подлежат элиминации (т. 1, с.383, 405, 462). Последовательные начальные стадии антигеннезависимой дифференцировки Т-клеток
· Протимоциты - носители маркеров ТДТ, CD2 (связывающий эритроциты барана) и СD7. Пролиферируют и развиваются под действием ИЛ-1,2, 6 и 7. Мигрируют из костного мозга и заселяют Т-зависимую субкапсулярную кортикальную зону селезёнки, а затем обнаруживаются в тимусе. Селезенка (путем аутофагоцитоза) и тимус (путем индукции апоптоза) выбраковывают аутореактивные клоны Т-клеток.
· Ранние тимоциты - дополнительно к вышеназванным маркерам, экспрессируют CD3 (адгезивный ко-рецептор взаимодействия Т-клетки с антигенпредставляющей клеткой -АПК) и CD5. Находятся под влиянием ИЛ-2 и ИЛ-4.
· Промежуточные тимоциты - имеют все маркеры предыдущей стадии, а также CD1 и, кратковременно - до определения их дальнейшей судьбы (коммитирования в хелперы или цитотоксические лимфоциты) - параллельно экспрессируют как CD4, так и CD8. Отвечают на те же цитокины, что и пре-тимоциты.
· Тимоциты СD4 или СD8 - альтернативные формы дифференцировки промежуточных тимоцитов. СD4-тимоциты не экспрессируют маркер CD8, cвязываются с белками ГКГС II класса и реагируют на обработанные АПК фрагменты антигенов, попавших в АПК путём фагоцитоза. Это Т-лимфоциты хелперы, регулирующие иммунный ответ В-лимфоцитов и цитотоксических лимфоцитов с помощью спектра цитокинов (см. т. 1, 404-409). В периферической крови именно они составляют большинство. CD8-тимоциты не экспрессируют маркер СD4, связываются с белками ГКГС I класса, реагируют на обработанные АПК фрагменты эндоцеллюлярных антигенов. Это - цитотоксические Т-лимфоциты, осуществляющие киллерную и, в частности - супрессорную функцию, уничтожая свои мишени с помощью перфоринового и связанных с ним механизмов (см. т.1, с. 286, 289, 457). Решающую роль в стимуляции роста и созревания Т-клеток играют такие цитокины как: ИЛ-2, ИЛ-3, ИЛ-4, а на завершающих антигензависимых этапах - костимуляция ИЛ-2 и антигеном или же антигеном и контактом с поверхностными лигандами АПК - В7-1 и В7-2. Т-клетки способны к продукции ИЛ-1, ИЛ-2, ФНО, ИЛ-4, интерферона-g - и множества других цитокинов.
· О-клетки - нулевые лимфоциты, наиболее ранние лимфоидные элементы, располагающие ТДТ, но не имеющие маркеров Т и В линий.
· НК-клетки (см. также т. 1, с. 129, 158, 188) - обладают цитотоксичностью без предварительной антигенной сенсибилизации, не рестриктированы ГКГС-белками, не варьируют структуру своих рецепторов, не выделяют антител - и поэтому не имеют ТДТ. НК-клетки - естественные киллеры - могут сканировать клетки на суммарное содержание белков ГКГС I класса и на плотность расположения этих белков с помощью особых ингибирующих рецепторов KIR (из суперсемейства иммуноглобулинов), имеющих ингибирующую тирозин-содержащую последовательность (ITIM), а также рецепторов комплекса СD94/NKG2а - из суперсемейства лектинов. Снижение плотности собственных ГКГС-I молекул на мишени, а также свойственное опухолевым клеткам повышение экспрессии так называемых MIC-молекул, взаимодействующих со стимулирующим НК-рецептором NKG2D, активируют естественные киллеры (Д'Андреа и соавт., 1996; Перуцци и соавт., 1996, Лернье, 1998; Исаков, 2001 - см. рис. 28). НК как факторы врожённого иммунитета усиливают свой потенциал под действием интерферонов и атакуют неопластические, вирус - инфицированные и поврежденные клетки, если те не имеют определённых лигандов поверхностных ингибирующих рецепторов. Киллерный эффект НК оказывают как непосредственно, так и по типу К-клеток - прикрепляясь к Fc-фрагментам противоклеточных Ig, для чего располагают Fc-рецептором. Маркером НК-клеток служит антиген CD16, подобно плазмацитам, у них есть антиген CD56. Внешне они имеют фенотип крупных клеток с отдельными гранулами в цитоплазме (большие гранулярные лимфоциты). Образование и рост НК стимулируется ИЛ-4, ИЛ-2 и, возможно, рядом других цитокинов (см. рис. в гл.3, ниже). В то же время, они сами освобождают такие паракринные сигнальные молекулы, как ГМ-КСФ, ИЛ-1, ИЛ-2, ИЛ-4 и интерферон-g.
Гетерогенность лимфоцитов велика. Большое практическое значение имеют многие другие их подгруппы, отличающиеся по своим кластерам дифференцировки и спектру паракринной секреции, в частности:
· T-хелперы 1-го типа - отличающиеся продукцией ИЛ-2, ИЛ-12 и g-интерферона и усиливающие клеточный иммунитет активаторы макрофагов, НК-клеток и СD8-лимфоцитов и ограничители анафилаксии.
· Т-хелперы 2-го типа - продуценты ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-10 и ИЛ-13, супрессоры клеточного иммунитета и усилители ГНТ и, особенно, анафилаксии (см. т.1 с. 423).
· СD5 -положительные В-клетки - производители естественных низкоаффинных аутоантител IgM (см. т. 1., с. 470, 607) к убиквитарным аутоантигенам, например - односпиральной ДНК - единственные В-лимфоциты, обладающие СD5, характерным для всех Т-клеток.
Лимфоцитарный лейкоцитоз (лимфоцитоз) характеризуется абсолютным количеством Лф в периферической крови более 5000/мкл и относительным - содержанием - более 40%. Основные причины лимфоцитоза следующие:
· физиологический лимфоцитоз - наблюдается у детей после нивелирования лимфопенического эффекта родового стресса. Начиная с 4-5 дня после рождения Лф начинают относительно преобладать в крови над гранулоцитами - "первый перекрёст". Физиологический лимфоцитоз продолжается несколько лет. В возрасте 5-6 лет имеет место выравнивание относительного содержания Лф и Нф на уровне 40-45% ("второй перекрёст"). Далее, физиологический относительный лимфоцитоз может сохраняться до 8-10 лет. При наличии железодефицита, гипотрофии и рахита возрастное преобладание Лф усугубляется и затягивается (Лавкович, Кржеминьска-Лавкович, 1964). Максимальное количество лимфоцитов, как правило, в норме не должно превышать 9000/мкл у дошкольников и 7200/мкл - у детей школьного возраста.
· Патологический лимфоцитоз - поликлональный обусловлен иммунными ответами на инфекционные или неинфекционные антигены и суперантигены, поликлональные иммуностимуляторы. Самая частая причина патологического поликлонального лимфоцитоза - иммунный ответ при инфекциях, сопровождаемых активацией клеточного иммунитета и выраженными ГЗТ. Это и понятно, если учесть, что Лф периферической крови представлены, в основном Т-клетками. Выраженный лимфоцитоз возникает при всех инфекциях, характеризующихся внутриклеточным персистированием возбудителей, а также при аутоиммунных процессах - так как при этом антигены процессируются и представляются как эндоцеллюлярные, в контексте ГКГС-белков 1 класса - и разворачивается активация CD8-положительных эффекторов ГЗТ. Не менее 4% Лф периферической крови в норме имеют увеличенные размеры, широкую цитоплазму и могут, по крайней мере - частично, относиться к НК-клеткам или к Т-лимфоцитам и В-лимфоцитам, претерпевающим в ходе штатного иммунного ответа бласт-трансформацию (см. т. 1, с. 408-410). При лимфоцитарных лейкоцитозах их доля и степень их отличия от обычных, преобладающих в крови малых лимфоцитов может сильно возрастать. В классической литературе такие лимфоциты условно именуют атипичными. Отдавая дань традиционной терминологии не следует забывать, что речь идёт при поликлональном лейкемоидном реактивном процессе о нормальных Лф, находящихся в определенном обратимом функциональном состоянии и имеющих своеобразный вид, а не о результате моноклональной необратимой неопластической трансформации - атипичных лейкозных бластах (см. ниже гл. 3). Как правило, при реактивном лимфоцитозе сменяют друг друга несколько стадий:
· лимфоцитоз на фоне гиперлейкоцитоза,
· лимфоцитоз с умеренным лейкоцитозом,
· следовая реакция - то есть, относительный лимфоцитоз без лейкоцитоза, а затем:
· нормализация картины крови.
Лимфоцитоз часто сочетается с моноцитозом (лимфомоноцитарные лейкемоидные реакции) - см. выше о моноцитах. В данном разделе представлена классификация поликлональных лимфоцитозов (лимфоидных лейкемоидных реакций), составленная с учетом данных Барта (1976), Эрслью и соавт. (1981), Бэрчану и соавт. (1985), Масловой и соавт. (1985), Воробьёва и соавт. (1986), Абдулкадырова и соавт., 1999; Розмарина (2000):
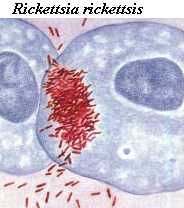
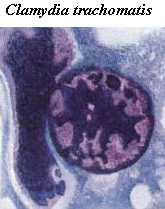
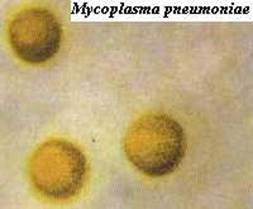
Табл. 9
Лимфоцитарные лейкемоидные реакции (поликлональные лимфоцитозы)
А. С преобладанием лимфоцитов атипичной морфологии.
1. Инфекционные:
1.1. При вирусных инфекциях:
1.1.1. Инфекционный монононуклеоз
1.1.2. Системная герпетическая инфекция
1.1.3. Цитомегаловирусная инфекция
1.1.4. Ветряная оспа и опоясывающий лишай
1.1.5. Вирусные гепатиты
1.2.При бактериальных инфекциях:
1.2. 1.Иерсиниозы
1.2.2.Болезнь кошачьих царапин
1.2.3.Листериоз
1.3.При паразитарных инфекциях:
1.3.1.Токсоплазмоз
2. Асептические иммунопатологические:
2.1. Гиперэргические реакции на лекарства
2.2. Изоиммунный Rh-конфликт
Б. С преобладанием лимфоцитов типичной морфологии.
1. Инфекционные:
1.1. При вирусных инфекциях:
1.1.1. Энтеровирусная инфекция (особенно - инфекционный лимфоцитоз)
1.1.2. Корь
1.1.3. Эпидемический паротит
1.1.4. Парвовирусная инфекция (инфекционная эритема новорождённых)
1.1.5. Грипп
1.1.6. Краснуха
1.1.7. Аденовирусная инфекция
1.1.8. Вакцинация против оспы
1.2. При бактериальных инфекциях:
1.2.1. Коклюш
1.2.2. Туберкулёз
1.2.3. Сифилис
1.2.4. Лептоспироз
1.2.5. Туляремия
1.2.6. Бруцеллез
1.2.7. Микоплазмоз
1.3. При инфекциях, вызванных невирусными доклеточными микроорганизмами
1.3.1. Риккетсиозы
1.3.2. Хламидиоз
1.4. При протозоонозах
1.4.1. Послеприступный период малярии
1.4.2. Лейшманиоз
1.4.3. Трипаносомоз
1.5. При микозах
1.5.1. Гистоплазмоз
1.5.2. Бластомикоз
1.5.3. Коккцидиоз и паракоккцидиоз
1.5.4. Споротрихоз
1.5.5. Криптококкоз
2. Асептические иммунопатологические:
2.1. РТПХ (при доказанном отсутствии цитомегаловирусной инфекции)
2.2. Сыворточная болезнь
2.3. Аутоиммунные гемоцитопении
2.4. Неспецифический язвенный колит
2.5. Аутоиммунные эндокринопатии
2.5.1. Болезнь Аддисона
2.5.2. Болезнь фон Базедова
2.5.3. Status thymicolymphaticus
2.6. Системные аутоиммунопатии с неорганоспецифическими аутоантителами
2.6.1. Системная красная волчанка
2.6.2. Синдром Шёгрена
 |  |  |  |  |
Лимфоидные лейкемоидные реакции с видоизменёнными Лф в крови могут быть асептическими и иметь иммунопатологическое происхождение. Прежде всего, это относится к случаям лимфоцитоза, спровоцированного лекарствами. В классической литературе подобные лимфоидные лейкемоидные реакции характеризовались без объяснения их механизмов - как "токсические" (Кассирский, 1953). В настоящее время выяснено, что данная группа гетерогенна по механизмам своего развития. Основную часть подобных лекарственных лимфоцитозов составляют гиперэргические реакции на лекарства как на гаптены. По этому типу формируются лимфоидные лейкемоидные реакции у некоторых пациентов, получавших ПАСК, новарсенол, атофан, дуамин. Некоторые медикаменты влияют на обмен циклонуклеотидов в лимфоцитах подобно экзотоксину возбудителя коклюша (см. ниже), являясь, по существу, химическими контрасупрессорами (хинин, хинидин). Иммуностимуляторы могут вызывать лимфоцитоз, усиливая продукцию соответствующих цитокинов (декарис). Наконец, ряд лекарств вызывает токсический, либо иммунозависимый агранулоцитоз и, таким образом, способствует относительному лимфоцитозу (см. выше - об амидопирине и аминазине). Ампициллин при аллергии на него провоцирует дерматит и иммунокомплексную реакцию, обусловливающие продукцию цитокинов, дающих лимфоцитоз. В любом случае, лекарственные лейкемоидные лимфоидные реакции нестойки и компенсируются при прекращении приёма вызвавшего их лекарства достаточно быстро. Крайне выраженный лимфоцитоз с появлением видоизмененных лимфоцитов сопровождает изоиммунный конфликт по Rh-антигену и связанную с этим гемолитическую болезнь новорождённых (см. выше гл. 1).
Многие инфекционные болезни провоцируют выраженный лимфоцитоз - но без появления "вироцитов-лимфомоноцитов", так как их возбудители не обладают свойствами поликлональных иммуностимуляторов. На одном из важнейших мест, как причина лимфоцитарных лейкоцитозов, стоит энтеровирусная инфекция (ЭИ). Так как имеется более 100 серотипов вирусов Коксэки и ECHO, являющихся её этиологическими агентами, то клиника данной инфекции крайне полиморфна. Из-за полиморфизма и большого количества стёртых форм, истинная частота ЭИ долго недооценивалась, хотя распространённость этого трудно верифицируемого заболевания является, практически, повсеместной (Колобова, Сорокина, Самарина, 2000). Среди различных форм ЭИ, протекающих всегда с лимфоцитозом (герпангина, болезнь Борнхольма - эпидемическая миальгия, серозный менингит, полиомиелитоподобные формы, гриппоподобные формы, энтеровирусная диарея, энтеровирусный энцефаломиокардит, геморрагический конъюнктивит), выделяется разновидность ЭИ, при которой лимфоцитарный лейкоцитоз достигает выдающейся степени проявления и служит основным симптомом. Это - инфекционный лимфоцитоз или болезнь Смита-Гаваша. Заболевание описано впервые отечественным автором Гавашом в 1940 г. на материале эпидемической вспышки в Новосибирской области. Через год его описал Смит. Возбудителем большинства случаев этой формы ЭИ считается вирус Коксэки B6. Есть сообщения об этиотропной роли вирусов Коксэки А и ЕСНО. Болезнь дебютирует симптомами назофаринготонзиллита, по месту внедрения вируса. Затем поражаются лимфоциты рассеянных неинкапсулированных лимфоидных скоплений ЖКТ. Отмечается энтерит и может быть "острый живот". Как и при других ЭИ, может поражаться поджелудочная железа. Вследствие аллергоидных реакций, формируются кореподобная пятнисто-папулёзная сыпь на коже и энантема. Появляется системная лимфаденопатия. Наиболее замечательный симптом болезни Смита-Гаваша - крайне выраженный лимфоцитарный лейкоцитоз. В крови от 20 000 до 200 000 (!) лейкоцитов на мкл, причём на 60-97% они представлены типичными лимфоцитами. Фаза подъёма лейкемоидной лимфоидной реакции длится 1-3 недели, нормализация числа лимфоцитов наступает на протяжении 3-х месяцев. Лимфоцитоз сопровождают нейтропения и моноцитоз. В фазу выздоровления возникает эозинофилия. Ответ острой фазы не достигает такой выраженности, как при ИМ, однако, бывает умеренная лихорадка. Атипичных лимфоцитов, чаще всего, совсем нет. Однако изредка описано появление "гистиоцитоподобных" лимфоцитов веретеновидной формы (Барта, 1976). Аутоиммунные проявления при ЭИ не исключены. Наблюдаются последствия разрушения клеток, покрытых аутоантителами, при приготовлении мазков крови - тени Боткина-Гумпрехта (характерные также для хронического лимфолейкоза - см. ниже). В позднем катамнезе у носителей антигенов ГКГС D3/D4 бывает аутоиммунный инсулит, спровоцированный перекрёстно-реагирующими пептидами энтеровирусов и цитокин-зависимой аберрантной экспрессией ГКГС-белков на b-клетках. Инсулит после ЭИ способен привести к инсулинзависимому сахарному диабету I типа (ИЗСД-I - см. т.1, с. 40,46,100; т.2, гл. 8). Умеренный лимфоцитоз, на фоне нейтропении, моноцитоза и, иногда - эозинофилии характерен для вызываемой РНК-содержащим миксовирусом кори. В лимфоузлах обнаруживаются при кори многоядерные гигантские клетки. Отмечается снижение противобактериального иммунитета и учащение аутоаллергических реакций. У переболевших корью повышена частота некоторых аутоиммунопатий, в частности - системной красной волчанки, инсулинзависимого сахарного диабета и рассеянного склероза. При присоединении бактериальных осложнений, в типичных случаях картина крови меняется и формируется нейтрофилия со сдвигом влево (Самарина, Сорокина, 2000). Другой РНК-содержащий миксовирус вызывает эпидемический паротит (свинку). Данная инфекция тоже протекает с лимфоцитозом и нейтропенией. Лимфоциты инфильтрируют слюнные железы, а иногда - яички, щитовидную железу, островки Лангерганса. В позднем катамнезе после свинки возможны аутоаллергические осложнения - вялотекущий аутоиммунный орхит, аутоиммунный инсулит. Лимфотропный РНК-вирус вызывает краснуху, для которой характерны выраженная шейно-затылочная или генерализованная лимфаденопатия, лимфоцитарный лейкоцитоз (до 90000 в мкл при 50-90% Лф), нейтропения, моноцитоз и увеличение в крови процента плазмацитов ( иногда - до 3% и более). В пунктате селезёнки, а иногда - в крови, можно обнаружить "плазмобласты" - клетки с крупным круглым ядром, сильно базофильной цитоплазмой и 3-4 нуклеолами в ядре (Барта, 1976; Кассирский, 1951). При наличии определённых особенностей гаплотипа ГКГС (D3 / D4 аллелей), перенесённая в фетальный период или в раннем детстве, краснуха предрасполагает к аутоиммунному инсулиту и ИЗСД I типа.
Невирусные инфекционные заболевания с типичным лимфоцитозом многочисленны. Большое значение в педиатрии всегда имел коклюш, до эпохи иммунопрофилактики обусловливавший в Европе и Северной Америке почти 40% детской смертности в первом полугодии жизни. Из-за снижения в последние годы иммунной прослойки в российской популяции, коклюш по-прежнему, имеет определённое распространение и его частота растёт. Болезнь вызывается грам-отрицательной палочкой Bordetella pertussis. Путь заражения - воздушно-капельный. Благодаря выделению лектинов, блокирующих слияние фагосомы с лизосомой, бордетелла тормозит завершение фагоцитоза и персистирует в мононуклеарных фагоцитах периферических лимфоидных органов, прежде всего - дыхательных путей. Коклюш - это разновидность трахеобронхита. Бордетелла выделяет экзотоксин, который активирует АТФ-азу, ингибирует продукцию ц-ГМФ и сдвигает в макрофагах, лимфоцитах и гладкомышечных клетках соотношение циклонуклеотидов (Хэдден, 1983). Сам токсин действует как кальмодулиновая аденилатциклаза и стойко связывает a-субъединицу Gi/Go белков в системе пострецепторной передачи сигнала в клетках иммунной системы и бронхов. Вследствие этого, происходит активация Лф и макрофагов, выделение цитокинов, ингибирование миграции Лф в лимфоузлы, усиливается пролиферация Лф и макрофагов, значительное количество гранулоцитов и макрофагов инфильтрирует бронхи, облегчается спазм и затрудняется релаксация гладких миоцитов, снижается бактерицидная активность гранулоцитов (см. также т.1, с. 121).. В периферической крови создаётся смешанный (истинный и перераспределительный) лимфоцитарный лейкоцитоз (15000 - 60000 в мкл при 80-90% типичных Лф). Токсин может персистировать на G-белках долгое время, даже после гибели бактерий, что предопределяет затяжное течение трахеобронхиальных симптомов болезни при отсутствии выраженного ответа острой фазы. В связи с этим, СОЭ при данной инфекции часто нормальная или сниженная. Лимфаденит и споленомегалия нетипичны, так как нет выраженной бактериемии. Патогномоничный кашель представляет собой приступы, которые носят спастический характер, провоцируются, чаще, ночью, предваряются озвученным вдохом - "репризом" и, нередко, оканчиваются мочеиспусканием или рвотой. Приступы облегчает холодный воздух. Механизм этих проявлений связан, в основном, с аллергоидным действием токсина бордетеллы на клетки бронхов, хотя в классической литературе он расценивался, как нейрорефлекторный, связанный с явлением патологической доминанты в ЦНС. Сходную, менее тяжелую картину имеет паракоклюш, при котором тоже бывает лимфоцитоз. Растворимый фактор из состава бордетеллы (компонент её экзотоксина) вызывает лимфоцитоз при введении подопытным животным. Многие близкие к иерсиниозу (см. выше) инфекции, вызываемые мелкими грам-отрицательными палочками, паразитирующими факультативно-внутриклеточно, также дают фазу септицемии, гнойно-гранулёматозный лимфаденит ("бубоны"), и лимфоцитоз (иногда - с моноцитозом). Как правило, клеток Дауни при этом в крови не наблюдается. К этой группе инфекционных причин лимфоцитоза относятся такие заболевания, как бруцеллёз, псевдотуберкулёз, туляремия, бубонная чума, мелиоидоз и сап. Умеренный лимфоцитоз без атипических Лф сопровождает многие микозы с факультативно-внутриклеточным паразитированием грибков, такие протозоонозы, как кала-азар, трипаносомоз, а при малярии наблюдается в предприступный период. Некоторые из этих поражений осложняются иммунокомплексными или аутоаллергическими процессами. Например трипаносомоз болезнь Шагаса (иная транскрипция - Чагаса) - может обернуться аутоиммунным поражением миокарда. Доклеточные паразитические организмы - риккетсии и хламидии - также размножаются интрацеллюлярно, поэтому персистируют в макрофагах и провоцируют макрофагально-лимфоцитарную ответную реакцию. Особенно выраженный лимфоцитоз и даже регионарный нагноительно-гранулёматозный лимфаденит бывает при болезни, вызванной Chlamydia trachomatis - lymphogranuloma venereum.
Аутоаллергические заболевания, вызванные цитотоксическими, иммунокомплексными и ГЗТ-механизмами, как правило, сопровождаются умеренным лимфоцитозом или лимфомоноцитозом. Многие другие варианты поликлональных лимфоцитарных реакций инфекционной и асептической этиологии не так часты и не столь выражены, поэтому они отдельно нами не расматриваются, хотя и отражены в вышеприведённой классификации. Обобщая данные о лимфоцитарных лейкемоидных реакциях, можно отметить, что выраженный лимфоцитоз очень часто предполагает нарушение регуляции аутоиммунитета и повышает риск аутоаллергических заболеваний.
Патологический лимфоцитоз - моноклонального характера - является результатом неопластических заболеваний лимфоцитов (острый лимфобластный лейкоз, хронический лимфолейкоз, лимфомы, волосатоклеточный лейкоз, миеломная болезнь - см. ниже). При данном типе патологического лимфоцитоза атипичные неопластические бластные клетки характеризуются рядом цитогенетических, иммунологических и цитохимических клональных особенностей, рассматриваемых в специальной главе 3 ниже.
 |  |  |  |  |
Лимфопения - состояние, когда в периферической крови менее 1500 Лф на мкл. Выраженный иммунодефицит соответствует лимфопении ниже 1000 Лф на мкл. Лимфопения может наступать при ограничении производства Лф, ускорении их гибели и нарушении миграции, а также в силу действия сочетаний этих причин. Ограничение производства Лф наступает, чаще всего, из-за дефицита белка в висцеральном секторе организма. Это происходит при голодании, причём особенно рано развивается белковый дефицит при квашиоркоре (см. т.2, гл. 3). Содержание Лф в крови ниже 1200 клеток на мкл, при отсутствии других возможных причин лимфопении, считается абсолютным признаком дефицита белка в висцеральном пуле организма. Другие причины ограничения лимфопоэза - костномозговая недостаточность, лучевые поражения, применение иммунодепрессантов, наследственные врождённые смешанные и Т-клеточные иммунодефициты (см. т. 1, гл. 17), например, синдром Незелова. Ограничение лимфопоэза наступает при лимфогранулёматозе и при крайне выраженных миелоидных лейкемоидных реакциях, в силу действия цитокинов, рекрутирующих клетки-предшественники и ресурсы, в основном, в миелопоэз.
Ускоренная гибель Лф типична для инфекций, непосредственно поражающих эти клетки. Лимфотропные вирусы - коревой, полиомиелитный, вирус Varicella-Zoster - ускоряют гибель Лф и могут привести к лимфопении при тяжелом течении соответствующих инфекций и малых ресурсах лимфопоэза.
Вирус иммунодефицита человека поражает CD4-положительные лимфоидные клетки, провоцирует их апоптоз и обусловливает лимфопению и панцитопению при развитии заболевания. Свой вклад в это вносит и цитостатический эффект ряда лекарств, применяемых у таких больных. Лимфопения от ускоренной гибели Лф может быть опосредована антилимфоцитарными аутоантителами, как это бывает при некоторых коллагенозах. Потеря лимфоцитов приводит к лимфопении при свищах и дренировании грудного лимфатического протока, экссудативных энтеропатиях, тяжёлой застойной сердечной недостаточности. Иногда ведущее значение для развития лимфопении в крови имеет нарушение миграции Лф. Стресс и гиперкортицизм вызывают хоуминг лимфоцитов в ткани, а при длительном течении стресса и высоких дозах глюкокортикоидов - усиление апоптоза лимфоидных клеток. В некоторых случаях гранулёматозный процесс в тканях при хронических инфекциях, сопровождаемых ГЗТ, так выражен, что при недостаточных ресурсах лимфопоэза возможна перераспределительная лимфопения в крови. Так бывает, например, при глубоких микозах и микобактериозах у некоторых пациентов. Проявления лимфопении включают, в каждом случае, снижение иммунитета и симптомы основного вызвавшего её заболевания.
 |  |  |  |  |
