Аллергические реакции, развивающиеся по IV (опосредованному Т-клетками) типу гиперчувствительности
Эта форма реактивности сформировалась на поздних этапах эволюции на основе иммунологических реакций и воспаления. Она направлена на распознавание и ограничение действия аллергена. IV тип иммунного повреждения лежит в основе многих аллергических и инфекционных заболеваний, аутоиммунных болезней, отторжения трансплантата, контактного дерматита (контактная аллергия), противоопухолевого иммунитета. Прототипом данной формы реагирования является туберкулиновая проба (реакция Манту), используемая в диагностике туберкулеза. Относительно позднее проявление этой реакции (не ранее чем через 6-8 ч в месте введения возникает покраснение, в дальнейшем эритема увеличивается с формированием через 24-48 ч после введения антигена воспалительной папулы (от лат. papula - выпуклость, прыщ) - инфильтрата округлой формы, возвышающегося над поверхностью кожи) позволило также назвать ее гиперчувствительностью замедленного типа (ГЗТ).
Этиология и особенности антигенной стимуляции при ГЗТ.Антигены, индуцирующие ГЗТ, могут иметь различное происхождение: микробы (например, возбудители туберкулеза, бруцеллеза, сальмонеллеза, дифтерии, стрептококки, стафилококки), вирусы коровьей оспы, герпеса, кори, грибы, тканевые белки (например, коллаген), антигенные полимеры аминокислот, низкомолекулярные соединения. По химической природе антигены, которые способны вызвать ГЗТ, относятся, как правило, к белковым соединениям.
Белки, вызывающие ГЗТ, отличаются низкой молекулярной массой и «слабыми» иммуногенными свойствами. Поэтому они не способны в достаточной мере стимулировать антителообразование. Иммунологическая реакция при ГЗТ обладает рядом отличительных особенностей. Иммунный ответ направлен не только к гаптену, как это имеет место при реакциях немедленного типа, но и к белку-носителю, причем специфичность в отношении антигена при ГЗТ выражена гораздо сильнее, чем при реакциях немедленного типа.
Патогенез реакций гиперчувствительности IV типа имеет следующие особенности (рис. 8-7):
I. Стадия иммунных реакций. Поступающий в организм антиген чаще всего контактирует с макрофагом, обрабатывается им, а затем в переработанном виде передается ТЫ, имеющим на своей поверхности рецепторы для антигена. Они распознают антиген, а затем с помощью интерлейкинов запускают пролиферацию эффекторных Т-клеток воспаления с фенотипами CD4+ и CD8+, а также клеток памяти, позволяющих сформировать быстрый иммунный ответ при повторном попадании антигена в организм.
После одновременного связывания Т-клетки с антигеном и молекулами главного комплекса гистосовместимости (HLA) и последующего «двойного распознавания» антигена и продуктов HLA начинается пролиферация лимфоцитов и их трансформация в бласты.
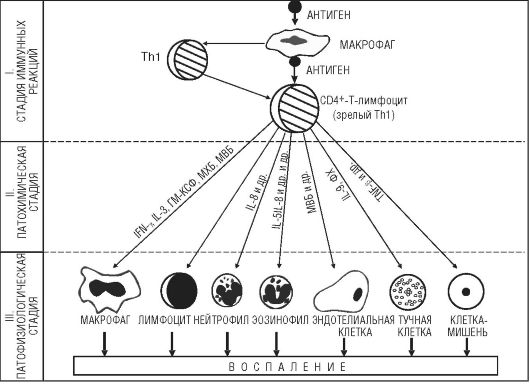 Рис. 8-7.Патогенез аллергических реакций IV (клеточно-опосредованного) типа: ГМ-КСФ - гранулоцитарно-макрофагальный колониестимулирующий фактор; МВБ - макрофагальный воспалительный белок; МХБ - макрофагальный хемоаттрактантный белок, Th (T-helper) - Т-хелпер
Рис. 8-7.Патогенез аллергических реакций IV (клеточно-опосредованного) типа: ГМ-КСФ - гранулоцитарно-макрофагальный колониестимулирующий фактор; МВБ - макрофагальный воспалительный белок; МХБ - макрофагальный хемоаттрактантный белок, Th (T-helper) - Т-хелпер
II. Стадия биохимических реакций. Антигенная стимуляция и бласттрансформация лимфоцитов сопровождаются образованием и выделением медиаторов - цитокинов (лимфокинов и монокинов), большинство из которых являются гликопротеинами. Медиаторы действуют на клетки-мишени (макрофаги и нейтрофилы, лимфоциты, фибробласты, стволовые клетки костного мозга, опухолевые клетки, остеокласты и др.), несущие на своей поверхности медиаторные рецепторы. Биологический эффект медиаторов разнообразен (табл. 8-4). Они изменяют клеточную подвижность, активируют клетки, участвующие в воспалении, способствуют пролиферации и созреванию клеток, регулируют кооперацию иммунокомпетентных клеток.
Таблица 8-4.Медиаторы аллергических реакций, опосредованных Т-клетками
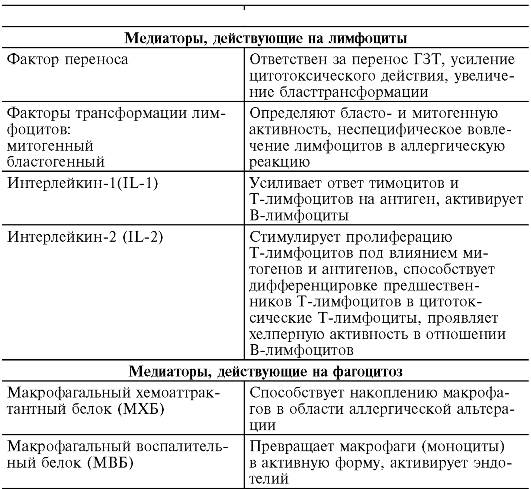
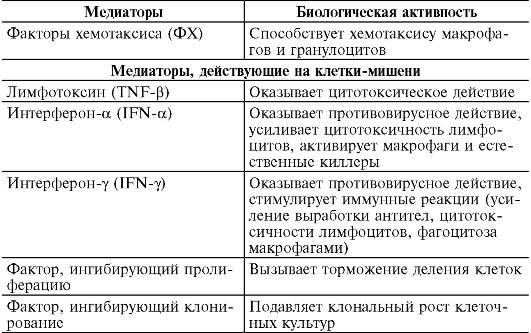 В зависимости от оказываемого эффекта медиаторы делятся на две большие группы:
В зависимости от оказываемого эффекта медиаторы делятся на две большие группы:
1) факторы, подавляющие функциональную активность клеток (макрофагальный хемоаттрактантный белок, TNF-β);
2) факторы, усиливающие функциональную активность клеток (фактор переноса; макрофагальный воспалительный белок; митогенный и хемотаксические факторы).
III. Стадия клинических проявлений зависит от природы этиологического фактора и той ткани, где «разыгрывается» патологический процесс. Это могут быть процессы, протекающие в коже, суставах, внутренних органах. В воспалительном инфильтрате преобладают мононуклеарные клетки (лимфоциты, моноциты/ макрофаги). Нарушение микроциркуляции в очаге повреждения объясняется повышением проницаемости сосудов под влиянием медиаторов (кинины, гидролитические ферменты), а также активацией свертывающей системы крови и усилением образования фибрина. Отсутствие значительного отека, так характерного для иммунных поражений при аллергических реакциях немедленного типа, связано с весьма ограниченной ролью гистамина в ГЗТ.
При гиперчувствительности IV типа иммунное повреждение развивается в результате:
1) прямого цитотоксического действия CD4+ и CD8+ Т-лимфоцитов на клетки-мишени (TNF-β и комплемент не принимают участия в этом процессе);
2) цитотоксического действия TNF-β (так как действие последнего неспецифично, повреждаться могут не только те клетки, которые вызвали его образование, но и интактные клетки в зоне его образования);
3) выделения в процессе фагоцитоза лизосомальных ферментов, повреждающих тканевые структуры (эти ферменты выделяют в первую очередь макрофаги).
Составной частью ГЗТ является воспаление, которое присоединяется к иммунной реакции действием медиаторов патохимической стадии. Как и при иммунокомплексном типе аллергических реакций, оно подключается в качестве защитного механизма, способствующего фиксации, разрушению и элиминации аллергена. Однако воспаление является одновременно фактором повреждения и нарушения функции тех органов, где оно развивается, и ему отводится важнейшая патогенетическая роль в развитии инфекционно-аллергических, аутоиммунных и некоторых других заболеваний.
ПСЕВДОАЛЛЕРГИЧЕСКИЕ РЕАКЦИИ
В аллергологической практике врачу-аллергологу все чаще приходится иметь дело с большой группой реакций, клинически часто не отличимых от аллергических. Эти реакции получили название псевдоаллергические(неиммунологические). Принципиальным их отличием от истинных аллергических реакций является отсутствие иммунологической стадии, т.е. в их развитии не принимают участие антитела или сенсибилизированные лимфоциты. Таким образом, при псевдоаллергиях выделяют только две стадии - патохимическую и патофизиологическую. В патохимической стадии псевдоаллергических реакций высвобождаются те же медиаторы, что и при истинных аллергических реакциях (гистамин, лейкотриены, продукты активации комплемента, калликреин-кининовой системы), что объясняет схожесть клинических симптомов.
Основными проявлениями псевдоаллергических реакций являются крапивница, отек Квинке, бронхоспазм, анафилактический шок.
По патогенезу различают следующие типы псевдоаллергических реакций:
1. Реакции, связанные с высвобождением медиаторов аллергии (гистамина и др.) из тучных клетокне в результате повреждения их комплексами АГ+АТ, а под действием факторов внешней среды
К IgE-независимым активаторам тучных клеток относятся антибиотики, миорелаксанты, опиаты, полисахариды, рентгеноконтрастные препараты, анафилатоксины (С3а, С5а), нейропептиды (например, субстанция Р), АТФ, IL-1 , IL-3 и др. Тучные клетки могут активироваться также под действием механического раздражения (уртикарный дермографизм) и физических факторов: холода (холодовая крапивница), ультрафиолетовых лучей (солнечная крапивница), тепла и физической нагрузки (холинергическая крапивница). Выраженным гистаминосвобождающим действием обладают многие пищевые продукты, в частности рыба, томаты, яичный белок, клубника, земляника, шоколад.
Однако повышение уровня гистамина в крови может быть связано не только с избыточным его высвобождением, но и с нарушением его инактивации гликопротеинами эпителия кишечника, белками плазмы (гистаминопексия), гистаминазой эозинофилов и печени, моноаминооксидазной системой. Процессы инактивации гистамина в организме нарушаются: при повышении проницаемости слизистой оболочки кишечника, когда создаются условия для избыточного всасывания гистамина; при избыточном поступлении гистамина в кишечник или его образовании в кишечнике; при нарушениях гистаминопектической активности плазмы; при патологии печени, в частности при токсических гепатитах (например, на фоне приема туберкулостатического препарата - изониазида), циррозе печени.
Кроме того, псевдоаллергические реакции, связанные с высвобождением медиаторов аллергии, могут развиваться у лиц, длительно применяющих ингибиторы ангиотензиногенпревращающего фермента (например, каптоприл, рамиприл и др.), участвующего в метаболизме брадикинина. Это приводит к повышению содержания брадикинина в крови и способствует развитию крапивницы, бронхоспазма, ринореи и др.
2. Реакции, связанные с нарушением метаболизма полиненасыщенных жирных кислот,в первую очередь арахидоновой кислоты. Так, при угнетении активности циклоксигеназы отмечается сдвиг метаболизма арахидоновой кислоты в направлении липоксигеназ-
ного пути. В результате образуется избыточное количество лейкотриенов. Развитие реакций этого типа может иметь место при действии нестероидных противовоспалительных препаратов, например аспирина.
3. Реакции, связанные с неконтролируемой активацией комплементав связи с наследственным дефицитом ингибитора первого компонента комплемента (врожденный ангионевротический отек Квинке), а также обусловленные неиммунологической активацией комплемента по альтернативному пути при действии яда кобры, бактериальных липополисахаридов, тромболитических средств, наркотических анальгетиков, ряда ферментов (трипсин, плазмин, калликреин и др.). Активация системы комплемента приводит к образованию промежуточных продуктов (C3а, C5a), которые вызывают высвобождение медиаторов (в первую очередь гистамина) из тучных клеток, базофилов и тромбоцитов.
Дифференциальная диагностика истинных аллергических реакций и псевдоаллергии имеет важное практическое значение, так как тактика лечения больных с истинной и ложной аллергией принципиально отличается.
АУТОИММУННЫЕ РАССТРОЙСТВА
В норме в каждом организме присутствуют антитела, В- и Т-лимфоциты, направленные против антигенов собственных тканей (аутоантигенов). Аутоантигены подразделяются на обычные(к ним относится самый широкий набор белков и других макромолекул, из которых построен человеческий организм), «секвестрированные»(они присутствуют в тканях, недоступных для лимфоцитов, таких, как мозг, хрусталик глаза, коллоид щитовидной железы, семенники) и модифицированные(т.е. образующиеся при повреждениях, мутациях, опухолевом перерождении). Следует также отметить, что некоторые антигены (например, белки миокарда и почечных клубочков) являются перекрестно реагирующимипо отношению к некоторым микробным антигенам (в частности, антигенам β-гемолитического стрептококка). Исследование аутоантител, направленных против аутоантигенов, позволило разделить их на три группы:
• естественные или физиологические(их большинство, они не могут при взаимодействии с аутоантигенами повреждать собственные ткани);
• антитела-«свидетели»(они соответствуют иммунологической памяти в отношении аутоантигенов, которые когда-либо образовывались вследствие случайных повреждений тканей);
• агрессивные или патогенные(они способны вызывать повреждение тканей, против которых направлены).
Само по себе наличие аутоантигенов, большинства аутоантител и аутореагирующих лимфоцитов не является патологическим явлением. Однако при наличии ряда дополнительных условий может запускаться и постоянно поддерживаться аутоиммунный процесс, который способствует развитию иммунного воспаления с деструкцией вовлеченных тканей, формированием фиброза и новообразованием сосудов, что в конечном счете приводит к утрате функции соответствующего органа. Важнейшими дополнительными условиями включения и поддержания аутоиммунного процесса являются:
• хронические вирусные, прионовые и другие инфекции;
• проникновение возбудителей с перекрестно реагирующими антигенами;
• наследственные или приобретенные молекулярные аномалии строения важнейших структурных и регуляторных молекул иммунной системы (включая молекулы, вовлеченные в контроль апоптоза);
• индивидуальные особенности конституции и обмена веществ, предрасполагающие к вялотекущему характеру воспаления;
• пожилой возраст.
Таким образом, аутоиммунный процесс - это иммунное воспаление, направленное против нормальных (неизмененных) антигенов собственных тканей и обусловленное образованием аутоантител и аутореактивных лимфоцитов (т.е. аутосенсибилизацией).
Условно патогенез аутоиммунных расстройств можно разделить на два этапа: индуктивный и эффекторный.
Индуктивный этаптесно связан со срывом иммунологической аутотолерантности.Толерантность к собственным антигенам организма является естественным состоянием, при котором деструктивная активность иммунной системы направлена только на внешние антигены. Процессы старения организма с иммунологической точки зрения обусловлены медленной отменой такой толерантности.
Имеется несколько механизмов, контролирующих поддержание долгосрочной аутотолерантности: клональная делеция, клональная анергия и иммуносупрессия, опосредованная Т-клетками.
Клональная делецияявляется формой центральной толерантности, которая формируется в ходе негативной селекции путем апоптоза Т-лимфоцитов (в тимусе) и В-лимфоцитов (в костном мозгу), имеющих высокоспецифические антигенраспознающие рецепторы к аутоантигенам. Клональная анергия - также форма центральной толерантности,которая характерна, главным образом, для В-клеток, имеющих BCR к растворенным аутоантигенам в низких концентрациях. При клональной анергии клетки не погибают, а становятся функционально неактивными.
Однако некоторые Т- и В-лимфоциты нередко избегают негативной селекции и при наличии дополнительных условий могут активироваться. Этому могут способствовать проникновение патогенов с перекрестными антигенами или поликлональными активаторами, сдвиг цитокинового профиля в сторону ТЫ, затяжной воспалительный процесс с поступлением в кровь и ткани множества медиаторов, которые могут модифицировать аутоантигены в очаге и др. Для сохранения толерантности периферические аутореактивные Т-лимфоциты должны быть подвержены апоптозу или стать анергичными под супрессивным влиянием цитокинов профиля Тh2. Если не происходит включение механизмов периферической толерантности,т.е. иммуносупрессии, опосредуемой Т-клетками, начинается развитие аутоиммунных расстройств. В значительной степени аутоиммунная патология (как и опухолевая прогрессия) - это дефицитность апоптоза. Описана летальная наследственная болезнь с дефектом гена, кодирующего Fas - одного из специализированных рецепторов для индукции апоптоза, которая проявляется лимфопролиферативным синдромом с системными симптомами, типичными для аутоиммунных заболеваний. Существенная роль в патогенезе многих форм аутоиммунной патологии отводится медленным вирусным и прионовым инфекциям, которые, вероятно, могут модифицировать процессы апоптоза и экспрессии важнейших регуляторных молекул. В последнее время исследуется роль ТЫ7 в развитии аутоиммунных болезней.
Одним из центральных аспектов патогенеза аутоиммунных болезней является наличие каких-либо молекулярных аномалий. Например, при ревматоидном артрите и ряде других патологий обнаружен дефект гликозилирования Fc-фрагмента собственных антител класса IgG, когда отмечается дефицит сиаловой кислоты и галактозы. Аномальные молекулы IgG образуют между собой конгломераты с сильными иммуногенными свойствами, которые ин-
дуцируют аутоиммунный ответ. Наличие молекулярных аномалий генов, ответственных за синтез цитокинов профиля Тh2, приводит к тому, что начавшийся аутоиммунный ответ не заканчивается восстановлением аутотолерантности.
Аутоиммунные болезни нередко развиваются в так называемых иммунологически привилегированных органах (мозг, хрусталик глаза, коллоид щитовидной железы, семенники); к таким патологиям относятся рассеянный склероз, симпатическая офтальмия, аутоиммунный тиреоидит Хасимото, иммунологическое бесплодие. Когда аутоантигены из этих органов оказываются в несвойственных местах (например, при травме тканевых барьеров) и имеются какие-либо дополнительные условия усиления их иммуногенности (дефицит Тп2-цитокинов, присутствие адъювантов и т.д.), включается аутоиммунный процесс.
Эффекторный этаплюбого аутоиммунного процесса протекает по одному или чаще нескольким (II, III, IV или V) типам гиперчувствительности по P.G.H. Gell и P.R.A. Coombs:
II тип: аутоиммунная гемолитическая анемия, пернициозная анемия, вульгарная пузырчатка, хроническая идиопатическая крапивница, тяжелая миастения (myasthenia gravis), аутоиммунный тиреоидит и др.;
III тип: системная красная волчанка, системные васкулиты и
др.;
IV тип: ревматоидный артрит, рассеянный склероз и др.;
V тип: иммуноопосредованный сахарный диабет I типа, болезнь Грейвса и др.
Реакции гиперчувствительности, развивающиеся по V (антирецепторному) типу,являются вариантом аутосенсибилизации, обусловленной формированием антител к компонентам клеточной поверхности (рецепторам), не обладающих комплементсвязывающей активностью. Результатом взаимодействия антител, направленных против антигенов-рецепторов, участвующих в физиологической активации клетки, является стимуляция клеток-мишеней. Такие реакции отмечаются при воздействии на клетку антител к рецепторам гормонов. Наиболее ярким их примером является образование тиреоидстимулирующих иммуноглобулинов, взаимодействующих с антигенными структурами рецептора тиреотропного гормона
(ТТГ), при болезни Грейвса1 (диффузный токсический зоб - ДТЗ), патогенез которой имеет следующие особенности:
I. Стадия иммунных реакций. При болезни Грейвса начальная фаза иммунопатологического процесса связана с миграцией и накоплением в щитовидной железе зрелых дендритных клеток, выполняющих функцию антигенпредставляющих клеток (АПК). Индукторами могут выступать антигены бактериального или вирусного происхождения, воспаление, стресс-реакция, а также йодсодержащие препараты (см. сноску). Процесс размножения и созревания дендритных клеток в щитовидной железе регулируется преимущественно грануломоноцитарным колониестимулирующим фактором (ГМ-КСФ). В эндосомах зрелых дендритных клеток происходит процессинг аутоантигена, в роли которого при болезни Грейвса выступает экстраклеточный домен рецептора к тиреотропному гормону (рТТГ) (субъединица А молекулы рТТГ). Далее процессируемый аутоантиген связывается с молекулами HLA-II и транспортируется на мембрану дендритной клетки. В результате создаются условия для включения в аутореактивный иммунный ответ CD4+ T-лимфоцитов (Th2). Взаимодействие между Th2 и дендритной клеткой осуществляется с помощью комплекса TCR/ CD3 при участии молекул адгезии (ICAM, LFA) и костимулирующих молекул (B7 на АПК и CD152 (CTLA-4) на Th2), которые взаимодействуют, связывая мембранные структуры Т-лимфоцита и дендритной клетки, и, наряду с секрецией IL-10 антигенпрезентирующими дендритными клетками, играют роль дополнительного сигнала Th2-активации.
II. Стадия биохимических реакций. Активированные CD4+ Т-клетки продуцируют цитокины (IL-4, IL-10, IFN-γ), индуцируя
1 Болезнь Грейвса является мультифакториальным заболеванием, при котором генетические особенности иммунного реагирования реализуются на фоне действия факторов окружающей среды. Наряду с генетической предрасположенностью (ассоциацией с гаплотипами HLA-B8, HLA-DR3 и HLA-DQA1O501 у европейцев, HLA-Bw36 - у японцев, HLA-Bw46 - у китайцев; CTLA-42 и др.) в патогенезе болезни Грейвса определенное значение придается психоэмоциональным и средовым факторам (стресс, инфекционно-воспалительные заболевания, прием в высоких концентрациях йода и йодсодержащих препаратов), в том числе «молекулярной мимикрии» между антигенами щитовидной железы и рядом стресс-протеинов, антигенов бактерий (Yersinia enterocolitica) и вирусов (например, вирусов группы герпеса).
CTLA-4 (cytotoxic T-lymphocyte-associated serine esterase 4) - Т-клеточный рецептор, ингибирующий пролиферацию Т-лимфоцитов и отвечающий за формирование иммунологической толерантности.
процесс дифференцировки В-лимфоцитов в плазматические клетки и продукцию ими специфических антител (IgG) к рецептору ТТГ (АТ-рТТГ). АТ-рТТГ связываются с рецептором ТТГ и приводят его в активное состояние, запуская аденилатциклазу, опосредующую наработку цАМФ, стимуляцию пролиферации тиреоцитов (что приводит к диффузному разрастанию железы), захват йода железой, синтез и высвобождение тиреоидных гормонов (трийодтиронина - Т3, тироксина - Т4).
Существует и другой путь инициации продукции тиреоидстимулирующих антител к рТТГ. В первую стадию на поверхности дендритных клеток экспрессируются белки СD1, которые распознаются натуральными киллерами (NК-клетками) и CD8+ Т-лимфоцитами. Активированные NK-клетки и СD8+ Т-клетки продуцируют цитокины (IL-4, IFN-γ), побуждающие экспрессию HLA-II, активацию Th2-лимфоцитов и формирование гуморальной реакции иммунитета.
Одновременно с образованием эффекторных лимфоцитов генерируются клетки памяти. В дальнейшем по мере прогрессирования патологического процесса арсенал АПК в щитовидной железе расширяется за счет макрофагов и В-лимфоцитов, которые обладают способностью активировать клетки памяти. Синтез IgG- аутоантител приобретает лавинообразный и непрерывный характер, поскольку не блокируется по принципу отрицательной обратной связи.
III. Стадия клинических проявлений. Клиническая картина болезни Грейвса определяется синдромом тиреотоксикоза (классическая триада симптомов - зоб, экзофтальм, тахикардия, а также похудение, потливость, нервозность, тремор, общая и мышечная слабость, быстрая утомляемость и др.). Характерный признак болезни Грейвса - претибиальная микседема1. При инструментальном обследовании (ультразвуковое исследование, сцинтиграфия) обнаруживается диффузное увеличение щитовидной железы, усиление захвата радиоактивного йода железой. Данные лабораторных исследований обнаруживают наличие высоких концентраций тиреоидных гормонов (Т3, Т4) в крови. В 70-80% случаев болезни Грейвса, наряду с АТ-рТТГ, могут определяться высокие уровни
1 Претибиальная микседема - это плотный отек передней поверхности голеней, имеющий вид асимметричных желтых или красновато-бурых бляшек, формирующийся в результате отложения в коже кислых гликозаминогликанов, в частности гиалуроновой кислоты; возможен зуд.
антител к тиреоидной пероксидазе (АТ-ТПО) и тиреоглобулину (АТ-ТГ), оказывающие цитолитическое действие.
Клиническая симптоматика аутоиммунных болезней характеризуется хроническим прогредиентным течением с деструктивными проявлениями в органах-мишенях.
