Динамика тиреоидных гормонов: нормальная физиология
Понятие «динамика тиреоидных гормонов» означает комплекс процессов синтеза гормонов в щитовидной железе, их транспорта в крови, действия и метаболизма в периферических тканях, а также комплекс регуляторных механизмов, определяющих нормальное обеспечение тканей тиреоидными гормонами. В этом разделе освещается нормальная физиология и биохимия динамики тиреоидных гормонов. Нарушения процессов транспорта, действия и метаболизма описываются в разделах, посвященных лабораторным тестам или отдельным заболеваниям.
Синтез и секреция гормонов. Синтез тиреоидных гормонов зависит от поступления в щитовидную железу достаточного количества йода — составной части активных гормонов (Т4 и Т3), интактности путей метаболизма йода в железе и одновременного синтеза
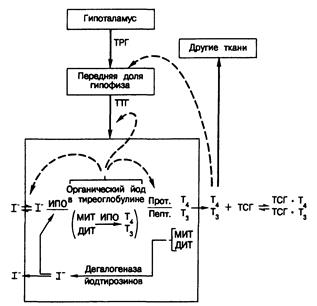
Рис. 324-2. Схема путей синтеза и секреции тиреоидных гормонов и механизмов супра- и интратиреоидной регуляции функции щитовидной железы.
Тонкими стрелками показаны пути метаболизма йода; жирными стрелками — стимулирующие влияния; пунктиром — ингибирующие влияния.
Обозначен и я : ТРГ — тиреотропин-рилнзинг гормон, ТТГ — тиреотропный гормон, И ПО — йодид-пероксидаза, Прот — тиреоидная протеаза, Пепт — тиреоидная пептидаза, МИТ — монойодтирозин, ДИТ — динодтирозин, T4 — тироксин, Т3 — 3, 5, 3' — трийодтиронин.
нормального белка, рецептирующего йод, — тиреоглобулина. Секреция достаточного количества гормонов требует в свою очередь как нормальной скорости их синтеза, так и интеграции с протекающими в железе процессами гидролиза тиреоглобулина, в результате которых активные гормоны высвобождаются. Йод проникает в щитовидную железу из крови в форме неорганического или органического йодида. Существует два источника его поступления: первый — при дейодировании тиреоидных гормонов или насыщенных йодом агентов, попавших в организм человека; и второй — с пищей, водой или лекарственными препаратами. Раньше для населения континентальной части США считалось нормой потребление с пищей примерно 200 мкг йода; этого было достаточно для поддержания концентрации йодида в плазме па уровне приблизительно 0,5 мкг/дл (5 мкг/л). Однако из-за присутствия йода в некоторых пищевых продуктах и широкого распространения йодсодержащих лекарственных средств, витаминных препаратов и антисептиков среднее потребление йода возросло до 1000 мкг в сутки, что привело к соответствующему повышению концентрации йодида в плазме крови. Йодид извлекается из плазмы щитовидной железой, почками, а также слюнными железами и в желудочно-кишечном тракте, но, поскольку йодид, выделяющийся в просвет кишечника, подвергается реабсорбции, чистый его клиренс осуществляется только щитовидной железой и почками. В сущности щитовидная железа и почки конкурируют друг с другом за йодид плазмы. Почечный клиренс зависит в основном от скорости клубочковой фильтрации, и на него не влияют гуморальные факторы или концентрация йодида в плазме. Поэтому почки в норме являются пассивными участниками этой конкуренции. Отсюда следует, что соотношение между скоростью поступления йодида в щитовидную железу и скоростью его экскреции с мочой определяется активностью именно щитовидной железы, а не почек.
Процессы синтеза и секреции активных тиреоидных гормонов можно разделить на четыре последовательных этапа (рис. 324-2). Первый включает активный транспорт йодида из плазмы в клетку щитовидной железы и в просвет фолликула. Скорость этого процесса превышает скорость пассивной днффузии йода из железы. В результате щитовидная железа оказывается способной удерживать градиент концентрации для йодида (отношение концентраций щитовидная железа/плазма) на весьма высоком уровне (до 500 и более в определенных условиях). Энергия для транспорта йодида черпается из фосфатных связей и поэтому зависит от окислительного фосфорилирования в железе. Второй этап биосинтеза гормонов включает окисление йодида в более реакционноспособную форму, способную йодировать тирозиновые остатки в молекуле тиреоглобулина — гликопротеида с мол. массой около 650 000, который синтезируется клетками фолликулов. Окисление йодида осуществляется йодид-пероксидазой, использующей перекись водорода, которая образуется но ходу окислительного обмена в железе. Йодирование органических структур происходит на границе между клеткой и коллоидом, где этому процессу подвергается в основном свежесинтезированный тиреоглобулин, поступающий путем экзоцитоза в просвет фолликула. В результате в составе пептида образуются неактивные предшественники гормонов — монойодтирозин (МИТ) и дийодтирозин (ДИТ). Затем эти йодтирозины вступают в реакцию окислительной конденсации опять-таки с помощью пероксидазы. Данная реакция протекает внутри молекулы тиреоглобулина и приводит к образованию различных йодтиронинов, включая Т4 и Т3 Хотя в крови и присутствуют небольшие количества тиреоглобулина, большая его часть некоторое время хранится в железе, играя роль запасной формы тиреоидных гормонов, или «прогормона». Высвобождение активных гормонов в кровь происходит путем пиноцитоза фолликулярного коллоида на апикальном краю клетки с образованием коллоидных капелек. Для этого процесса необходимо функционирование микротрубочек. Коллоидные капельки сливаются с тиреоидными лизосомами, образуя «фаголизосомы», в которых тиреоглобулин гидролизуется протеазами и пептидазами. Конечный этап заключается в выделении свободных йодтиронинов — Т4 и Т3 — в кровь. Единственным источником эндогенного Т4 служит щитовидная железа. В отличие от этого только около 20% образующегося в норме Т3 поступает из щитовидной железы; остальная его часть образуется во внетиреоидных тканях путем ферментативного отщепления 5'-йода от наружного кольца молекулы Т . Неактивные йодтирозины, высвобождающиеся при гидролизе тиреоглобулина, отдают свой йод под действием внутритиреоидного фермента — дегалогеназы йодтирозинов. В норме высвобождающийся таким образом йод в основном реутилизируется в синтезе гормонов, но небольшая его доля все же теряется, поступая в кровоток («утечка йода»). В патологических условиях эта доля может возрастать.
Щитовидная железа способна концентрировать и другие одновалентные анионы, такие как пертехнетат, который имеется в виде радиоактивного изотопа — натрий [99mТc] пертехнетат. В отличие от йодида пертехнетат очень мало связывается органическими соединениями. Поэтому он присутствует в щитовидной железе только короткое время. Это свойство наряду с его коротким физическим периодом полураспада делает пертехнетат ценным радионуклидом для получения изображения щитовидной железы с помощью методов сцинтилляционного сканирования.
Перечисленные выше реакции служат объектом торможения различными химическими соединениями. Их обычно называют зобогенными веществами, поскольку в силу своей способности ингибировать синтез гормонов и косвенно стимулировать секрецию ТТГ они вызывают образование зоба. Некоторые неорганические анионы, в том числе перхлорат и тиоцианат, ингибируют механизм транспорта йодида и тем самым уменьшают доступность субстрата для образования гормонов. Однако развивающиеся в результате этого зоб и гипотиреоз можно предотвратить или ликвидировать достаточно большими дозами йодида, которые обеспечивают поступление нужных его количеств в железу за счет простой диффузии. Широко используемые антитиреоидные средства, такие как производные тиомочевины и меркаптоимидазола, оказывают на биосинтез гормонов более сложное воздействие. Эти вещества, равно как и некоторые производные анилина, ингибируют первоначальное окисление (органическое связывание) йодида, снижая долю образующегося ДИТ относительно МИТ и блокируя конденсацию йодтирозинов в гормонально-активные йодгиронины. Последняя реакция наиболее чувствительна. Таким образом, синтез гормонально-активных йодтиронинов может быть резко заторможен в условиях лишь небольшого снижения общего захвата йода щитовидной железой. В отличие от эффекта одновалентных анионов зобогенное действие ингибиторов органического связывания йода не преодолевается большими его количествами. Действительно, некоторые слабые зобогенные вещества, такие как сульфонамиды и антипирин, при введении вместе с йодидом становятся почему-то даже более активными. Острое введение больших доз самого йода тоже может приводить к блокаде органического связывания и реакции конденсации. В норме это действие (эффект Вольффа — Чайкоффа) транзиторно, но у некоторых здоровых лиц, длительно получающих йод, имеет место постоянное торможение синтеза гормонов, сопровождающееся развитием зоба с гипотиреозом (йодная микседема) или без него. Большинство больных с болезнью Грейвса, особенно перенесшие радиойодтерапию или хирургическую операцию, а также больные с болезнью Хашимото чрезвычайно чувствительны к блокирующему действию йодида, и при хроническом приеме йодидов у них развивается гипотиреоз. Точно так же высокую чувствительность обнаруживает и щитовидная железа плода, и поэтому во избежание зобного гипотиреоза у плода беременные женщины не должны получать больших доз йодида. Йодид в больших дозах может ингибировать и протеолиз тиреоглобулина, т. е. высвобождение гормонов. Этот эффект легче всего проявляется в условиях гиперфункции щитовидной железы, и именно он определяет быстрое терапевтическое действие йодидов у большинства больных гипертиреозом. Литий, вводимый ряду больных с депрессивными состояниями в виде карбонатной соли. оказывает несколько эффектов на внутритиреоидный обмен йода, один из которых заключается в торможении секреции гормонов. Большие дозы дексаметазона также ингибируют секрецию гормонов и в сочетании с йодидом могут быстро уменьшать выраженность тиреотоксикоза.
