Глава 7 Клиническая фармакология Ингаляционные анестетики
На заре анестезиологии для индукции и поддержания общей анестезии использовались только ингаляционные анестетики — закись азота, эфир и хлороформ. Эфир и хлороформ уже давно запрещены к применению в США (в основном из-за токсичности и огнеопасности). В настоящее время в арсенале клинической анестезиологии находится семь ингаляционных анестетиков: закись азота, галотан (фторотан), метоксифлюран, энфлюран, изофлю-ран, севофлюран и десфлюран.
Течение общей анестезии подразделяют на три фазы: 1) индукцию; 2) поддержание; 3) пробуждение. Индукцию ингаляционными анестетиками целесообразно применять у детей, потому что они плохо переносят установку системы для внутривенных инфузий. У взрослых, наоборот, предпочтительна быстрая индукция анестезии с помощью неингаляционных анестетиков. У больных любого возраста ингаляционные анестетики широко применяют для поддержания анестезии. Пробуждение зависит главным образом от элиминации анестетика из организма.
Благодаря уникальному пути введения ингаляционные анестетики проявляют полезные фармакологические свойства, которыми неингаляционные анестетики не обладают. Например, поступление ингаляционного анестетика непосредственно в легкие (и в легочные сосуды) обеспечивает более быстрое его попадание в артериальную кровь по сравнению с внутривенно введенным препаратом. Учение о взаимоотношениях между дозой лекарственного препарата, концентрацией препарата в тканях и продолжительностью действия называется фармакокинетикой. Учение о действии препарата, включая токсические реакции, называется фармакодинамикой.
После описания общей фармакокинетики (как организм влияет на лекарственное средство) и фар-макодинамики (как лекарственное средство влияет на организм) ингаляционных анестетиков в этой главе будет охарактеризована клиническая фармакология отдельных ингаляционных анестетиков.
Фармакокинетика ингаляционных анестетиков
Механизм действия ингаляционных анестетиков остается неизвестным. Принято считать, что конечный эффект их действия зависит от достижения терапевтической концентрации в ткани головного мозга. Поступив из испарителя в дыхательный контур, анестетик преодолевает ряд промежуточных "барьеров", прежде чем достигает мозга (рис. 7-1).
Факторы, влияющие на фракционную концентрацию анестетика во вдыхаемой смеси (Fi)
Свежий газ из наркозного аппарата смешивается с газом в дыхательном контуре и только потом поступает к больному. Следовательно, концентрация анестетика во вдыхаемой смеси не всегда равна концентрации, установленной на испарителе. Реальный состав вдыхаемой смеси зависит от потока свежего газа, объема дыхательного контура и абсорбирующей способности наркозного аппарата и дыхательного контура. Чем больше поток свежего газа, меньше объем дыхательного контура и ниже абсорбция, тем точнее концентрация анестетика во вдыхаемой смеси соответствует концентрации, установленной на испарителе] клинически это со-
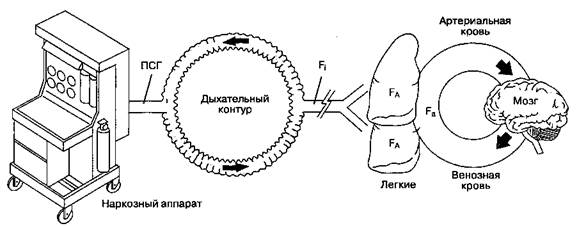
ПСГ (поток свежего газа) зависит от установок испарителя ингаляционных анестетиков
и дозиметра медицинских газов Fi (фракционная концентрация анестетика во вдыхаемой смеси) зависит от следующих
факторов:
1) скорости ПСГ
2) объема дыхательного контура
3) абсорбции анестетика в дыхательном контуре FA (фракционная альвеолярная концентрация анестетика) определяется рядом факторов:
1) поглощением анестетика кровью [поглощение = λк/г х C(A-V)]
2) вентиляцией
3) эффектом концентрации и эффектом второго газа
а) концентрационный эффект
б) эффект усиления притока
Fа (фракционная концентрация анестетика в артериальной крови) зависит от состояния вентиляционно-перфузионных отношений
Рис. 7-1."Барьеры" между наркозным аппаратом и головным мозгом
ответствие выражается в быстрой индукции анестезии и быстром пробуждении больного после ее завершения.
Факторы, влияющие на фракционную альвеолярную концентрацию анестетика (fa)
