Генетически обусловленные дефекты биосинтеза гормонов
Биосинтез любого гормона представляет собой сложный многозвеньевой процесс, в котором принимает участие множество ферментов. При этом образование любого фермента, точнее, его апофермента, определяется активностью соответствующего гена. Мутация гена может привести к недостаточности образования апофермента или такому его изменению, при котором образующийся фермент теряет свою активность. В этом случае нарушается последовательный ход биосинтеза соответствующего гормона, что обусловливает: 1) гипофункцию железы; 2) накопление в железе промежуточных продуктов биосинтеза, образующиеся до места блокады, которые выделяются в кровь и оказывают специфический патофизиологический эффект; 3) нарушение механизма обратной связи и развитие дополнительных патологических процессов. Иллюстрацией к этому служат два примера.
Первый пример. На рис. 20-3 в общих чертах представлен биосинтез кортизола и участки его блокады. В настоящее время хорошо изучены два вида блокады образования кортизола в связи с дефицитом ферментов - 21-гидроксилазы (I) в одном случае и 11 β-гидроксилазы (II) - в другом. При дефиците 21-гидроксилазы (I) процесс биосинтеза заканчивается образованием прогестерона и 17а-оксипрогестерона. Кортизол не образуется. Это по механизму обратной связи растормаживает секрецию кортиколиберина в гипоталамусе, что, в свою очередь, ведет к усилению образования АКТГ. АКТГ стимулирует стероидогенез до места блокады, и так как кортизол не образуется, то вся эта стимуляция переключается на образование D4-андростен-3,17-диона, обладающего андрогенными свойствами. Его поступление в кровь значительно увеличивается. Образующиеся в надпочечниках андрогены включаются в механизм обратной связи, регулирующей развитие половых желез, и приводят к выключению этой регуляции, что сопровождается атрофией половых желез как у мальчиков, так и у девочек. Дефект выявляется уже в период эмбрионального развития. У эмбриона женского пола к этому периоду внутренние половые органы уже заложены, поэтому избыток андрогенов вызывает их гипоплазию и развитие вирилизма. Маскулинизация продолжается и после рождения. У мальчиков же появляются признаки преждевременного полового созревания.
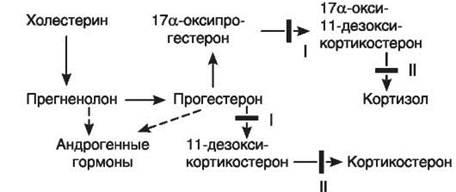
Рис. 20-3.Участки блокады биосинтеза кортизола
Подобный механизм включается и при дефекте фермента 11b-гидроксилазы (II). Кортизол также не образуется, но в этом случае (в отличие от предыдущего синдрома) накапливается избыточное количество 11-дезоксикортикостерона и 17а-окси-11- дезоксикортикостерона, первый из которых обладает выраженными минералокортикоидными свойствами. Это ведет к повышению кровяного давления. Всю эту патогенетическую цепь можно разорвать введением глюкокортикоидов (рис. 20-4). Они тормозят образование АКТГ и тем самым уменьшают образование андрогенов.
Второй пример. Биосинтез тиреоидных гормонов, происходящий в клетках фолликулярного эпителия щитовидной железы, также является сложным многозвеньевым процессом. В общих чертах он представлен на рис. 20-5 и состоит из следующих основных процессов: 1) захват йода железой и окисление его пероксидазой в молекулярный йод или йодит; 2) йодирование тирозина тирозинйодиназой с образованием монойодтирозина (МИТ) и дийодтирозина (ДИТ); тирозин, как и МИТ и ДИТ, находится в составе тиреоглобулина; 3) конденсация молекул МИТ и ДИТ с образованием трийодтиронина (Т3) и тироксина (Т4); 4) образование свободных МИТ и ДИТ и их дегалогенизация; выделяющийся при этом йод снова идет на йодирование тирозина. В связи с дефектами соответствующих ферментов каждый из указанных этапов может блокироваться.
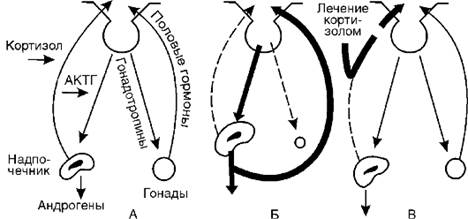
Рис. 20-4.Механизм атрофии половых желез при врожденном адреногенитальном синдроме и механизм лечебного действия кортизола: А - регуляторные механизмы в норме; Б - адреногенитальный синдром; В - патогенетическая терапия кортизолом (по Гоффу); АКТГ - адренокортикотропный гормон
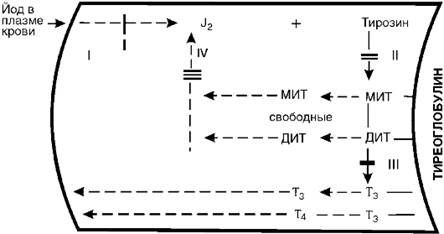
Рис. 20-5.Участки блокады биосинтеза тиреоидных гормонов. МИТ - монойодтирозин, ДИТ - дийодтирозин
Установлена возможность блокады йодзахватывающей системы (I). Для этого случая характерна неспособность железы поглощать J131 при соответствующем исследовании. Исправление этого дефекта достигается введением в организм небольших доз йодистого калия, который в связи с повышением его концентрации в крови, в силу диффузии проникает в щитовидную железу и, таким образом, компенсирует дефект йодзахватывающей системы. II - блокада йодирования тирозина. Поглощенный йод сохраняется в железе в неорганической форме и не включается в тирозин. Этот дефект на данном этапе компенсируется введением готовых тиреоидных гормонов. III - дефект конденсации йодтирозинов. Характеризуется накоплением промежуточных продуктов - МИТ и ДИТ и следовыми количествами Т3 и Т4. Компенсация дефекта проводится также введением гормонов. IV - дефект йодтирозин-дегалогеназы. Он характеризуется угнетением дегалогенизации МИТ и ДИТ. Эти продукты накапливаются, выделяются в кровь и выводятся из организма. Организм теряет йод, развивается йодная недостаточность. Компенсация дефекта может быть обеспечена введением в организм йодистого калия. Каждый из указанных дефектов приводит к недостаточному образованию тиреоидных гормонов. В результате возникает гипофункция щитовидной железы, сопровождаемая развитием зоба (увеличением щитовидной железы) и кретинизма. Последнее объясняется тем, что эти дефекты возникают еще до рождения или в детском возрасте.
