Иллюстрация роли ионов в формировании потенциала покоя
ФИЗИОЛОГИЯ ВОЗБУДИМЫХ ТКАНЕЙ
Основой приспособительных реакций организма является раздражимость – способность живых структур реагировать на действие различных факторов среды, изменяя текущую активность. Раздражимостью обладают все ткани животных и растений. В процессе эволюции происходила постепенная дифференциация тканей, обеспечивающих адаптивные реакции. Так возникло новое свойство этих тканей – возбудимость. Под этим термином понимаютспособность клеток и тканей отвечать на действие раздражителя специфической реакцией – генерацией процесса возбуждения. Возбуждение – сложный биологический процесс, характеризующийся временной деполяризацией мембран клеток, изменением обменных процессов, теплообразования и других физиологических и биофизических явлений.
Торможение, как и возбуждение, возникает в ответ на действие раздражителя, но при этом функциональная активность структуры снижается.
Свойство возбудимости и признаки возбуждения наиболее отчетливо выражены у нервной и мышечной ткани. Эти ткани и относят к возбудимым.
Возбудимость различных тканей неодинакова. Ее оценивают по минимальной силе раздражителя, способного вызвать возбуждение (порогу раздражения).
Факторами, внешней или внутренней среды, вызывающими возбуждение – раздражителями– могут быть любые действующиеиз внешней среды или возникающие в самом организме воздействия.
По степени приспособленности живых тканей к их восприятию, раздражители условно разделяют на адекватные и неадекватные. К действию адекватных раздражителей структура максимально приспособлена. Например, адекватным раздражителем для рецепторов сетчатки является свет, для барорецепторов – изменения давления. Неадекватные раздражители действуют на рецепторы, не специально приспособленные для их восприятия. Однако сила такого воздействия должна значительно превышать пороговый уровень возникновения возбуждения при адекватном раздражении.
Биоэлектрические явления в возбудимых тканях.
Природа возбуждения
Согласно мембранной теории, все клетки имеют мембрану, которая, обладая специфической ионной проницаемостью, несет определенный электрический заряд – мембранный потенциал, способный изменяться при действии раздражителя. Поэтому основные свойства возбудимых тканей определяются структурно-функциональными особенностями их мембран.
Возбуждение представляет собой систему физико-химических процессов, в результате которых происходит быстрое и кратковременное изменение мембранного потенциала.
Первые исследование электрической активности живых тканей были начаты более двух столетий назад. В 1780 году итальянский физиолог, профессор анатомии в Болонье Луиджи Гальвани обнаружил, что если к изолированной мышце лягушки прикоснуться одновременно двумя разными металлическими предметами, то мышца сократится. Способность мышц препарированной лягушки сокращаться под влиянием электрического тока Гальвани объяснил существованием «животного электричества».
Физик А. Вольта, осуществив серию экспериментов, пришел к другому заключению. Источником тока, по его мнению, является не животное электричество, а разность потенциалов в месте контакта разнородных металлов – меди и железа, а нервно-мышечный препарат является лишь проводником электричества. Л. Гальвани ответил оппоненту, усовершенствовав опыт – исключив из него металлы. Он препарировал седалищный нерв вдоль бедра лягушки, затем набрасывал нерв на мышцы голени, наблюдая сокращение мышцы. Тем самым Л. Гальвани доказал существование «животного электричества».
Позднее Э.Г. Дюбуа-Реймон установил, что при набрасывании нерва, между поврежденным, отрицательно заряженным и неповрежденным, положительно заряженным участками мышцы, возникает ток, который раздражает нерв и вызывает сокращение мышцы. Так было показано, что наружная поверхность мышечных клеток заряжена положительно по отношению к внутреннему содержимому.
Лабораторная работа № 1
Иллюстрация роли ионов в формировании потенциала покоя
Потенциал покоя — это разность электрических потенциалов между внутренней и наружной средами клетки в состоянии ее покоя.
Непосредственной причиной формирования потенциала покоя является неодинаковая концентрация анионов и катионов внутри и вне клетки - следствие разной проницаемости клеточной мембраны для различных ионов и работы ионных насосов, главную роль среди которых играет NA+/K+-нacoc, что осуществляется непосредственной затратой энергии (АТФ). Одна молекула АТФ обеспечивает один цикл работы NA+/K+-нacocа, при этом переносится 3Na+ из клетки и возвращается 2К+ в клетку.
Если заблокировать выработку энергии, потенциал покоя клетки постепенно уменьшается, его величина приближается к уровню, наблюдаемому при установлении равновесия Доннана при наличии разной проницаемости мембраны, разделяющей растворы различной концентрации и содержащие разные по величине ионы.
Если бы проницаемость клеточной мембраны для всех ионов быт одинаково высокой (все ионы могли бы проходить свободно через клеточную мембрану), то потенциал покоя значительно снизился бы и составлял только 5... 10 мВ за счет работы Na+/K+-нacocа; (в норме величина потенциала покоя в нейронах и исчерченных миоцитах составляет 50...90 мВ).
Для иллюстрации непосредственной причины существования потенциала покоя (разной концентрации анионов и катионов внутри и вне клетки) разработан модельный опыт с растворами CuSO4 различной концентрации (В.М. Смирнов).
Для работы необходимы: милливольтметр; раствор CuSO4 (1% и 2%); дистиллированная и водопроводная вода; устройство, обеспечивающее создание в его камерах растворов с разной концентрацией анионов и катионов.
Конструкция устройства весьма проста, его легко изготовить в условиях кафедры. Состоит устройство из корпуса в виде коробки (дерево, пластмасса) и укрепленных в ней четырех пар стеклянных банок (например, флаконы из-под пенициллина (рис. 1)).
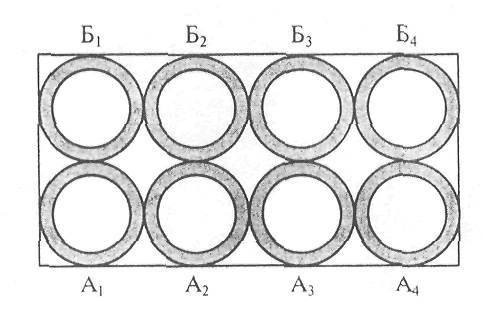
Рис. 1. Устройство для иллюстрации роли ионов
в формировании потенциала покоя:
А1-А4 - банки внутренней среды; Б1-Б4 — банки внешней среды.
Каждая пара банок выполняет роль клетки с окружающей средой: банка А - внутренняя среда клетки, банка Б - внешняя среда клетки. Банки каждой пары соединены между собой серебряной (медной) проволокой в виде скрепки. Эти электроды должны быть в изоляторе (свободные только концы - срез) для исключения короткого замыкания клемм батарейки. Первую пару банок (А1-Б1) заполняют дистиллированной водой, вторую (А2-Б2) - водопроводной, третью (А3-Б3) - 1% раствором CuSO4, четвертую (А4-Б4) - 2% раствором CuSO4. Для забора противоположных но заряду ионов из растворов используют батарейку от карманного фонарика (в данном случае плоская, 4,5 В) и электроды в виде медных или серебряных пластин размером 1x3 см, к которым припаяны медные гибкие провода. К свободным концам проводов припаивают медную проволоку диаметром 1,0-1,5 мм и длиной 5-7 см, концы которой затачивают в виде иглы. Во время исследования концы вводят под пластины батарейки; этого достаточно для обеспечения хорошего контакта.
Ход работы. Первая серия исследования контрольная. Проверьте наличие или отсутствие разности электрических потенциалов в каждой паре банок (А-Б и А-А) с помощью милливольтметра до забора ионов из банок по двум схемам и полученные показатели запишите в тетрадь.
Схема 1. А1-Б1 = ... мВ; А2-Б2 = ... мВ; А3-Б3 = ... мВ; А3-Б3 = ... мВ; А4-Б4 = ... мВ, т.е. между банками с одинаковыми жидкостями (одинаковая концентрация ионов или их отсутствие - дистиллированная вода).
Схема 2. А1-А2 = ... мВ; А1-А3 = ... мВ; А1-А4 = ... мВ; A2-А3 = ... мВ; А2-A4 = ... мВ; А3-A4 = ... мВ (между банками с жидкостями с разной концентрацией ионов).
При измерении разности электрических потенциалов между парами банок с разными жидкостями (схема 2) используйте дополнительный электрод-скрепку и помещайте его по очереди между банками, в которых измеряете разность электрических потенциалов.
Вторую серию исследований проведите после забора катионов К+ из банок А и анионов SO2-4 из банок Б, для чего введите катод источника постоянного тока в банку А1 (внутренняя среда клетки), а анод - в банку Б1 (внешняя среда клетки) первой пары банок на 3 мин. Помните, что растворы в банках должны быть соединены электродом-скрепкой. Через 3 мин выньте оба электрода, проверьте с помощью милливольтметра, имеется ли разность электрических потенциалов между банкой А1 и банкой Б1. Проведите подобные исследования и в остальных парах банок: А2-Б2, А3-Б3, А4-Б4. После забора ионов из банок А3-Б3 и А4- Б4 тщательно протирайте электроды-пластины марлевым тампоном, смоченным дистиллированной водой. Для надежности можно их поместить в дистиллированную воду и поменять полюса электродов (как известно, одноименные заряды отталкиваются друг друга).
Запишите полученные данные на 2-3 секундах, так как вначале разность потенциалов быстро убывает вследствие нейтрализации ионов электролитов разноименными ионами воздуха. Затем разность потенциалов по той же причине убывает, но уже медленно. Вылейте жидкость из всех банок, ополосните их сначала водопроводной водой, затем дистиллированной.
Рекомендации по оформлению протокола работы. Внесите в тетрадь протоколов опытов показатели разности электрических потенциалов между каждой парой банок А и Б после забора из них ионов по схеме 3.
Схема 3. А1- Б1 = мВ; А2-Б2 = мВ; А3- Б3 = мВ; А4- Б4 = мВ (она повторяет схему 1, но после забора ионов из банок).
Делая выводы, подумайте:
1. Обнаружили ли вы разность электрических потенциалов в контрольном исследовании? Почему?
2. Что является непосредственной причиной формирования потенциала покоя?
Лабораторная работа № 2
