Другие вирусные гастроэнтериты и диареи 5 страница
Суточная доза глюкокортикостероидов — не менее 180—240 мг преднизо-лона или других препаратов в эквивалентных дозах, которые вводят парентерально. Инфузионную терапию осуществляют с применением концентрированных глюкозокалиевых растворов с инсулином, альбумина, аминокислотных смесей, протеина при строгом соблюдении суточного баланса жидкости. Важным элементом инфузионной терапии является свежезамороженная плазма, которую следует применять при сниженном протромбиновом индексе (менее 50%). При желудочно-кишечных кровотечениях и других проявлениях геморрагического синдрома назначают ингибиторы протеаз и фибринолиза (5% раствор эпсилон-аминокапроновой кислоты по 200 мл 2 раза в сутки, контрикал по 100—200 тыс. ЕД через каждые 3—4 ч).
Для устранения гипоксии и отека-набухания головного мозга проводят постоянную ингаляцию увлажненного кислорода через носовые катетеры со скоростью 5 л/мин. Показана оксигенобаротерапия, которая в случаях раннего применения (по 2—3 сеанса в сутки) может предупредить развитие комы. Использование средств коррекции КОС и электролитного баланса осуществляется под соответствующим контролем. Из специальных методов лечения могут быть использованы различные варианты экстракорпоральной детоксикации с учетом коагулопатии, операция замещения крови.
Прогноз.У подавляющего большинства больных (65—80%) ГВ заканчивается выздоровлением. У 10-12% заболевание приобретает хроническое течение (см. цв. вклейку, рис. 18). У 12—15% реконвалесцентов сохраняются астс-но-вегетативный синдром, дискинезия желчевыводящих путей, хронический холецистохолангит, гепатомегалия без нарушения функции печени. «Здоровое» хроническое носительство HBsAg формируется у 4—6% реконвалесцентов. Частота летальных исходов ГВ составляет 0,5—2%.
Правила выписки.Реконвалесценты могут быть выписаны из стационара при отсутствии жалоб, уменьшении печени до нормальных размеров, нормализации уровня билирубина в крови, при отрицательных реакциях мочи на уробилин и желчные пигменты. Допускается выписка при небольшом увеличении активности аминотрансфераз (в 2—3 раза) и при увеличении вертикального размера печени на 1—2 см.
Диспансеризация.Первый контрольный осмотр после выписки проводится через 15—30 дней в стационаре, где больной находился на излечении. Реконвалесценты, у которых субъективных и объективных отклонений не обнаружено, в дальнейшем обследуются в поликлинике через 3, 6,12 мес. В течение 6 мес. противопоказаны профилактические прививки, кроме противодифтерийного и противостолбнячного анатоксинов и антирабической вакцины. Запрещается алкоголь. Женщинам рекомендуется избегать беременности в течение года после выписки. При ухудшении состояния здоровья больной направляется в стационар для продолжения лечения.
Реабилитация военнослужащих, перенесших ГВ, осуществляется в реабилитационных отделениях военных госпиталей: после легкой формы заболевания в течение 21 дня, после среднетяжелой формы — 30 дней.
Профилактика и мероприятия в очаге.Мероприятия по профилактике должны быть ориентированы на активное выявление источников инфекции и разрыв естественных и искусственных путей заражения, а также проведение вакцинопрофилактики в группах риска.
В первую очередь вакцинации подлежат контингента, относящиеся к группам высокого риска заражения гепатитом В: медицинские работники; студенты медицинских учреждений; больные, получающие повторные гемотрансфузии или находящиеся на гемодиализе; семейное окружение больных хроническим ГВ; наркоманы. При достаточном количестве вакцины прививки против ГВ можно проводить всем группам населения. Схема иммунизации взрослых состоит из трех прививок: две первые с интервалом в 1 мес, третья через 6 мес. Ревакцинация проводится через 7 лет.
Среди подлежащих вакцинации групп населения будет некоторое число лиц, имеющих HBsAg или антитела к вирусу ГВ в результате перенесенной инфекции. Эти две категории не нуждаются в вакцинации, однако она не наносит им вреда. Вакцинация не отягощает течение хронического ГВ. У лиц, перенесших ГВ и имеющих антитела к данному вирусу, вакцинация может оказать лишь бустерный эффект.
У детей вакцинопрофилактика проводится поэтапно. В первую очередь иммунизации подлежат: новорожденные, родившиеся у матерей, имеющих HBsAg и больных ГВ в третьем триместре беременности (вакцинацию таких детей проводят четырехкратно: первые три прививки с интервалом в один месяц, при этом первое введение вакцины осуществляется в первые 24 ч жизни, а четвертое введение препарата проводят в возрасте 12 мес); все новорожденные, родившиеся в регионах с распространенностью «носительства» HBsAg выше 5%; дети, в семьях которых есть «носитель» HBsAg или больной хроническим ГВ; дети домов ребенка и интернатов; дети, регулярно получающие кровь и ее препараты, а также находящиеся на гемодиализе. Второй этап вакцинации предусматривает охват всех детей в рамках календаря прививок. На третьем этапе, учитывая рост заболеваемости ГВ среди подростков, следует вакцинировать против ГВ детей в возрасте 11 лет.
Защитный уровень антител в крови достигается после полного курса иммунизации у 85—95% вакцинированных. После двух прививок антитела образуются лишь у 50—60% вакцинированных.
Иммунопрофилактика по экстренным показаниям проводится у тех людей, у кого произошел контакт с возбудителем, при этом ее эффективность повышается при одновременном введении вакцины и специфического иммуноглобулина, содержащего антитела к вирусу ГВ.
Врачебная экспертиза.Реконвалесценты ГВ после выписки из стационара нетрудоспособны не менее 30 дней, а затем вопрос трудоспособности определяется в зависимости от клинико-биохимических показателей.
Военнослужащим, перенесшим ГВ в тяжелой форме, представляется отпуск по болезни на 30 сут.
ГЕПАТИТ С (ГС)
ГС — заболевание, сходное по эпидемиологическим признакам с ГВ, однако протекающее более легко и отличающееся при желтушных формах сравнительно быстрым обратным развитием болезни. Чаще встречаются безжелтушные, субклинические и инаппарантные формы ГС, которые переносятся без стационарного лечения, однако в 80—90% случаев переходят в хронический гепатит и у 20—30% больных — в цирроз печени.
Этиология.Вирус ГС (ВГС, HCV) относится у семейству флавивирусов (Flaviviridae), содержит РНК, покрыт липидорастворимой оболочкой и имеет размеры в диаметре около 50 нм. Геном HCV кодирует структурные (С, Е1, E2/NS1) и неструктурные (NS2, NS3, NS4, NS5) белки. К структурным белкам относятся: сердцевинный (С — ядерный, core protein) и два гликопротеина оболочки (El, Е2— envelope protein); соответственно, к четырем неструктурным белкам — ферменты, играющие роль в репликации вируса (в частности, NS3—про-теаза/геликаза, NS5—РНК-полимераза). К каждому из этих белков вырабатываются антитела, циркулирующие в крови. Вариабельность их соотношения определяет наличие ряда серотипов. Они не обладают вируснейтрализующими свойствами, особенно у лиц с хроническим течением ГС.
Важной особенностью возбудителя ГС является его генетическая неоднородность. Выделяют, по меньшей мере, шесть генотипов вируса (1—6), которые, в свою очередь, подразделяются на субтипы. В настоящее время описано более 50 субтипов ВГС, обозначаемых буквами. Считается, что для целей клинической практики необходимо различать следующие генотипы HCV: la, lb, 2а, 2b и За. На территории России преобладают lb и За генотипы.
Сведения о чувствительности ВГС к внешним физико-химическим воздействиям весьма малочисленны. Известно, что вирус устойчив к нагреванию до 50° С, но инактивируется растворителями липидов (хлороформ) и ультрафиолетовым облучением. Во внешней среде возбудитель нестоек, однако степень его устойчивости к инактивации выше, чем вируса иммунодефицита человека.
Эпидемиология.Распространенность ГС во многом совпадает с ГВ. что находит объяснение в общности многих черт эпидемиологии этих инфекций. К особенностям распределения ГС можно отнести меньшее различие в инфицированноcти между развивающимися и высокоразвитыми странами. Гиперэндемичные зоны по заболеваемости ГС, в сравнении с ГВ, не столь очерчены в связи с широким распространением наркомании как в развивающихся, так и развитых странах.
Источниками ГС являются больные острой и хронической формами инфекции. Учитывая преобладание бессимптомных форм ГС, наибольшую эпидемическую опасность представляют больные скрыто протекающим гепатитом, особенно с наличием РНК HCV в крови.
Механизм передачи возбудителя контактный. При этом заражающая доза для ВГС в несколько раз больше, чем для ВГВ. В отличие от возбудителя ГВ естественные пути распространения вируса ГС имеют меньшее значение: риск инфицирования в быту, при половых контактах и при рождении ребенка от инфицированной матери относительно низок. ГС с полным основанием можно назвать «гепатитом наркоманов». Каждый второй пациент с HCV-ин-фекцией относится к лицам, вводившим внутривенно наркотические средства. Заражение также происходит при гемотрансфузиях, парентеральных вмешательствах.
В связи с вариабельностью генома HCV у лиц, перенесших инфекционный процесс, не вырабатывается специфическая невосприимчивость к повторным заражениям. Возможно множественное инфицирование различными генотипами и субтипами возбудителя.
Патогенез и патологическая анатомия.Доминирующая роль биологических свойств HCV по сравнению с иммунным ответом — это главное отличие патогенеза ГС от ГВ. Непременным условием развития инфекции является проникновение вируса в гепатоциты, где и происходит его репликация. Следует отметить, что при ГС не происходит интеграции патогена с геномом печеночных клеток, так как жизненный цикл вируса не включает промежуточной ДНК, а следовательно, интегративные формы не регистрируются. Принято считать, что ВГС, в отличие от ВГВ, обладает прямым цитопатическим действием. Однако быстрой санации гепатоцитов от возбудителя не происходит, что обусловлено слабой его иммуногенностью. При этом главным механизмом «ускользания» вируса из-под иммунного надзора является высокая изменчивость возбудителя, которая реализуется прежде всего путем непрерывного обновления его антигенной структуры, к чему не успевает приспосабливаться иммунная система. Такое сосуществование у одного больного множества постоянно изменяющихся антигенных вариантов HCV получило наименование «quasispecies». В результате сохраняются гипервариабельные штаммы, они становятся преобладающими и поддерживают активную репликацию. Причем скорость мутаций превышает скорость репликации, что и формирует присущую ГС многолетнюю персистенцию инфекции. Необходимо отметить, что максимальная изменчивость происходит в антигенах оболочки, которые кодируются участками El, E2/NS1 генома HCV и являются основной мишенью иммунной атаки.
Также установлено, что ВГС обладает способностью индуцировать пептиды, которые являются функциональными антагонистами Т-лимфоцитарных рецепторов. Вызываемая «Т-клеточная анергия» в значительной степени блокирует хелперную и цитотоксическую активность, что способствует хронизации инфекционного процесса. Возможно, в подавлении клеточного звена иммунного ответа определенная роль принадлежит апоптозу вирусспецифических Т-клеток. Гуморальный иммунный ответ при ГС также выражен слабее, чем при ГВ, вследствие менее интенсивного антителообразования. К тому же, анти-HCV практически лишены вируснейтрализующих свойств. В последнее время стало известно, что у реконвалесцентов острого ГС преобладает продукция цитокинов Т-хелперами 1-го типа (интерлейкин-2, гамма-интерферон), которые активируют клеточное звено иммунной системы. В свою очередь, при хронизации ГС превалируют цитокины, вырабатываемые Т-хелперами 2-го типа (интерлейкин-4, -5, -10), активирующие гуморальный иммунитет.
Патоморфологические изменения в печени зависят, в основном, от стадии процесса. При остром ГС у 1/5 части больных обнаруживают признаки слабовыраженных ступенчатых некрозов. По мере прогрессирования болезни происходит увеличение выраженности лимфоидной инфильтрации перипортальной соединительной ткани и развитие фиброза.
Симптомы и течение.Инкубационный период продолжается от 20 до 150, в среднем — 40—50 дней. Острый ГС, как правило, остается нераспознанным, так как патологический процесс обычно протекает латентно (субклинические, инаппарантные формы). Он может быть диагностирован лишь по повышению активности АлАТ, положительным результатам исследований на РНК HCV, несколько реже анти-HCV IgM, IgG и при отсутствии антител к неструктурному белку NS4, 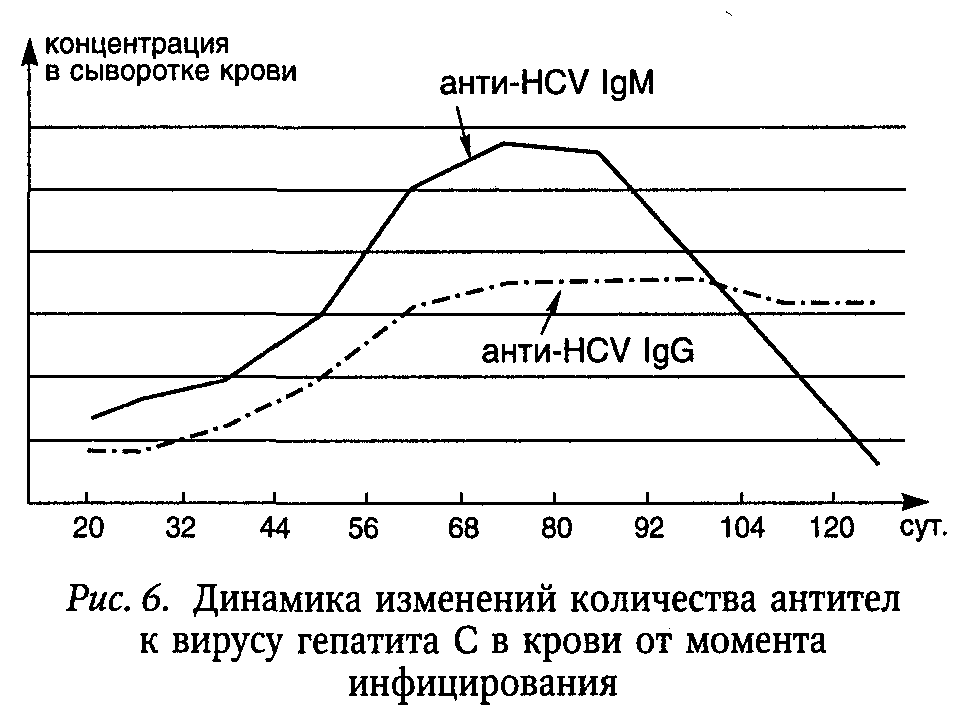 которые обычно появляются значительно позже, когда патологический процесс переходит в хроническую форму.
которые обычно появляются значительно позже, когда патологический процесс переходит в хроническую форму.
Для безжелтушных и начального периода желтушных (встречаются гораздо реже) форм ГС характерны астеновегетативный и диспепсический синдромы. Клиническая симптоматика скудная. Больные отмечают слабость, вялость, быструю утомляемость, ухудшение аппетита, иногда ощущение тяжести в правом подреберье. Жалобы большей частью выражены нерезко. В желтушном периоде признаки общей интоксикации незначительны. Проявления желтухи, как правило, минимальны (субиктеричность склер и слизистых неба, легкое окрашивание кожи, транзиторные холурия и ахолия), может быть выявлено слабо выраженное увеличение печени. Клинически манифестный острый ГС протекает преимущественно (в 75—85% случаев) в легкой, реже - в среднетяжелой форме. Острая печеночная недостаточность (энцефалопатия) развивается крайне редко.
Диагноз и дифференциальный диагноз.Для ГС эпидпредпосылки тс же, что и при ГВ, с акцентом на парентеральную передачу. Острый гепатит большей частью протекает бессимптомно, с очень высокой вероятностью хронизации. Основным подтверждением диагноза является обнаружение в крови РНК HCV (методом ПЦР), несколько реже — анти-HCV IgM и IgG (рис. 6). Исключение хронического ГС осуществляется на основании выявления минимальных изменений в гепатобиоптатах, отсутствия фиброза и aнти-NS4 в крови.
Лечение.Принципы лечения такие же, как при ГА и ГВ, с той лишь разницей, что противовирусную терапию целесообразно назначать во всех случаях острого ГС, учитывая крайне высокую вероятность хронизации. При этом процент хронизации уменьшается приблизительно в 3 раза.
Прогноз.В целом, в 85—90% случаев острой HCV-инфекции наступает хронизация и в 10—15% — выздоровление.
Правила выписки, диспансерное наблюдение и врачебная экспертизаосуществляются, как при ГВ.
Профилактика и мероприятия в очагетакие же, как при ГВ. До настоящего времени вакцина не разработана.
ГЕПАТИТ D (TD)
Этиология.ГО вызывается РНК-содержащими вирусами генотипов I, II, III. В России, как и во всем мире, преобладает I генотип.
Возбудитель (ВГО, HDV) способен к репликации только в присутствии вируса ГВ, встраиваясь в его внешнюю оболочку. Таким образом, полноценный вирус ГО состоит из РНК, внутреннего антигена (HDAg) — собственно ВГГЗ — и его внешней оболочки, состоящей из HBsAg. Поэтому ГО встречается только у лиц, инфицированных возбудителем ГВ. В структуре HDV нет собственной полимеразы, и ее функции, как полагают, компенсирует клеточная полимераза.
ВГО термоустойчив, инфекционная активность его при ультрафиолетовом облучении не утрачивается.
Заражение может произойти одновременно обоими возбудителями с развитием HBV/HDV-коинфекции (микст-гепатит B+D) или в случаях инфицирования возбудителем ГО лиц с HBV-инфекцией с возникновением HDV/ HBV-cyперинфекции (ГО).
Эпидемиология.Распространение ГО неравномерно в различных регионах и коррелирует с уровнем выявления HBsAg. Считают, что HDV-инфекция на разных территориях регистрируется с частотой от 0,1% до 20—30% к общему числу случаев HBV-инфекции. Источники инфекции общие, механизм передачи возбудителя ГО аналогичен таковому при ГВ, но инфицирующая доза существенно меньше. Пути передачи ВГО совпадают с путями передачи ВГВ, однако при HDV-инфекции наблюдается меньшая частота перинатального пути передачи от инфицированных матерей. Это определяет относительно меньшую заболеваемость ГО среди детей.
Патогенез и патологическая анатомия.Основной особенностью патогенеза HDV-инфекции является ведущая роль HDV по сравнению с HBV. При этом активная репликация HDV чаще приводит к подавлению репродукции HBV. Разной является и характеристика повреждающего действия. При ГD, в отличие от ГВ, допускают прямое цитопатическое действие вируса. Это подтверждается более ранним появлением цитолитического синдрома и более коротким инкубационным периодом, близким по продолжительности к ГА. Однако значимость иммунного ответа также важна в связи с широким диапазоном вариантов течения HDV-инфекции — от латентных форм до клинически манифестных, в том числе крайне тяжелых. Необходимо отметить, что каких-либо патоморфологических различий при клинически близких формах ГВ и ГD не отмечено.
Симптомы и течение.Острый гепатит чаще всего развивается при HBV/HDV-коинфекции. Инкубационный период при этом составляет 20— 40 дней. По сравнению с острым ГВ заболевание отличается более высокой и более длительной лихорадочной реакцией, более частым появлением полиморфной сыпи, суставных болей, увеличением селезенки, двухволновым течением болезни.
Несколько чаще наблюдаются и фульминантные формы. В крови выявляют маркеры острой фазы: анти-НВс IgM и анти-HDV IgM. Для микст-гепатита B+D в основном характерна циклическая среднетяжелая форма, завершающаяся выздоровлением. Прогредиентное течение наблюдается у немногих больных. Соответственно, угроза хронизации возникает примерно с той же частотой, что и при остром ГВ.
При HDV/HBV-суперинфекции клинически манифестный острый гепатит наблюдается намного реже, чем при коинфекции. Однако если данная форма имеет место, то часто отмечаются тяжелые и фульминантные формы заболевания с резко выраженными симптомами интоксикации, геморрагическим и, нередко, отечно-асцитическим синдромами, болями в области правого подреберья, с повторными волнами обострения, иногда превышающими по тяжести первую. В части случаев происходит лишь повышение активности аминотранс-фераз без клинических проявлений. Диагноз устанавливается только при обнаружении в сыворотке крови соответствующих маркеров гепатитов В и D (HBsAg в сочетании с анти-HDV IgM и/или РНК HDV).
Диагноз и дифференциальный диагноз.Острый гепатит при HDV-инфекции подтверждается выявлением в крови анти-HDV IgM, РНК HDV наряду с HBsAg. Отсутствие в данном случае анти-НВс IgM, HBeAg (и, наоборот, наличие анти-НВс IgG, анти-НВе) свидетельствует об HDV/HBV-суперинфекции. Напротив, присутствие анти-НВс IgM и HBeAg характерно для HDV/HBV-ko-инфекции. HDAg в сыворотке крови обнаруживается редко, анти-HDV IgG появляются позже. Дифференциальный диагноз проводится по аналогии с ГА и ГВ.
Лечение.При ГО применяется такой же комплекс лечебных мероприятий, как при ГА и ГВ.
Прогноз.Исходы острой коинфекции аналогичны таковым при остром ГВ. При острой суперинфекции вероятность хронизации очень высокая (в связи с наличием уже предшествующего хронического ГВ), а летальность может достигать 20%.
Правила выписки, диспансерное наблюдение и врачебная экспертизаосуществляются, как при ГВ.
Профилактика и мероприятия в очагетакие же, как при ГВ. Вакцинация против ГВ эффективна и в отношении ограничения распространения дельта-инфекции.
ГЕПАТИТ Е (ГЕ)
Этиология.Вирус гепатита Е (ВГЕ, HEV) относится к РНК-содержащим калициподобным вирусам, диаметром 32—34 нм. По сравнению с ВГА он менее устойчив к термическим и химическим воздействиям.
Эпидемиология.ГЕ, как и ГА, также характеризуется фекально-оральным механизмом передачи возбудителя, распространен в регионах преимущественно тропического и субтропического пояса у лиц молодого возраста. Эпидемиологическими особенностями ГЕ являются резко выраженная неравномерность территориального распространения заболевания; взрывообразный характер вспышек с высоким уровнем заболеваемости в районах с неудовлетворительным водоснабжением (доминирующая роль водного пути передачи); наиболее частое поражение лиц в возрасте 15—30 лет, преимущественно мужчин; осенне-зимняя сезонность.
Патогенез и патологическая анатомия.Факторы патогенеза ГЕ в значительной мере те же, что и ГА. ВГЕ обладает цитопатическим эффектом. В поражении печеночной клетки иммунопатологические клеточные механизмы существенной роли не играют.
Специфическим маркером ГЕ служит обнаружение в сыворотке крови антител класса IgM. Дополнительное значение имеет индикация антигена вируса в фекалиях. После перенесенного ГЕ формируется достаточно устойчивый иммунитет (анти-HEV IgG), однако, в отличие от ГА, он не пожизненный. Хронические формы заболевания и вирусоносительство не зарегистрированы.
Симптомы и течение.Инкубационный период составляет от 20 до 65 дней, чаще около 35 суток. В клинической картине преобладают признаки, характерные для ГА. Однако в начальном периоде лихорадочная реакция не выражена. Чаще беспокоят общая слабость, отсутствие аппетита, тошнота, ноющие боли в правом подреберье и эпигастрии. Продолжительность начального периода составляет 5—6 дней. С появлением желтухи синдром общей интоксикации не уменьшается, что отличает ГЕ от ГА. В неосложненных случаях желтушный период длится 2—3 нед.
Особого внимания заслуживает ГЕ у женщин во второй половине беременности. Заболевание у них в 20—25% случаев может приобретать злокачественное течение по фульминантному типу с быстрым развитием массивного некроза печени и острой печеночной энцефалопатии. При этом нередко возникает ДВС-синдром и характерен усиленный гемолиз, сопровождающийся гемоглобинурией, приводящей к острой почечной недостаточности. Тяжелое течение ГЕ часто сопровождается самопроизвольным прерыванием беременности, которое, как правило, сопровождается резким ухудшением состояния больных. Необходимо отметить, что даже при доношенной беременности из детей, родившихся живыми, более половины умирает в течение первого месяца жизни.
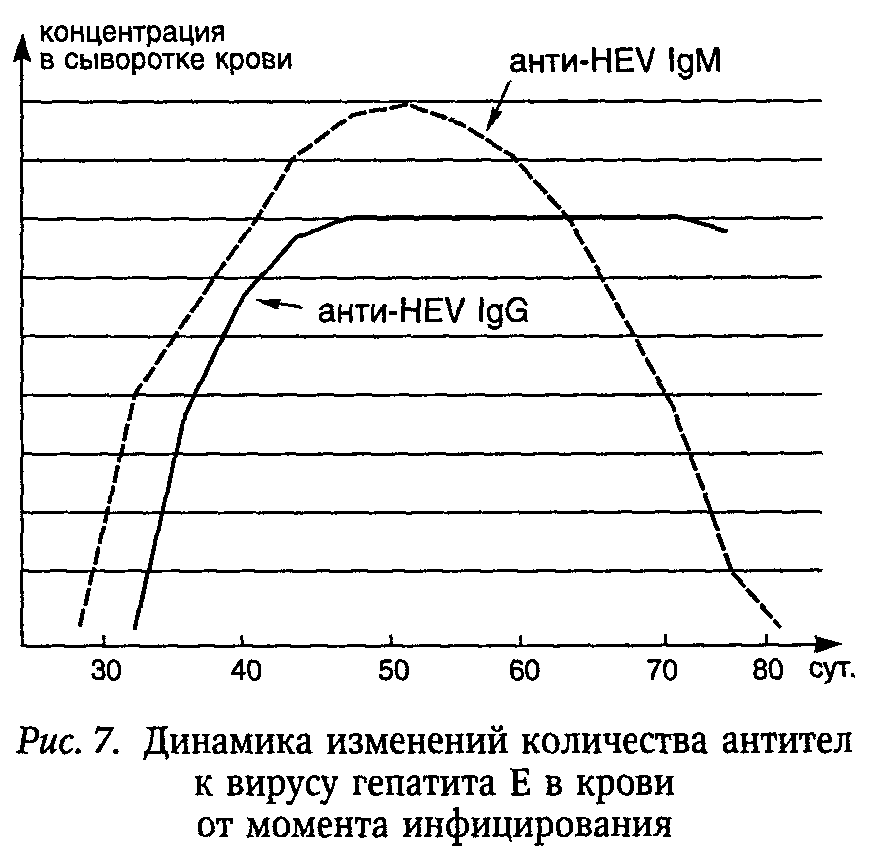
Диагноз и дифференциальный диагноз.Опорными диагностическими признаками ГЕ являются предположение о водном механизме передачи, возраст от 20 до 40 лет, распространение в регионах преимущественно тропического и субтропического пояса, клинические проявления, подобно ГА, с преобладанием легких форм, регистрация тяжелых форм с угрозой летального исхода у беременных женщин во второй половине беременности, реже в раннем послеродовом периоде и у кормящих матерей (протекают с интенсивным гемолизом, гемоглобинурией, острой почечной недостаточностью и тяжелым тромбогеморрагическим синдромом). Подтверждает диагноз выявление анти-HEV IgM (анти-HEV IgG появляются гораздо позже и свидетельствуют о перенесенном заболевании) (рис. 7). Дифференциальный диагноз проводится, как при ГА.
Лечение.При ГЕ применяется такой же комплекс лечебных мероприятий, как и при ГА.
Прогноз.Исходы ГЕ также подобны таковым при ГА, за исключением большей частоты летальности у беременных женщин.
Правила выписки, диспансерное наблюдение и врачебная экспертизаосуществляются, как при ГА.
Профилактика и мероприятия в очаге.Профилактические и противоэпидемические мероприятия гигиенической направленности, в первую очередь существенное улучшение водоснабжения населения, проводимые для снижения заболеваемости ГА, эффективны и в отношении ГЕ. На данный момент вакцина не разработана.
МИКСТ-ГЕПАТИТЫ
Гемоконтактные микст-гепатиты с наибольшей частотой регистрируются у лиц, использующих внутривенное введение наркотиков. Это отчасти объясняет тот факт, что микст-инфекция преимущественно наблюдается у пациентов молодого возраста. В первую очередь это касается сочетания ГВ и ГС. Клинико-лабораторные и эпидемиологические данные у большей части больных свидетельствуют о наслоении ГВ на предшествующий ГС (острый ГВ на фоне хронического ГС) или о сочетанном заражении. В последнем случае клинические проявления в основном соответствуют моноинфекции ГВ. Частота хронизации при остром микст-гепатите В+С и остром ГС приблизительно одинаковая.
Необходимо отметить, что более чем в половине случаев при микст-гепатитах В+С в клинической практике приходится иметь дело уже с обострениями хронического гепатита смешанной этиологии, особенностью которого является преобладание активности ВГС, которая определяет характер течения инфекции. У небольшой части больных могут выявляться и маркеры HDV-инфекции. Такой «тройной» микст-гепатит в острую фазу рассматривают как потенциально тяжелое заболевание, которое также обусловливает частую хрониза-цию. Назначение противовирусной терапии гемокоптактных микст-гепатитов зависит от наличия репликативной активности того или иного возбудителя.
Микст-инфекция ГА. В последние годы отмечается снижение уровня заболеваемости моноинфекцией ГА и одновременный рост микст-инфекции ГА (ГА + ГВ, ГА + ГС и ГА + ГВ + ГС). Данное обстоятельство заставляет по-другому взглянуть на клинику и течение микст-инфекции ГА. Результаты наших исследований свидетельствуют, что почти во всех случаях ГА протекает на фоне хронического ГВ или ГС. При этом микст-гепатит отличается от моноинфекции смешанным вариантом преджелтушного периода примерно в 75% случаев, большей частотой среднетяжелых форм, развитием холестатического синдрома, тенденцией к затяжному течению, длительным выздоровлением с сохраняющимся после выписки слабо выраженным цитолизом в 60—65%. В этой связи, выявление ГА-микст требует обязательного определения маркеров активности репликации ВГВ (HBeAg, анти-НВс IgM, ДНК HBV) и ВГС (РНК HCV) для решения вопроса о необходимости этиотропной противовирусной терапии. Сочетание острого ГА и острых парентеральных гепатитов (В, С, D) отмечается крайне редко.
ГЕМОРРАГИЧЕСКИЕ ЛИХОРАДКИ
Группа геморрагических лихорадок включает острые лихорадочные заболевания вирусной этиологии, в патогенезе и клинических проявлениях ведущую роль играет поражение сосудов, приводящие к развитию тромбогеморрагического синдрома. В изучении геморрагических лихорадок ведущую роль играли отечественные ученые. Впервые в качестве самостоятельной нозологической формы геморрагическую лихорадку (под названием «геморрагический нефрозонефрит») описал в 1941 г. А. В. Чурилов, который наблюдал это заболевание на Дальнем Востоке в период 1935—1939 гг. После защиты докторской диссертации он работал на кафедре инфекционных болезней Военно-медицинской академии. Патоморфология болезни была изучена В. Г. Чудаковым (профессор кафедры патологической анатомии Военно-медицинской академии). Вирусную этиологию заболевания обосновал академик А. А. Смородинцев, хотя ему и не удалось получить культуру вируса. В настоящее время эту болезнь называют геморрагической лихорадкой с почечным синдромом.
В 1944—1945 гг. на основании изучения крупной эпидемической вспышки в Крыму М. П. Чумаков с соавторами выделили как самостоятельную нозологическую форму крымскую геморрагическую лихорадку, позднее подобное заболевание наблюдалось в Конго, и болезнь получила название геморрагическая лихорадка Крым-Конго. В 1946 г. выявлена новая геморрагическая лихорадка, названная омской геморрагической лихорадкой (Р. Н. Ахрем-Ахремович, А. Ф. Билибин, М. П. Чумаков).
В последующие годы был описан целый ряд геморрагических лихорадок в различных регионах, в частности группа африканских лихорадок, включающих лихорадки Ласса, Эбола, Марбург. В Южной Америке — лихорадки аргентинская и боливийская. Для Юго-Восточной Азии характерны Киасанурская лесная болезнь, лихорадка чикунгунья, в группу геморрагических лихорадок включены болезни, которые описаны раньше (желтая лихорадка, денге).
Геморрагические лихорадки относятся к зоонозам с природной очаговостью. По путям передачи выделяют клещевые, геморрагические лихорадки (геморрагическая лихорадка Крым-Конго, омская геморрагическая лихорадка, Киасанурская лесная болезнь), комариные геморрагические лихорадки (желтая лихорадка, денге, лихорадка чикунгунья) и группа контагиозных зоонозов (аргентинская геморрагическая лихорадка, боливийская геморрагическая лихорадка, геморрагическая лихорадка с почечным синдромом, лихорадки Ласса, Марбург). Многие геморрагические лихорадки протекают тяжело (желтая лихорадка, лихорадки Ласса, Марбург, Эбола), желтая лихорадка относится к карантинным инфекциям. При диагностике необходимо учитывать пребывание в эндемичных природных очагах, а также возможность завоза тропических геморрагических лихорадок.
