Инфаркт миокарда и его проявления
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ ТУЛЬСКОЙ ОБЛАСТИ
ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
СРЕДНЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«Тульский областной медицинский колледж»
Белевский филиал
КУРСОВАЯ РАБОТА
Уровень образования: базовый
Специальность: Сестринское дело
Квалификация: Медицинская сестра
Роль медицинской сестры
При оказании помощи пациентам при инфаркте миокарда
Выполнила:
Студентка группы мс А 9 III Б
Асеева Татьяна Павловна.
Белев, 2015.
Содержание
ВВЕДЕНИЕ
Глава 1. Теоретическая часть
1. Инфаркт миокарда и его проявления
1.1 Характер и классификация инфаркта миокарда
1.2 Этиология инфаркта миокарда
1.3 Клиническая картина инфаркта миокарда
2. Лечение, диагностика, профилактика инфаркта миокарда
2.1 Диагностика инфаркта миокарда
2.2 Лечение инфаркта миокарда
2.3 Профилактика инфаркта миокарда
Глава 2. Практическая часть
ЛЕЧЕБНАЯ ФИЗИЧЕСКАЯ КУЛЬТУРА
ВЫВОДЫ И ЗАКЛЮЧЕНИЕ
СПИСОК ЛИТЕРАТУРЫ
ПРИЛОЖЕНИЕ
Введение
Ишемическая болезнь сердца (ИБС) – одно из основных заболеваний человека, значительно ухудшающее качество жизни и приводящее к летальному исходу. Статистические исследования свидетельствуют о том, что более 50% населения в возрасте от 65 лет страдают сердечно - сосудистыми заболеваниями. В России, по данным разных авторов, ежегодно ишемическая болезнь сердца диагностируется у 2,8-5,8 млн. человек, смертность же составляет до 30% общей.
Острый инфаркт миокарда (ОИМ) – заболевание, которое может закончиться выздоровлением больного без вмешательства врачей, и наоборот, привести к смерти, несмотря на все их усилия. Однако между этими крайностями находится многочисленная группа больных, судьба которых зависит от своевременного вмешательства врача и использования современных методов лечения.
Самой опасной является ранняя фаза заболевания – первые часы, когда высок риск остановки сердца. Своевременная и адекватная медицинская помощь при ОИМ заключается в максимально раннем проведении процедуры тромболизиса, оптимально в течение первого часа от возникновения симптомов. Госпитализация пациента должна осуществляться в кардиореанимационное отделение, обладающее возможностью проведения ангиопластики и стентирования коронарных артерий. Чем раньше будет восстановлен кровоток в сосуде, тем больше шансов на благоприятный исход. Между тем, если симптомы заболевания нетяжелы или нетипичны, может пройти несколько часов, пока пациент обратится за помощью.
Заболеваемость населения болезнями системы кровообращения в 2011 году составила в целом по России 32 490 372 случаев (против 29 812 599 в 2006 году), при этом, например, повышенным кровяным давлением страдают 12 045 777 в 2011 году (против 10 146 174 в 2006 году). Год от года растет число болеющих врожденными аномалиями системы кровообращения: на 100 000 населения в 2011 году это в среднем 294,3 пациента (в 2010-м — 285,1; в 2006-м — 237,5).
А вот число случаев инфаркта миокарда в целом по РФ сократилось – всего 152 022 в 2011 году против 162 581 в 2006 году и 187 126 в 2009 году![1]
При этом в некоторых регионах коэффициент заболеваемости инфарктом миокарда на 100 000 населения все-таки вырос в сравнении с предыдущим годом.
Актуальность темы - заключается в том, что инфаркт миокарда — одна из клинических форм ишемической болезни сердца, характеризующаяся развитием локального некроза миокарда вследствие остро возникшего несоответствия коронарного кровотока потребностям миокарда.
Инфаркт миокарда является одним из наиболее частых проявлений ишемической болезни сердца и одной из наиболее частых причин смерти.
Это распространенное заболевание является одной из основных причин смертности, а так же временной и стойкой утраты трудоспособности населения в развитых странах мира. В связи с этим проблема ИБС занимает одно из ведущих мест среди важнейших медицинских проблем настоящего времени.
Цель исследования– максимально полно изучить теоретические основы острого инфаркта миокарда, роль медицинской сестры в лечении этого заболевания.
Для решения данной цели определен ряд задач:
1. Изучить теоретический материал по инфаркту миокарда.
2. Изучить клинические проявления острого инфаркта миокарда.
3. Изучить диагностические базы инфаркта миокарда
4. Изучить элементы сестринского ухода за больными страдающими инфарктом миокарда.
Предмет исследования - острый инфаркт миокарда, как самостоятельная нозологическая единица.
Объект исследования - больные, страдающие острым инфарктом миокарда.
Гипотеза- при подробном рассмотрении данной темы мы сможем узнать больше о заболевании, причинах его возникновения, своевременном лечении, правильном уходе за пациентом.
ГЛАВА 1. Теоретическая часть
Инфаркт миокарда и его проявления
1.1 ХАРАКТЕРИСТИКА И КЛАССИФИКАЦИЯ ИНФАРКТА МИОКАРДА
Инфаркт миокарда — это острое заболевание сердца, обусловленное развитием очагов омертвения в сердечной мышце вследствие резкого снижения кровотока по сосудам сердца и проявляющееся нарушением сердечной деятельности. Основу болезни составляет атеросклеротическое сужение коронарных артерий, питающих сердечную мышцу. Часто к этому процессу присоединяется закупорка сосудов в зоне поражения тромбами, в результате чего полностью или частично прекращается поступление крови к соответствующему участку мышцы сердца. Часто инфаркт миокарда развивается на фоне учащения приступов стенокардии, при которой резкое физическое или психическое перенапряжение может стать непосредственной причиной инфаркта миокарда.
В зависимости от симптомов инфаркта миокарда, различают следующие классификации.
По стадиям развития:
1. Продромальный период (0-18 дней)- характеризуется появлением впервые или учащением и усилением привычных ангинозных болей, изменением их характера, локализации или иррадиации, а также изменением реакции на нитроглицерин. В этом периоде заболевания могут отмечаться динамические изменения ЭКГ, свидетельствующие об ишемии или повреждении сердечной мышцы
2. Острейший период (до 2 часов от начала ИМ) длится от начала болевого синдрома до появления признаков некроза сердечной мышцы на ЭКГ. АД в это время неустойчиво, чаще на фоне болей отмечается АГ, реже — снижение АД вплоть до шока. В острейшем периоде наиболее высокая вероятность фибрилляции желудочков. По основным клиническим проявлениям заболевания в этом периоде различают следующие варианты начала болезни: болевой (ангинозный), аритмический, цереброваскулярный, астматический, абдоминальный, малосимптомный (безболевой).
3. Острый период (до 10 дней от начала ИМ) В это время формируется очаг некроза, происходит резорбция некротических масс, асептическое воспаление в окружающих тканях и начинается формирование рубца. С окончанием некротизации боль стихает и если возникает вновь, то лишь в случаях рецидива инфаркта миокарда или ранней постинфарктной стенокардии.
4. Подострый период (с 10 дня до 4-8 недель) Происходит организация рубца. Исчезают проявления резорбционно-некротического синдрома. Симптоматика зависит от степени выключения из сократительной функции поврежденного миокарда (признаки сердечной недостаточности и др.).
5. Период рубцевания (с 4-8 недель до 6 месяцев) период, когда окончательно формируется и уплотняется рубец, а сердце привыкает к новым условиям работы.[2]
По анатомии и объему поражения:
I. Крупноочаговый инфаркт, трансмуральный (некроз, захватывающий все слои миокарда), Q-инфаркт.
II. Мелкоочаговый инфаркт (не Q-инфаркт).Выделяют два типа мелкоочагового инфаркта:
- Интрамуральный- омертвление стенки миокарда, но при этом эндокард и эпикард не повреждены.
- Субэндокардиальный- некроз участков сердца, прилегающих к эндокарду.
Локализация очага некроза.
1. Инфаркт миокарда левого желудочка (передний, боковой, нижний, задний).
2. Изолированный инфаркт миокарда верхушки сердца.
3. Инфаркт миокарда межжелудочковой перегородки (септальный).
4. Инфаркт миокарда правого желудочка.
5. Сочетанные локализации: задне-нижний, передне-боковой и др.
По течению:
1. Моноциклическое
2. Затяжное
3. Рецидивирующий ИМ (в 1у коронарную артерию подсыпает, новый очаг некроза от 72 часов до 8 дней)
4. Повторный ИМ (в др. кор. арт.,новый очаг некроза через 28 дней от предыдущего ИМ)[3]
1.2 Этиология острого инфаркта миокарда
В настоящее время является общепризнанным предположение о патофизиологической роли коронаротромбоза в развитии острого инфаркта миокарда, выдвинутое в 1909 г. Н.Д. Стражеско и В.П. Образцовым, а в 1912 г. J.B. Herrick. Причиной острого инфаркта миокарда, как и других форм, острый коронарный синдром, более чем в 90% случаев является внезапное уменьшение коронарного кровотока, вызванное атеросклерозом в сочетании с тромбозом, с наличием или без сопутствующей вазоконстрикции. Редко отмечают острый инфаркт миокарда как следствие септической (тромба-)эмболии коронарной артерии или внутрикоронарный тромбоз как следствие воспалительного процесса в эндотелии сосуда при коронаритах различного генеза. Также описаны случаи острого инфаркта миокарда, развившиеся на фоне изолированного коронароспазма интактных артерий (чаще интоксикационной природы).
Среди этиологических факторов, способствующих развитию острого инфаркта миокарда, первое место занимает атеросклероз. Другие факторы риска инфаркта миокарда являются также факторами риска развития атеросклероза. К «большим» факторам риска относят некоторые формы гипер- и дислипопротеинемии, артериальная гипертония, курение табака, низкую физическую активность, нарушения углеводного обмена (особенно сахарный диабет II типа), ожирение, возраст пациента старше 50 лет (средний возраст госпитализированных больных с острым инфарктом миокарда в Италии составляет 67 лет). Действительно, нарушения липидного обмена диагностируют у больных с инфаркт миокарда значительно чаще, чем у здоровых людей (особенно дислипопротеинемии IIб и III типов). В то время как артериальная гипертония является доказанным фактором риска инфаркта миокарда, симптоматические формы артериальной гипертонии не сопряжены с высоким риском инфаркта миокарда. Это можно объяснить особенностями патогенеза артериальной гипертонии, которая, с одной стороны, способствует развитию атеросклероза, а с другой — предрасполагает к локальным спазмам артерий.
Результаты обширных исследований свидетельствуют о повышении частоты инфаркт миокарда у курящих. Объясняют это тем, что вещества, образующиеся при сгорании табака (в первую очередь никотин), повреждают эндотелий сосудов и способствуют вазоспазму, а высокое содержание карбоксигемоглобина в крови курящих снижает способность крови к переносу кислорода. Избыточная масса тела является фактором риска прогрессирования атеросклероза и инфаркта миокарда, если протекает по типу абдоминального ожирения. У больных со сниженной физической активностью на фоне развития атеросклероза недостаточно эффективно происходит адаптивное развитие коллатералей в миокарде и толерантности кардиомиоцита к ишемии (феномен прекондиции). Кроме того, вследствие гиподинамии происходит неадекватное повышение тонуса САС в случае нерегулярных значительных физических и психоэмоциональных нагрузок. Хроническое повышение уровня глюкозы и продуктов незавершенного углеводного обмена в крови при сахарном диабете приводит к повреждению эндотелия и развитию полиангиопатии.
При сочетании двух и более указанных факторов степень риска повышается пропорционально. Кроме перечисленных, существует еще множество так называемых «малых» факторов риска (подагра, псориаз, дефицит фолиевой кислоты и др.), удельный вес которых в общей структуре заболевания относительно невелик.
Клинические проявления и исходы зависят от локализации обструкции, степени и длительности ишемии миокарда. В частности, существуют отличия в степени проявления болевого обусловливающей наличие гипертензии, тахикардии, гипергликемии, лейкоцитоза с анэозинофилией в первые часы заболевания. Характерно, что во время развития острого инфаркта миокарда со стойкой элевацией сегмента ST формируется так называемый «красный» тромб, который содержит значительно большее количество эритроцитов.
Такое отличие от «тромбоцитарного», или «белого», тромба, связанного с развитием ОКС без стойкой элевации сегмента ST, свидетельствует о более глубоком и длительном нарушении реологических и коагуляционных свойств крови и о более значительных стойких тромбогенных изменениях в эндотелии поврежденного участка коронарной артерии. Следовательно, при остром инфарктом миокарда с элевацией сегмента ST развивается преимущественно окклюзивный и персистирующий тромбоз. Приблизительно в ⅔–¾ случаев формированию коронарного тромба предшествует внезапный разрыв уязвимой бляшки (воспаленной, богатой липидами бляшки, покрытой тонкой фиброзной оболочкой). Другие случаи связывают с механизмами, не определенными до конца, такими как эрозия бляшки. В ¾ случаев бляшки, которые становились базисом для окклюзивного тромбообразования во время острого инфаркта миокарда, вызывали лишь незначительный или умеренный стеноз, что предшествовало развитию инфаркта. Впрочем, на фоне выраженного стеноза разрывы бляшек приводят к более частому развитию острого инфаркта миокарда (по сравнению с незначительными стенозами).
Инфаркт миокарда, вызванный полной окклюзией коронарной артерии, развивается через 20–30 мин после начала выраженной ишемии (отсутствие кровотока по артерии) и прогрессирует со временем от субэндокардиального к субэпикардиальному участку (феномен фронта волны). Реперфузия и вовлечение коллатералей могут предотвращать возникновение некроза или способствуют уменьшению его размера (сохраняя в среднем до 70% ишемизированного миокарда периинфарктной зоны). Наличие же длительной стенокардии перед острым инфарктом миокарда может способствовать формированию развитых коллатералей, что обусловливает сохранение или длительное поддержание жизнеспособности зоны ишемии (при коронарной ангиографии развитые коллатерали определяют в 30% случаев острого инфаркта миокарда). [4]
У таких больных отмечена тенденция к менее выраженному повреждению миокарда, более редкому развитию сердечной недостаточности и меньшей летальности; в отдаленном периоде после острого инфаркта миокарда насосная функция сердца у них сохраняется в большей степени. При длительности коронарной окклюзии более 6 ч лишь небольшая часть (10–15%) ишемизированного миокарда остается жизнеспособной. Наличие субкритического, но стойкого кровотока может расширить временное окно для спасения миокарда путем полной реперфузии
Рисунок 1. Патогенетические стадии атеросклероза
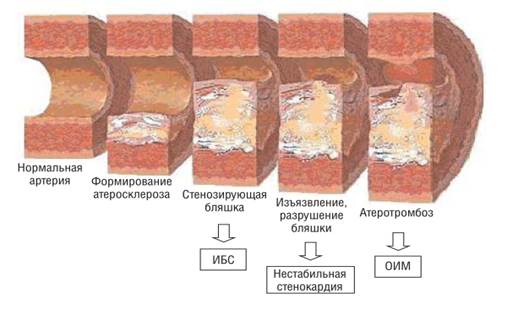
Ответ на разрыв бляшки является динамическим: аутогенные тромбоз и тромболизис, часто ассоциируемые с вазоспазмом, развиваются одновременно, вызывая преходящую обструкцию кровотока. В небольшом проценте случаев тромб, вызвавший развитие острого инфаркта миокарда, может быть разрушен в первые часы с начала заболевания собственной фибринолитической системой организма при содействии эндогенных вазодилататоров, устраняющих коронароспазм. В таком случае говорят о спонтанном (или аутогенном) лизисе тромба и реканализации инфарктобусловившей коронарной артерии.
Еще одним неблагоприятным последствием разрушения атеросклеротической бляшки и коронарного тромбоза является дистальная эмболизация тромботическими и атероматозными массами, которая ведет к микрососудистой обструкции и может препятствовать успешной реперфузии миокарда на тканевом уровне, неcмотря на восстановление адекватной проходимости инфарктобусловившей артерии
Рисунок 2. Развитие острого коронарного синдрома
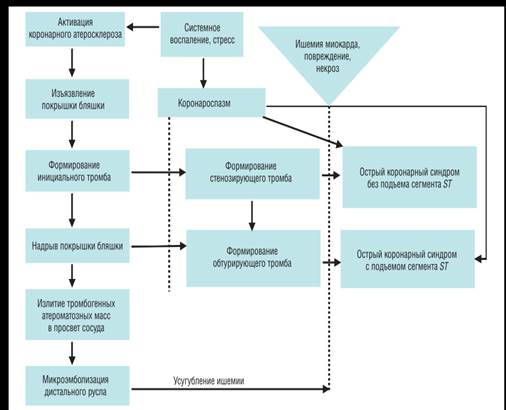
Развитие окклюзии коронарного сосуда ведет к гибели кардиомиоцитов. От уровня и длительности окклюзии сосуда зависит величина очага некроза миокарда. Нарушение коронарного кровотока и развитие некроза миокарда запускают каскад нейрогуморальных реакций, воспалительного и пролиферативного процесса. Все эти структурно-функциональные и метаболические перестройки миокарда ведут к ремоделированию полости левого желудочка: дилатации полости левого желудочка, изменению его геометрии и развитию гипертрофии, что может вести к появлению сердечной недостаточности и определяет отдаленный прогноз у пациентов, перенесших острый инфаркт миокарда
рисунок 3 патогенез постинфарктного ремоделирования полости ЛЖ (адаптировано по St. John Sutton, 2000).
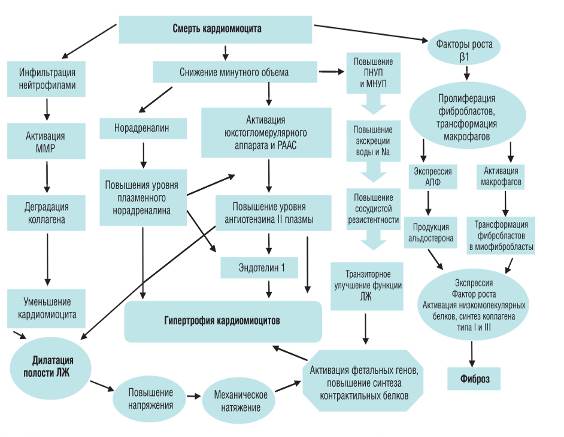
ПНУП — предсердный натрийуретический пептид; МНУП — мозговой натрийуретический пептид; ММР — матриксные металлопротеазы
В течение острого инфаркта миокарда можно выделить несколько патогенетических периодов. Продромальный период, или так называемое прединфарктное состояние, отмечают по разным данным в 30–60% случаев. Средняя длительность этого периода 7 дней, часто его начало сопряжено с физической или психоэмоциональной нагрузкой, причем наиболее неблагоприятными являются «малые», но регулярные стрессы, постоянное стрессовое состояние. Клинически его характеризуют возникновение или значительное учащение и усиление тяжести приступов стенокардии (так называемая нестабильная стенокардия), а также изменения общего состояния (слабость, утомляемость, снижение настроения, тревога, нарушение сна).
1.3 КЛИНИЧЕСКАЯ КАРТИНА
Острому инфаркту миокарда обычно предшествует стенокардия разной длительности течения, которая незадолго до развития инфаркта часто приобретает прогрессирующий характер: приступы ее учащаются, возрастает их продолжительность, они плохо купируются нитроглицерином. В ряде случаев инфаркт миокарда развивается внезапно у больных без клинически проявлявшегося заболевания сердца. Однако тщательный расспрос нередко позволяет и в подобных случаях установить, что за несколько дней до этого самочувствие больного ухудшилось: отмечались быстрая утомляемость, слабость, снизилось настроение, возникли неопределенные неприятные ощущения в грудной клетке. [7]
Типичные проявления инфаркта миокарда — ощущение сильного сдавления или боли за грудиной либо несколько левее или правее от нее. Боль чаще всего сжимающая, давящая, раздирающая (чувство кола в груди), иногда жгучая. Колющая или режущая ноющая боль не типичны. Характерна иррадиация боли в левые надплечье, плечо, руку, реже в шею и нижнюю челюсть, иногда в правую половину плечевого пояса, в межлопаточное пространство. Сравнительно редко (преимущественно при инфаркте задней стенки левого желудочка) боль локализуется в эпигастральной области.
Таблица 1. Характеристика и иррадиация боли:
| Болевой (status anginosus) | - типичное клиническое течение, основным проявлением при котором служит ангинозная боль, не зависящая от позы и положения тела, от движений и дыхания, устойчивая к нитратам; боль имеет давящий, душащий, жгущий или раздирающий характер с локализацией за грудиной, во всей передней грудной стенке с возможной иррадиацией в плечи, |
| Продолжение табл.1. | |
| шею, руки, спину, эпигастальную область; характерны сочетание с гипергидрозом, резкой общей слабостью, бледностью кожных покровов, возбуждением, двигательным беспокойством. | |
| Абдоминальный (status gastralgicus) | - проявляется сочетанием эпигастральных болей с диспептическими явлениями - тошнотой, не приносящей облегчения рвотой, икотой, отрыжкой, резким вздутием живота; возможны ирадиация болей в спину, напряжение брюшной стенки и болезненность при пальпации в эпигастрии. |
| Атипичный болевой | - при котором болевой синдром имеет атипичный характер по локализации (например, только в зонах иррадиации - горле и нижней челюсти, плечах, руках и т.д.) и/или по характеру. |
| Астматический (status astmaticus) | - единственным признаком, при котором является приступ одышки, являющийся проявлением острой застойной сердечной недостаточности (сердечная астма или отек легких). |
| Аритмический | - при котором нарушения ритма служат единственным клиническим проявлением или преобладают в клинической картине. |
| Цереброваскулярный | - в клинической картине, которого преобладают признаки нарушения мозгового кровообращения (чаще - динамического): обморок, головокружение, тошнота, рвота; возможна очаговая неврологическая симптоматика. |
| Малосимптомный (бессимптомный) | - наиболее сложный для распознавания вариант, нередко диагностируемый ретроспективно по данным ЭКГ. |
Лицо больного в период боли имеет страдальческий вид, кожа обычно бледная, иногда с цианотичным оттенком. Кисти, стопы, а нередко и весь кожный покров холодные и влажные. Дыхание учащенное и нередко поверхностное. Артериальное давление в момент возникновения боли может повышаться, но вскоре падает до необычно низкого для больного уровня. Выявляется мягкий и частый пульс слабого наполнения. Тоны сердца ослаблены, иногда над верхушкой сердца и в четвертом межреберье слева от грудины выслушивается во время диастолы дополнительный третий тон (диастолический ритм галопа). У большинства больных можно выявить различные аритмии сердца. При неосложненном инфаркте миокарда возникновение шумов сердца незакономерно; у некоторых больных над верхушкой сердца определяется слабый систолический шум. Внезапное появление выраженного шума характерно для осложненного инфаркта миокарда (аневризма, разрыв перегородки, инфаркт сосочковой мышцы и др.). На 2 —5-й день болезни примерно у четверти больных над передней поверхностью сердца появляется шум трения перикарда вследствие развития фибринозного перикардита. Через несколько часов от начала заболевания повышается темпратура тела (редко превышая 38,5 °С), нормализующаяся обычно в течение последующих 5 дней.
Инфаркт миокарда может начинаться или сочетаться с картиной острой мозговой сосудистой катастрофы, спутанностью сознания, расстройствами речи В основе церебральной симптоматики лежат нарушения мозгового кровообращения вследствие уменьшения сердечного выброса и спазма сосудов мозга.
Клиническое течение инфаркта миокарда крайне разнообразно. Одни больные переносят его на ногах, у других он протекает хотя и с типичной клинической симптоматикой, но без серьезных осложнений, в ряде случаев — как тяжелое длительное заболевание с опасными осложнениями, которое может привести к смертельному исходу. У некоторых больных в результате инфаркта миокарда наступает внезапная смерть.[9]
