Основы количественного анализа.
Кафедра общей химии
РАБОЧАЯ ТЕТРАДЬ
ПО КУРСУ ХИМИИ
ДЛЯ СТОМАТОЛОГИЧЕСКОГО ФАКУЛЬТЕТА
СТУДЕНТА __________ ГРУППЫ
СТОМАТОЛОГИЧЕСКОГО ФАКУЛЬТЕТА
__________________________________________________
__________________________________________________
20___ – 20___ учебный год
ОСНОВНЫЕ ПРАВИЛА РАБОТЫ В ХИМИЧЕСКОЙ ЛАБОРАТОРИИ И ТЕХНИКА ВЫПОЛНЕНИЯ ХИМИЧЕСКОГО ЭКСПЕРИМЕНТА
Правила поведения в химической лаборатории и технику безопасности:
ü к эксперименту приступают только после ознакомления со всеми его этапами;
ü на лабораторном столе должны находиться только необходимые для эксперимента приборы, оборудование лабораторный журнал;
ü в лаборатории работают только в халате;
ü нельзя брать руками вещества и пробовать их на вкус;
ü опыты с ядовитыми и летучими веществами, концентрированными растворами кислот и щелочей проводят под тягой;
ü при приливании реактивов нельзя наклоняться над отверстием сосуда во избежание попадания брызг на лицо и одежду;
ü нельзя работать с легковоспламеняющимися жидкостями вблизи включенных электрических и нагревательных приборов;
ü нельзя выливать в раковину остатки кислот, щелочей и огнеопасных веществ их следует сливать в специально предназначенные для этого склянки;
ü для засасывания кислот и щелочей в пипетку пользуются резиновыми грушами;
ü разбавляя концентрированные кислоты, осторожно вливают кислоту в воду, а не наоборот.
При несоблюдении правил техники безопасности в лаборатории, бывают несчастные случаи, требующие первой неотложной помощи, для ее оказания в лаборатории должна быть аптечка. Основные правила скорой помощи следующие:
- при термическом ожоге кожу обрабатывают спиртом или свежеприготовленным раствором перманганата калия, а затем смазывают мазью от ожогов или присыпают танином;
- при химических ожогах глаз обильно промывают глаза водой, используя глазную ванночку, после этого следует обратиться к врачу;
- при ожогах кислотой необходимо омыть реактив большим количеством воды, затем обработать кожу растворам соды;
- при ожогах щелочью необходимо смыть реактив большим количеством воды, затем промыть участок кожи разбавленной уксусной кислотой, а затем снова водой.
Прежде чем приступить к эксперименту, студенты должны изучить соответствующий раздел учебника, лекций, а также ознакомиться с описанием работы и ответить на вопросы для самоподготовки.
С правилами поведения в химической лаборатории и техникой безопасности ознакомлен:
_____________________________________________________________
Дата:
Подпись:
______________ ______________
Основы количественного анализа.
Способы выражения концентрации раствора.
Основные способы выражения состава растворов
Массовая доля _______________________
Молярная концентрация ____________________
Массовая концентрация _____________________
Моляльная концентрация ____________________
Формулы перехода от одних способов выражения состава раствора к другим
| Обозначение | w (Х) | с(Х) | сm(X) |
| Массовая доля w (Х) | w | с(Х) М(Х) 1000 r | с(Х) М(Х)______ 1000 + с(Х) М(Х) |
| Молярная концентрация с(Х), моль/л | w(Х) r 1000 М(Х) | с | сm(X) r 1000 1000 + сm(Х)М(Х) |
| Моляльная концентрация сm(X), моль/л | 1000 w(Х)__ (1 - w(Х)) М(Х) | 1000 с(Х)_____ 1000r - с(Х)М(Х) | сm |
Задания для самостоятельной работы
1) Рассчитайте молярную концентрацию раствора нитрата алюминия с массовой долей 16%, плотность раствора 1,14 г/мл.
2) Рассчитайте, какой объем дихромата калия с массовой долей 12% (плотность 1,086 г/мл) потребуется для приготовления 1,5 л раствора с молярной концентрацией 0,05 моль/л.
3) Раствор хлорида железа (П) с концентрацией 0,1 моль/л объемом 250 мл смешали с раствором хлорида железа (Ш) с концентрацией 0,5 моль/л объемом 200 мл. Вычислите молярные концентрации веществ в образовавшемся растворе.
4) Для проведения химической реакции требуется сульфат марганца массой 18 мг. Какой объем раствора с концентрацией 0,2 моль/л содержит эту массу вещества?
Занятие 2
Основы количественного анализа.
Кислотно – основное титрование.
Дата_________Лабораторная работа № ______
Ход работы.
- Бюретку заполняют стандартизованным раствором HCl.
- Контрольный раствор NaOH переносят из пробирки в мерную колбу, объем раствора доводят до метки дистиллированной водой.
- Раствор перемешивают и переносят в коническую колбу (250 мл), из которой берут пробы для титрования (аликвотные доли) с помощью пипетки Мора.
- Каждую аликвотную долю переносят в 5 сухих конических колб для титрования. В каждую колбу добавляют по 2 капли индикатора.
- титруют растворы в колбах по очереди до изменения окраски индикатора. Перед каждым последующим титрованием доливают титрант в бюретку до нулевого деления.
Экспериментальные данные.
Концентрация титранта с(HCl) = ______________ моль/л
Объем анализируемого раствора
после разбавления V(NaOH) = __________ мл
Аликвотная доля анализируемого раствора
после разбавления Vа(NaOH) = _________ мл
Результаты титрования V(HCl), мл 1 _________________
2 _________________
3 _________________
4 _________________
Среднее значение V(HCl), мл _________________
Расчеты:
Вывод:
Задания для самостоятельной работы
1) Вычислите объем раствора азотной кислоты с концентрацией 0,065 моль/л, необходимый для титрования раствора, содержащего 0,1 г гидроксида калия.
2) Раствор муравьиной кислоты массой 2,32 г разбавлен водой до 100 мл. На титрование 10 мл разбавленного раствора затрачено 7,2 мл раствора гидроксида калия с концентрацией 0,15 моль/л. Рассчитайте массовую долю муравьиной кислоты в исходном растворе.
Занятие 2.
Ход работы.
1. Измеряют температуру исходных растворов.
Мерным цилиндром переносят требуемый объем щелочи в колориметрический стакан и измеряют температуру раствора.
Мерным цилиндром отмеривают такой же объем кислоты и измеряют температуру
2. Измеряют максимальную температуру после сливания растворов.
Экспериментальные данные.
| № опыта | Температура раствора, о С | ||
| кислоты (исх) | щелочи (исх) | после нейтрализации | |
| Среднее значение |
Концентрации растворов _____
Объемы растворов _____
Плотности растворов________________
Масса калориметрического стакана
Справочные величины
Суд (р-ра) = 4,184 Дж/г×К Суд (стекла) = 0,753 Дж/г × К
Расчеты
Вывод:
Занятие 3. Химическая термодинамика. II начало термодинамики.
Химическая кинетика.
Задания для самостоятельной работы
1) Константа скорости реакции: (СН3СО)2О + Н2О <=> 2 СН3СООН при 15оС равна 0,45 мин-1. Исходная концентрация уксусного ангидрида равна 0,5 моль/л. Вычислите скорость реакции в момент, когда концентрация уксусной кислоты станет равной 0,1 моль/л.
2) Рассчитайте период полупревращения реакции при 77оС, если энергия активации реакции равна 65кДж/моль, аконстанта скорости при 37оС равна 0,25 ч-1.
3) Вычислите температурный коэффициент скорости реакции разложения трихлоруксусной кислоты в воде (20 – 40оС), энергия активации равна 155кДж/моль.
4) Во сколько раз возрастет скорость реакции разложения ацетондикарбоновой кислоты в растворе при 298К, если энергия активации реакции без катализатора равна 97кДж/моль, а в присутствии катализатора снижается на 40% (считать, что А=Const).
Задания для самостоятельной работы
3-56. Константа скорости гидролиза этилового эфира фенилаланина при рН 7,3 и t = 20 °С в присутствии ионов меди равна 2,67×10-3 с-1. Начальная концентрация эфира равна 0,2 моль/л. Чему будет равна скорость реакции по истечении двух периодов полупревращения?
3-57. Константа скорости разложения хлорида фенилдиазония в воде при 50 °С равна 0,071 мин-1. Сколько времени нужно нагревать раствор с начальной концентрацией, равной 0,03 моль/л, чтобы концентрация стала равна 0,0001 моль/л?
3-62. При лечении онкологических заболеваний в опухоль вводят препарат, содержащий радионуклид иридий-192. Какая часть введенного радионуклида останется в опухоли через 10 суток?
3-63. Для проведения исследований были взяты равные массы двух радионуклидов: цезий-137 и цирконий-95. Какая часть 95Zr останется к тому моменту, когда 2 % 137Cs подвергнется распаду?
3-69. Гидролиз инсектицида в воде при 20 °С протекает с константой скорости 2,5
год-1. Некоторое количество инсектицида было смыто в озеро, где средняя его концентрация составила 0,72 мкг/мл. Вычислите время, необходимое для уменьшения концентрации инсектицида в озере до 0,30 мкг/мл.
3-84. Энергия активации некоторой реакции первого порядка равна 80 кДж/моль. При 25 °С за 10 мин вступает в реакцию 30 % вещества. Какая масса (в % от исходной) вещества вступает в реакцию за то же время при 45 °С?
3-85. Денатурация вируса - процесс первого порядка с энергией активации 630 кДж/моль. Период полупревращения при 30 °С равен 5 часам. Рассчитайте период полупревращения при 37 °С.
3-107. Вычислите температурный коэффициент константы скорости реакции разложения ацетондикарбоновой кислоты в водном растворе (20 °С - 40 °С), Еа = 97 кДж/моль.
3-108. При повышении температуры от 25 °С до 45 °С скорость реакции увеличилась в 7 раз. Вычислите температурный коэффициент скорости реакции.
Занятие 5 Коллигативные свойства растворов.
Задания для самостоятельной работы
1) Какую массу сахарозы надо растворить в 250 г воды, чтобы получить раствор, кипящий при 100,2оС. При какой температуре замерзает такой раствор?
2) Опишите поведение эритроцитов при 310К в растворе глюкозы с массовой долей 2%, плотность раствора 1,01 г/мл.
3) Раствор, содержащий уксусную кислоту массой 0,571 г в 100 г воды, замерзает при температуре –0,181оС. Вычислите изотонический коэффициент уксусной кислоты и осмотическое давление раствора при 298К (плотность раствора 1 г/мл).
4) К 150 мл раствора гидроксида калия с концентрацией 0,01 моль/л добавили 200 мл соляной кислоты с концентрацией 0,1 моль/л. Вычислите активность ионов водорода в полученном растворе.
Занятие 6
Экспериментальные данные
Приблизительное значение рН _____________
Выбранный индикатор ____________________________
Светофильтр ___________________
Значения оптической плотности: Ах = ______________ Аmax = ________________
Сущность работы.
Для расчета рН ацетатной буферной системы используют уравнение:
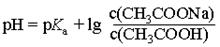 |
Анализ приведенного уравнения позволяет сделать следующие выводы: рН буферных растворов зависит от константы диссоциации сопряженной кислоты, от соотношения концентраций (количеств веществ) компонентов кислотно-основной пары, практически не зависит от разбавления раствора водой.
При введении в буферный раствор небольшого количества (X моль) сильной кислоты рН получившегося буферного раствора можно рассчитать следующим образом:
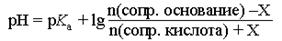 |
где n – количество вещества компонента буфера, моль.
При введении в буферный раствор небольшого количества (Y моль) сильного основания, рН буферного раствора можно рассчитать по формуле:
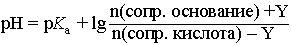 |
Ход работы.
Опыт 1. Приготовление буферных растворов с различным значением рН.
1. Готовят серию буферных растворов с разными соотношениями концентраций компонентов. Рассчитывают, какие объемы исходных растворов требуются для приготовления буферных растворов объемом по 10,0 мл с соотношением концентраций соли (CH3COONa) и кислоты (CH3COOH): в пробирке №1-1:9; в пробирке №2- 1:1; в пробирке №3-9:1. Точные объемы растворов уксусной кислоты и ацетата натрия отмеривают в пробирки из бюреток; содержимое пробирок тщательно перемешивают стеклянной палочкой.
2. Готовят серию буферных растворов с тем же соотношением концентраций соли и кислоты, но с меньшей суммарной концентрацией компонентов. Для этого пипеткой отбирают по 1,0 мл приготовленных ранее растворов и к каждому добавляют по 8,0 мл дистиллированной воды, после чего содержимое перемешивают. Таким образом, в пробирках №1 и №4, №2 и №5, №3 и №6 находятся растворы с одинаковыми соотношениями концентраций соли и кислоты, но растворы в пробирках №№4,5 и 6 являются разбавленными по сравнению с растворами в пробирках №№1,2 и 3.
3. Во все пробирки добавляют по 5 капель раствора лакмоида, после чего содержимое пробирок перемешивают. На белом фоне сравнивают окраску растворов между собой.
4. Рассчитывают рН приготовленных буферных растворов.
Экспериментальные данные
| Пробирка с исходным буферным раствором | №1 | №2 | №3 |
| С(NaCH3COO): C(CH3COOH) | |||
| Цвет буферного раствора после добавления лакмоида | |||
| рН исходного буферного раствора | |||
| Пробирка с разбавленным буферным раствором | №4 | №5 | №6 |
| С(NaCH3COO): C(CH3COOH) | |||
| Цвет разбавленного буферного раствора после добавления лакмоида | |||
| рН разбавленного буферного раствора |
Справочные данные: рКа(CH3COOH/ CH3COO-) = ________________
Расчет рН
Вывод к опыту 1:
Опыт 2. Влияние добавления небольших количеств сильных кислот и оснований на рН буферного раствора.
1. В пробирках №1 и №2 готовят по 10 мл буферного раствора с соотношением концентраций ацетата натрия и уксусной кислоты, равным 2:3, для чего предварительно рассчитанные объемы растворов наливают из бюреток. В пробирки №3 и №4 отбирают с помощью пипетки по 10 мл физиологического раствора (0,9% раствора хлорида натрия). Ко всем растворам добавляют по 5 капель раствора лакмоида и содержимое пробирок перемешивают. Наблюдаемую окраску записывают в таблицу. При необходимости окраску физиологических растворов выравнивают, добавляя в пробирки №3 и №4 по каплям разбавленную соляную кислоту с концентрацией 0,01 моль/л. После каждой добавленной капли кислоты раствор перемешивают стеклянной палочкой.
2. В пробирки №1 и №3 добавляют по 5 капель раствора гидроксида натрия с концентрацией 0,1 моль/л. В пробирки №2 и №4 добавляют по 5 капель соляной кислоты с концентрацией 0,1 моль/л. Все растворы перемешивают и наблюдаемую окраску записывают в таблицу.
Экспериментальные данные
| № раствора | Объект изучения | Окраска раствора после добавления лакмоида | + 5 капель HCl, с =0,1 моль/л. | +5 капель NaOH, с =0,1 моль/л. |
| Буферный раствор | ------ | |||
| Буферный раствор | ----- | |||
| Физиологический раствор | ------ | |||
| Физиологический раствор | ------ |
Вывод к опыту 2:
Задания для самостоятельной работы
4-55. Водный раствор сульфата меди с массовой долей 1 % назначают в малых дозах для улучшения кроветворной функции. Вычислите активность ионов меди в таком растворе (плотность раствора 1,009 г/мл).
4-56. При отравлениях цианидами внутривенно вводят 2 %-ный водный раствор нитрата натрия с плотностью 1,011 г/мл. Вычислите активности ионов в этом растворе.
4-57. К 150 мл раствора гидроксида калия с(КОН) = 0,01 моль/л добавили 200 мл соляной кислоты с(НСl) = 0,15 моль/л. Вычислите активность ионов гидроксония в получившемся растворе.
4-59. Вычислите температуру кипения и температуру замерзания водного раствора
сахарозы с массовой долей, равной 2 %.
5-52. Вычислите рН соляной кислоты с молярной концентрацией хлороводорода, равной 0,004 моль/л.
5-53. Вычислите рН раствора гидроксида натрия с концентрацией 2,5 ммоль/л.
5-54. Вычислите рН раствора азотной кислоты с массовой долей 1,255 % (r = 1,005 г/мл).
5-56. Вычислите рН водного раствора смеси хлороводорода и хлорида натрия, в котором концентрация каждого вещества равна 0,05 моль/л (с учетом коэффициента активности).
5-57. Вычислите рН раствора уксусной кислоты с молярной концентрацией, равной 0,001 моль/л.
5-59. Чему равно значение рН раствора азотной кислоты с концентрацией 0,002 моль/л? Чему равна концентрация раствора уксусной кислоты, имеющего такое же значение рН?
5-60. Вычислите рН раствора аммиака с молярной концентрацией 0, 15 моль/л.
5-125. Какое максимальное и минимальное количество вещества гидроксида натрия можно прибавить к 12 г ледяной уксусной кислоты, чтобы после растворения смеси в 1 л воды получился буферный раствор?
5-126. Как изменится рН фосфатного буферного раствора, содержащего 100 мл раствора дигидрофосфата натрия и 300 мл раствора гидрофосфата натрия (концентрации исходных растворов равны по 0,1 моль/л), при добавлении к нему 20 мл раствора NaOH с концентрацией 0,1 моль/л?
Занятие 8
Гетерогенные процессы.
Дата_________Лабораторная работа
Экспериментальные данные
Таблица 1
| Исходная концентрация Са2+, моль/л | Исходная концентрация аниона, моль/л | Пс | Ks | Наблюдения |
| С2О42- - | ||||
| SO42— |
Расчет ПС:
Опыт 2.
1. В три пробирки отмеривают по 1мл (точно, с помощью градуированной пипетки или из бюретки) раствора хлорида кальция. В пробирки №1 и №2 добавляют по 1 мл дистиллированной воды, в пробирку №3 добавляют 1 мл раствора цитрата натрия. После этого в пробирки №1 и №3 отмеривают по 1 мл раствора гидрофосфата натрия, а в пробирку №2 – 1 мл раствора дигидрофосфата натрия. Содержимое пробирок перемешивают с помощью стеклянной палочки. Наблюдения записывают в таблицу 1.
2. В пробирку №1 прибавляют по каплям соляную кислоту (с = 0,1 моль/л), а в пробирку №2 – по каплям раствор гидроксида натрия (с = 0,1 моль/л). Содержимое пробирок при необходимости перемешивают с помощью стеклянной палочки.
Уравнения реакций:
Наблюдения записываю в таблицу 2.
Экспериментальные данные
Таблица 2
| № | Содержимое пробирки | Пс | Ks | Наблюдения | Наблюдения | |
| НCl | ||||||
| NaOH | ||||||
| _____ |
Расчет ПС:
Опыт 3. В пробирку вносят 3-4 капли раствора нитрата свинца (с=0,2 моль/л), добавляют несколько капель раствора хлорида натрия (с=0,2 моль/л) до образования осадка. К содержимому пробирки приливают 1-2 мл дистиллированной воды до растворения осадка, после чего прибавляют несколько капель насыщенного раствора хлорида натрия. Отмечают и объясняют изменения, происшедшие в пробирке.
Уравнения реакций:
Наблюдения:
Опыт 4. В пробирку вносят 10 капель растворов сульфата натрия и хромата натрия; после перемешивания к содержимому пробирки добавляют по каплям раствор нитрата свинца. Отмечают изменения, происходящие в пробирке. Последовательность выпадения осадков объясняют с помощью термодинамических данных.
Уравнения реакций:
Справочные данные: КS(PbSO4) = _______________ КS(PbCrO4) = ____________________
Наблюдения:
Выводы:
Задания для самостоятельной работы
6-26. Растворимость оксалата никеля (II) равна 3 мг/л. Вычислите константу растворимости этого соединения.
6-27. Вычислите массу серебра, содержащегося в виде ионов в насыщенном водном растворе цианида серебра объемом 500 мл.
6-28. Вычислите массу золота, находящегося в виде ионов в насыщенном водном растворе хлорида золота (I) объемом 150 мл.
6-29. Вычислите массовую концентрацию ионов таллия (в граммах на литр) в насыщенном водном растворе оксалата таллия (I).
6-30. Вычислите массу карбоната магния, находящуюся в 750 мл его насыщенного раствора.
6-35. Токсичность ионов бария проявляется при концентрации выше 4 мг/л. Докажите, что сульфат бария можно использовать как рентгеноконтрастное средство при исследовании желудочно-кишечного тракта.
6-36. В каком объеме насыщенного раствора фосфата серебра находится ионное серебро массой 0,2 мг?
6-50. Вычислите, во сколько раз растворимость сульфата стронция в дистиллированной воде больше его растворимости в растворе сульфата калия с концентрацией 0,3 моль/л.
Занятие 9
Экспериментальные данные.
| Опыт | Золь | Метод получения | Внешний вид | Наблюдение конуса рассеяния света | ||
| Физический или химический | Диспергирование или конденсация | В проходящем свете | В отраженном свете | |||
Опыт 4. Определение порогов коагуляции.
1. Проводят последовательно два опыта с растворами электролитов Na2SO4 и К3[Fe(CN)6]. Готовят исходные растворы электролита различных концентраций, смешивая в пяти пробирках отмеренные с помощью бюреток исходный раствор электролита и дистиллированную воду в соотношениях, указанных в таблице.
2. В пять хорошо вымытых пробирок отмеривают из бюретки по 5,0 мл гидрозоля железа(III). Во все пробирки с золем приливают по возможности одновременно приготовленные растворы электролита и тотчас же перемешивают. Через 10 мин отмечают, в каких пробирках наблюдается помутнение или образование осадка. Результаты наблюдений записывают в таблицу: знаком «+» отмечают наличие коагуляции, знаком «─» отсутствие.
Экспериментальные данные.
| Пробирка | Объем, мл | Результаты наблюдений Коагулирующий электролит | |||
| Раствор электролита | Вода | Na2SO4 | К3[Fe(CN)6]. | ||
| 2,5 | 0,5 | ||||
| 2,0 | 1,0 | ||||
| 1,5 | 1,5 | ||||
| 1,0 | 2,0 | ||||
| 0,5 | 2,5 |
Выводы
Вопросы и задания к лабораторной работе:
1) Напишите схемы реакций образования гидротартрата и тартрата калия.
Наличие какого структурного фрагмента в винной кислоте доказывает реакция образования фелинговой жидкости?
2) Напишите уравнение реакции салициловой кислоты с гидрокарбонатом натрия. Наличие какой функциональной группы в салициловой кислоте доказывает эта реакция?
Какие кислотные центры присутствуют в молекуле салициловой кислоты? Сравните их силу (значения констант ионизации салициловой кислоты по первой ступени: К1 = 1,1×10-3, по второй ступени: К2 = 2,6 ×10-14).
4) Напишите уравнение реакции салициловой кислоты с раствором брома.
5) Напишите уравнение реакции декарбоксилирования салициловой кислоты.
6) Приведите схему реакции гидролиза ацетилсалициловой кислоты.
Чем обусловлено появление фиолетовой окраски после добавления хлорида железа (III)?
Задания для самостоятельной работы
1) Заполните таблицу
| Функциональные группы | Название класса гетерофункциональных соединений | Пример соединения структурная формула название | |
| - OH ü ý - NH2 þ | 2-аминоэтанол (коламин) | ||
| - OH ü ý - COOH þ | 2-гидроксипропано вая (молочная) кислота | ||
| - NH2 ü ý - COOH þ | 2-аминопропано- вая кислота (глицин) | ||
 ü ü  C=O ý - COOH þ C=O ý - COOH þ | 2-оксопропановая (пировиноградная) кислота |
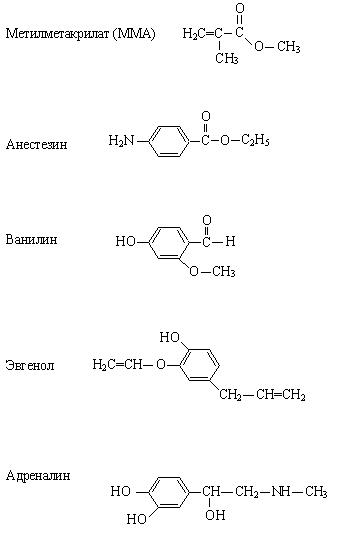
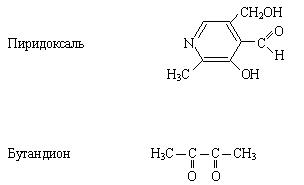
2) -Обозначьте сопряженный фрагмент, укажите вид сопряжения в молекулах.
-Укажите функциональные группы, назовите их.
-Укажите соединения, относящиеся к полифункциональным; к гетерофункциональным.
Коричная кислота С6Н5¾СН=СН¾СООН
Сорбиновая кислота СН3¾СН=СН¾ СН=СН¾СООН
Фумаровая кислота НООС¾СН=СН¾СООН

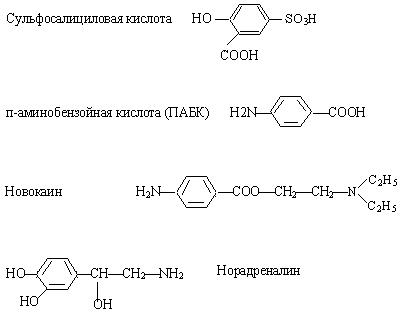
3) Напишите схемы образования и дайте название продукта:
1) циклического моноэфира g-лактона из 4-гидроксибутановой (g-гидроксимасляной) кислоты:
2) циклического моноамида g-лактама из 4-аминобутановой (g-аминомасляной) кислоты:
3) циклического сложного эфира лактида из 2-гидроксипропановой (молочной) кислоты:
Занятие 15
Выводы
Задания для самостоятельной работы
1) В соответствии с общей схемой окисления тиолов в дисульфиды:
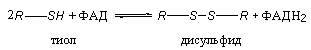
допишите реакцию окисления дигидролипоевой кислоты в липоевую:
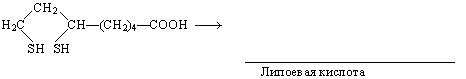
2) Заполните схему окислительного дезаминирования a-аминокислот:
H
| НАД+ Н2О (Н+или ОН-)
R-C-COOH ¾¾¾¾® ¾¾¾¾®
| - НАДН _______________ __________________
NH2
a-аминокислотa a-иминокислотa a-оксокислотa
3) Заполните схемы:
НООС-СН-СН2-СООН + НАД+ ¾® + НАДН + Н+
| ________________________
ОН щавелевоуксусная
яблочная кислота кислота
НООС-СН2 -СН2-СООН + ФАД ¾® + ФАДН2
_____________________
янтарная кислота фумаровая кислота
Занятие 16 Гетероциклические соединения
Задания для самостоятельной работы
1) Приведите структурные формулы гетероциклических соединений:
__________________ ___________________ ____________________
пиррол тиофен фуран
____________________ ____________________
пиразол имидазол
_________________ ____________________ ____________________
пиридин пиримидин хинолин
_______________ ____________________ ____________________
цитозин урацил тимин
_________________ ___________________ ____________________
пурин аденин гуанин
______________________ _____________________________
ксантин барбитуровая кислота
2) Дайте определение понятия «ароматичность». Покажите соответствие критериям ароматичности следующих соединений:
| Соединение | Структурная формула | Соответствие критериям ароматичности |
| Салициловая Кислота | ||
| Нафталин | ||
| Никотиновая кислота | ||
| Гистамин | ||
| Аденин | ||
| 8-гидроксихинолин | ||
| Кофеин | ||
| Имидазол |
Занятие 17
Занятие 18
Экспериментальные данные
| Пробирка | Полимер | Среда | Результаты наблюдений |
| 1. 2. 3. 4. | Желатин Желатин Резина Резина | Вода Толуол Вода Толуол |
По окончании работы толуол выливают в специальную склянку для слива органических растворителей.
Опыт 2. Изучение влияния электролитов на величину набухания ВМС.
В три сухие пронумерованные пробирки одинакового диаметра помещают примерно одинаковое количество желатина (0,5 см по высоте пробирки). С помощью полоски миллиметровой бумаги измеряют высоту слоя сухого желатина до набухания (h0); результаты записывают в таблицу. Пробирки примерно до середины заполняют из бюреток: 1 — дистиллированной водой, 2 — раствором сульфата натрия с концентрацией 1,0 моль/л, 3 — раствором иодида натрия с концентрацией 1,0 моль/л. Через 1—2 мин после заполнения пробирок содержимое их осторожно перемешивают стеклянной палочкой, чтобы набухшие частицы верхнего слоя желатина не затрудняли доступ жидкости к частицам нижнего слоя. Примерно через 20 мин осторожным постукиванием по верхней части пробирки добиваются осаждения всплывших частиц желатина и измеряют высоту слоя набухшего желатина (h). Рассчитывают степень набухания желатина в воде и растворах электролитов. Результаты измерений и расчетов записывают в таблицу.
Экспериментальные данные
| Пробирка | Среда | Высота слоя сухого желатина ho, мм | Высота слоя набухшего желатина h, мм | Степень набухания |
| 1. | Вода | |||
| 2. | Раствор Na2SO4 | |||
| 3. | Раствор NaI |
Опыт 3. Определение изоэлектрической точки желатина.
В шесть сухих пронумерованных пробирок (одинакового диаметра или градуированные) помещают примерно одинаковое количество желатина (0,5 мл по высоте пробирки); с помощью полоски миллиметровой бумаги измеряют высоту сухого желатина в каждой пробирке (h0) и результаты измерений записывают в таблицу. В каждую из пробирок осторожно по стенке наливают из бюреток по 7,0 мл растворов с различными значениями рН. Через 1—2 мин содержимое пробирок осторожно перемешивают, а через 20 мин осаждают всплывшие частицы желатина (как в опыте 2) и измеряют высоту слоя набухшего желатина (h); результаты измерений записывают в таблицу.
Экспериментальные данные
| Пробирка | рH раствора | Высота слоя сухого желатина ho, мм | Высота слоя набухшего желатина h, мм | Dh, мм |
Обработка результатов эксперимента:
Для определения ИЭТ желатина строят график зависимости Dh = f (pH). ИЭТ находят, опустив из точки минимума на кривой перпендикуляр на ось абсцисс.
Приложение
Органические вещества
| Вещество или ион | Состояние | DfH°298 | DfG°298 | S°298 |
| СН4 | г | - 85 | - 51 | |
| С2Н2 | г | |||
| С2Н4 | г | |||
| С2Н6 | г | -107 | - 33 | |
| С6Н6 | ж | |||
| CH3CI | г | -82 | -59 | |
| СН2С12 | г | -88 | -59 | |
| СНС13 | г | -100 | -67 | |
| СС14 | г | -107 | -64 | |
| CH3Br | г | -35,6 | -26 | |
| СН2Вг2 | г | -4,2 | -5,9 | |
| СНВгэ | г | |||
| СВг4 | г | |||
| CH3OH | ж | -239 | -166 | |
| C2H5OH | ж | -278 | -175 | |
| Глицерин | ж | -671 | -479 | |
| Формальдегид | г | -116 | -110 | |
| Ацетальдегид | г | -166 | -134 | |
| Ацетон | ж | -247 | -154 | |
| HCOOH | ж | -410 | -346 | |
| HCOO- | aq | -410 | -335 | |
| CH3COOH | ж | -487 | -392 | |
| CH3COO - | aq | -404 | ||
| СзН7СООН | ж | -535 | -376 | |
| СзН7СОО - | к | -536 | -372 | |
| Г люкозо-1-фос форная кислота | aq | -1789,5 | ||
| Нитробензол | ж | |||
| Анилин | ж | |||
| Глицин | к | -537 | -378 | 103,5 |
| Глицин | aq | -523 | -380 | 158,6 |
| Цистеин | к | -532,6 | .-342,7 | 169,9 |
| L-лейцин | aq | -643,4 | -352,3 | 207,5 |
| D. L-лейцилгли- цин | aq | -464 | ||
| Глицилглицин | aq | -734,3 | 492,1 | 231,4 |
| Пируват-ион | aq | -596,2 | -472,4 | 171,5 |
| L-молочная кис- | aq | -686 | -539 | |
| лота | ||||
| Сахароза | к | -2222 | -1545 | |
| D-глюкоза | aq | -1263,8 | -917,0 | 269,5 |
| D-глюкоза | к | -1274,5 | -910,6 | 212,1 |
4. Теплоты сгорания (DcH°, кДж/моль) некоторых органических веществ
| Вещество | Состояние | DcH° | Вещество | Состояние | DcH° |
