ПРИ ИЗУЧЕНИИ ХИМИИ d-ЭЛЕМЕНТОВ
САМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ
ПРИ ИЗУЧЕНИИ ХИМИИ
D-ЭЛЕМЕНТОВ
ВОРОНЕЖ 2013
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ
РОССИЙСКОЙ ФЕДЕРАЦИИ
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ «ВОРОНЕЖСКИЙ ГОСУДАРСТВЕННЫЙ ПЕДАГОГИЧЕСКИЙ УНИВЕРСИТЕТ»
САМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ
ПРИ ИЗУЧЕНИИ ХИМИИ d-ЭЛЕМЕНТОВ
Методические указания
для студентов II курса профилей “Химия”, “Экология”
естественно-географического факультета
Составитель: к. х. н., доцент кафедры химии
Звонарева Е.А.
ВОРОНЕЖ 2013
УДК 546 (076) Изданы по решению
ББК 24.1 я 73 учебно-методического совета ВГПУ
С о с т а в и т е л ь:
кандидат химических наук, доцент кафедры химии
Е.А. Звонарева
Р е ц е н з е н т ы:
кандидат технических наук, доцент кафедры химии
Н.И. Кочергина (ВГПУ)
кандидат химических наук, доцент кафедры химии
О.В. Дьяконова (ВГАУ)
П69 Самостоятельная работа студентов при изучении химии d-элементов:Методические указания для студентовII курса профилей “Химия”, “Экология” естественно-географического факультета. - Воронеж: ВГПУ, 2013. - 38 с.
Методические указания содержат планы практических занятий по химии d-элементов, вопросы для самостоятельной подготовки по наиболее важным разделам курса, вопросы, упражнения и задачи для самоконтроля. Приведен список рекомендуемой литературы.
Для студентов II курса профилей “Химия”, “Экология” естественно-географического факультета.
УДК 546 (076)
ББК 24.1 я 73
© Звонарева Е.А., составление, 2013. Редакционно-издательское оформление. ВГПУ, 2013.
СОДЕРЖАНИЕ
ПРЕДИСЛОВИЕ АВТОРА… … … … … … … … … … … … … … … ... … … 5
КОМПЕТЕНЦИИ ОБУЧАЮЩЕГОСЯ, ФОРМИРУЕМЫЕ В РЕЗУЛЬТАТЕ ОСВОЕНИЯ ДИСЦИПЛИНЫ… … … … … … … … … … … … … … … ... …5
СОСТАВ, КЛАССИФИКАЦИЯ И НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙ… … … … … … … … … … … … … … … … … … … … … ..7
РАВНОВЕСИЯ В РАСТВОРАХ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ … … … ..9
ПРОСТРАНСТВЕННАЯ СТРУКТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙ, ИХ СВОЙСТВА … … … … … … … … … … … … … … … … … … … … … ... .11
d-ЭЛЕМЕНТЫ VIII В-ГРУППЫ. СЕМЕЙСТВО ЖЕЛЕЗА И ЕГО СОЕДИНЕНИЯ … … … … … … … … … … … … … … … … … … … … … 13
d-ЭЛЕМЕНТЫ VII В-ГРУППЫ. МАРГАНЕЦ, ТЕХНЕЦИЙ, РЕНИЙ И ИХ СОЕДИНЕНИЯ … … … … … … … … … … … … … … … … … … … …. …16
d-ЭЛЕМЕНТЫ VI В-ГРУППЫ. ХРОМ, МОЛИБДЕН, ВОЛЬФРАМ И ИХ СОЕДИНЕНИЯ … … … … … … … … … … … … … … … … … … … … … 19
d-ЭЛЕМЕНТЫ V В-ГРУППЫ. ВАНАДИЙ, НИОБИЙ, ТАНТАЛ И ИХ СОЕДИНЕНИЯ … … … … … … … … … … … … … … … … … … … … … 21
d-ЭЛЕМЕНТЫ IV В-ГРУППЫ. ТИТАН, ЦИРКОНИЙ, ГАФНИЙ И ИХ СОЕДИНЕНИЯ … … … … … … … … … … … … … … … … … … … … … 23
d-ЭЛЕМЕНТЫ III В-ГРУППЫ. ЭЛЕМЕНТЫ f–СЕМЕЙСТВА И ИХ СОЕДИНЕНИЯ … … … … … … … … … … … … … … … … … … … … … 25
d-ЭЛЕМЕНТЫ II В-ГРУППЫ. ЦИНК, КАДМИЙ, РТУТЬ И ИХ СОЕДИНЕНИЯ … … … … … … … … … … … … … … … … … … … … … 28
d-ЭЛЕМЕНТЫ I В-ГРУППЫ. МЕДЬ, СЕРЕБРО, ЗОЛОТО И ИХ СОЕДИНЕНИЯ … … … … … … … … … … … … … … … … … … … … … 31
ЛИТЕРАТУРА … … … … … … … … ... … … … … … … … … … … … … . 36
ПРЕДИСЛОВИЕ
Химия d-элементов является основой для изучения последующих дисциплин естественнонаучного цикла, таких как экология, естественнонаучная картина мира, концепции современного естествознания и т.д..
Курс “Химия d-элементов” способствует формированию диалектико-материалистического мировоззрения у будущих молодых бакалавров.
Учебно-методическое руководство к практическим занятиям по химии d-элементов предназначено для студентов профилей “Химия”, “Экология” естественно-географического факультета ВГПУ. Предлагаемое руководство содержит материал по всем изучаемым разделам химии d-элементов:”Комплексные соединения” и “Химия элементов I – VIII групп побочных подгрупп и их соединений”. Методические указания содержат планы практических занятий по химии, вопросы для самостоятельной подготовки по наиболее важным разделам курса, задания для индивидуальной проверки, упражнения и задачи. Этот материал дает ориентацию студентам при теоретической подготовке к практическим занятиям.
В разделе “Вопросы для самостоятельной подготовки” содержится информация, которую необходимо использовать при теоретической подготовке домашних заданий. В “Заданиях для индивидуальной проверки” предложены студентам, в том числе, и внеурочные задания, для того, чтобы подготовка к занятиям была продуктивной, укреплялись умения выполнять упражнения и решать задачи, вырабатывались навыки использования учебной и справочной литературы, и дифференцированно оценивалась самостоятельная работа студента (используя порядковый номер студента в списке, равный номеру индивидуального домашнего задания).
Подборка “Упражнений и задач” должна помочь более глубокому усвоению материала.
Цель практических занятий – углубить и закрепить представления о физических и химических свойствах неорганических веществ, образованных d-элементами, а так же способы получения и применение данных соединений. Привить навыки самостоятельного выполнения эксперимента и обобщения полученных данных. Настоящие методические указания призваны помочь в достижении данной цели.
Компетенции обучающегося, формируемые в результате освоения дисциплины:
Изучение дисциплины “Химия d-элементов” направлено на формирование у обучающихся следующих компетенций.
1. Владеет основными физическими и химическими понятиями, знаниями фундаментальных законов физики и химии, явлений и процессов, изучаемых этими науками:
- знает сущность стехиометрических и газовых законов, понятия и основные положения термодинамики, фазовые равновесия, равновесия в растворах электролитов, понятия и основные закономерности химической кинетики, катализа и электрохимии;
- знает вербальные формулировки и аналитические выражения основных законов, изучаемых в общей химии;
- знает основные методы эмпирических исследований в естественных науках;
- иллюстрирует закономерности примерами, в том числе из человеческой практики;
- умеет использовать справочную химическую и физическую литературу для нахождения и расчёта характеристик изучаемых систем;
- находит необходимые справочные данные, рассчитывает энергетику химических реакций;
- находит и учитывает с целью прогноза направления реакций потенциалы различных химических и электрохимических процессов (потенциалы Гиббса, электродные) в стандартных условиях;
- решает типовые, нестандартные качественные и расчётные задачи;
- владеет современным химическим языком, терминологией и символами;
- использует современную систему наименований веществ, термины и символы, используемые в общей и неорганической химии.
2. Способен выбрать методику экспериментальной работы, обосновать и изложить основы метода, составить план проведения работы, выбрать реактивы, посуду, детали прибора, собрать установку, провести необходимые расчеты:
- знает общие правила проведения эксперимента, общие положения по организации охраны труда и техники безопасности при выполнении конкретных работ, опытов и отдельных операций в химической лаборатории;
- соблюдает правила техники безопасности при работе в химической лаборатории;
- выполняет рекомендации по подготовке рабочего места, оборудования, приборов, реактивов;
- владеет навыками обращения с наиболее широко применяемыми в учебной и исследовательской практике реактивами, материалами, посудой и оборудованием;
- работает с обычной и мерной посудой (колбами, цилиндрами, мензурками, пипетками);
- проводит химический эксперимент на оборудовании, с приборами и посудой рекомендованными для макро- и полумикрометодов работы;
- умеет проводить описанные в практикумах опыты, представлять результаты в табличной, графической формах и диаграммах, давать качественную оценку полученным результатам;
- использует компьютерную графику;
- знает типы и источники экспериментальных ошибок;
- понимает простейшие методики статистической обработки экспериментальных данных.
Задания для индивидуальной проверки
1. В следующих комплексах определите заряд комплексного иона, степень окисления комплексообразователя и его координационное число: K2[Fe(CN)5 NH3]; [CoCl2(en)2]Cl, гдеen –этилендиамин.
2. Дайте названия следующим комплексным соединениям:K3[Fe(CN)6]; [CoCl2 H2O(NH3)3]Cl; [Fe(C5H5)2](NO3)3; [PtCl2(NH3)2].
3. Напишите координационную формулу соединения общей формулы Ba(CN)2 Cu(SCN)2, если известно, что H2SO4осаждает весь барий в виде BaSO4, а изменение электрической проводимости показало, что соединение диссоциирует в воде на два иона.
4. Определите координационное число центрального атома в следующих комплексах: [CoCl3(NH3)3]; K4[Fe(CN)6]; [CrCl2(en)2]Cl; Na2[Zn(OH)4]; K4[TiCl8].
5. Определите степень окисления комплексообразователя в следующих соединениях: K2[SiF6]; K[AuCl4]; Na2[PtCl4]; K3[AsS4]; Ca[PtCl6]; Cu2[Fe(CN)6].Дайте названия этим соединениям.
6. Составьте координационные формулы следующих соединений: а) триамминтринитрокобальт, б) диамминнитротрихлорплатина, в) нитрат пентаамминтиоцианатокобальта (III), г) бромид гексаамминосмия (IV), д) гексацианокобальтат (III) гексаамминкобальта (III), е) тетрахлороплатинат (II) тетраамминдигидроксоплатины (IV).
7. Определите дентатность следующих полидентатных лигандов в комплексных соединениях меди, платины и хрома, если координационные числа меди и платины равны 4, а хрома 6: [Cu(dipy)2]Cl2; K[Cr(edita)]; [Pt(en)2]Br2; [Cu(dipy)C2O4]; [Cr C2O4(NH3)4]Cl; [Pt(gly)2].
8. Определить величину и знак заряда комплексных ионов. Составить формулы комплексных соединений с приведенными катионом или анионом: а) [Bi+3J4]; б) [Cr+3(NH3)5Cl]; в) [Pd+2(NH3)2(CN)2]; г) [Hg+2(SCN)4]; д) [Cr+3(H2O)4Cl2]; е) [Co+3(NH3)2(NO2)4]; ж) [Zr+4(OH)6]; з) [Fe+3(H2O)5Br].
9. Написать координационные формулы следующих комплексных соединений, обосновать выбор комплексообразователя: а) 3NaF · AlF3; б) 2 Ca(CN)2 · Fe(CN)2; в) 2 NH4Br · CuBr2 · 2 NH3; г) Cd(OH)2 · 4 NH3; д) 2 KNO3 · HNO3 · Au(NO3)3;е) KCl · PtCl4 · NH3; ж) KCN · Co(CN)3 · 2 H2O; з) 2 Ba(OH)2 · Cu(OH)2.
Упражнения и задачи
1. Электрическая проводимость растворов комплексов PtCl4 · 6NH3; PtCl4 · 5NH3; PtCl4 · 4NH3; PtCl4 · 3NH3; PtCl4 · 2NH3; KPtCl5 · NH3; K2PtCl6 уменьшается, достигая нуля для PtCl4 · 2 NH3, и затем снова возрастает. Зная, что электрическая проводимость прямопропорциональна числу ионов, на которые диссоциирует электролит, и что координационное число платины в этих комплексах равно 6, напишите их координационные формулы. Назовите данные комплексы. Определите степень окисления комплексообразователя одного из них.
2. Дайте название, определите степень окисления комплексообразователя, заряд иона, класс комплексного соединения (NH4)2[CuSO4(OH)2], [Co(H2O)3(NH3)3](OH)3, NH4[Cr(CNS)4(NH3)2], K[PtCl2BrSO4NH3].
3. Дайте названия следующим комплексным соединениям: K2[PtBr4]; [PtCl3(NH3)3]Br; [PtCl4(NH3)2]; [Co(NO2)3(NH3)3]; Na3[Fe(CN)5NH3]; [Co(NH3)6][Co(NO2)6]; [Cu(NH3)4][PtCl4]; Na3[Cr(OH)6]; K2[SiF6].
4. При добавлении раствора нитрата серебра к раствору комплексной соли общей формулы CrCl3 · 5 H2O объемом 100 мл и молярной концентрации соли 0,100 моль/л образовался осадок массой 2,87 г. Напишите координационную формулу соли.
5. Напишите графические формулы глицинатов меди и цинка (солей аминоуксусной кислоты). Какой тип комплексных соединений они представляют?
6. При действии нитрата серебра на раствор комплексного соединения общей формулы CoCl3 · 5 NH3 осаждается 2/3 содержащегося в нем хлора. Напишите координационную формулу этого соединения.
Задания для индивидуальной проверки
1. Что определяет направление реакций, протекающих в водных растворах, в сторону образования комплексных ионов? Какое равновесие характеризует их устойчивость?
2.Характеристиками каких процессов являются Кнест и Куст комплекса? Как они связаны между собой? Напишите их выражения для соединений: Na3[Ag(S2O3)2]; K2[Ni(CN)4]; [Cu(NH3)4]SO4.
3. Как по сравнительным значениям Кнест и Куст определяется относительная прочность однотипных комплексных соединений?
4. Можно ли разрушить комплекс [Ag(NH3)2]+, концентрация которого в растворе составляет 0,1 моль/л добавлением раствора KСl равного объема и равной концентрации? Увеличение объема раствора при сливании исходных растворов можно не учитывать.
5. Возможно ли разрушение того же комплекса при тех же условиях, что и в предыдущем задании, но при наличии избытка NH3, концентрация которого в растворе составляет 10 моль/л?
6. Приведите примеры разрушения комплекса и осаждения иона комплексообразователя. Чем должен определяться выбор осадителя? В каких случаях он должен использоваться в больших концентрациях?
7. Какое влияние на возможность разрушения комплекса имеют величины комплекса Кнест и ПР осаждаемого соединения, а также наличие в растворе лигандов?
8. Равновесные концентрации ионов Ag+ и молекулы NH3в растворе аммиаката серебра соответственно равны 3,0 · 10 – 4; 5,0 · 10 – 3 моль/л. Найдите концентрацию самого комплекса в этом растворе (Кнест = 6,8 · 10 – 8).
9. Найдите концентрацию Ag+- и CNS¯-ионов в растворе дитиоцианатоаргентата (I) калия с С = 0,10 моль/л, если для него Кнест = 2,7 · 10–8. Как она изменится для ионов серебра после введения в раствор тиоцианата калия до концентрации равной: 1,0 моль/л, 10 моль/л.
10. Чему равна концентрации ионов серебра в растворе дисульфитоаргентата (I) натрия концентрации 1,0 моль/л, если он содержит сульфит натрия количеством вещества 0,010 моль на каждый литр раствора. (Кнест[Ag(SO3)2])=4,5·10–8)?
11. Определите концентрацию ионов меди в растворе [Cu(NH3)4]SO4 объемом 1 л и Скомпл. соли = 0,10 моль/л. Раствор содержит 1,0 моль NH3.
12. Какова концентрация ионов меди в растворе K2[Cu(CN)4] объемом 1 л и концентрацией 0,10 моль/л, если принять равной концентрацию цианида в растворе 5,0 моль/л, а степень диссоциации его принять равной 100%?
13. Какое количество ионов Zn2+ находится в растворе объемом 1л и с(K2[Zn(CN)4]) = 0,10 моль/л, в который добавили 0,010 моль KCN, если степень диссоциации последнего равна 85%?
14. Напишите уравнение реакции гидролиза солей цинка как взаимодействие аквакомплекса [Zn(H2O)4]2+ с водой. В какой роли здесь выступает гидратированный ион цинка с точки зрения протолитической теории кислот и оснований?
15. Допишите приведенные ниже уравнения реакций. Укажите к какому типу относится каждая из них и чем определяется ее направленность:
Таблица 1.
| K2[CuCl4] + NH3 → … | Na3[Ag(S2O3)2] + Na2S → … |
| Fe3+ + [Fe(CN)6] 4— → … | [Ni(NH3)6]SO4 + NaOH → Ni(OH)2 + … |
| Fe2+ + [Fe(CN)6] 3— → … | K4[Fe(CN)6] + Cl 2 → … |
| K+ + [Co(NO2)6] 3— → … | [Co(H2O)6]Cl 3 → … |
| Cu(OH)2 + Na2SO4 → [Cu(SO4)4]6— + … | CoSO4 + NaNO2 + CH3COOH → Na3[Co(NO2)6] + NO + … |
Упражнения и задачи
1. К 1 мл раствора соли никеля, содержащему 4,1 мг никеля, прибавлено 20 г цианида калия. Рассчитайте концентрацию ионов [Ni(CN)4]2–, CN–иNi2+ в растворе.
2. Вычислите концентрацию ионов Zn2+ в растворе, 1 л которого содержит 0,020 моль хлорида цинка и 0,10 моль аммиака.
3. В каком растворе концентрация ионов Cd2+ больше: в 0,1 М растворе K2[Cd(CN)4] или в 0,1 М растворе [Cd(NH3)4]SO4?
4. Вычислите концентрацию ионов Hg2+ в 0,10 М растворе тетрахлорогидраргирата (II) калия K2[HgCl4], если Кнест [HgCl4]2– = 6·10–17.
5. Константа нестойкости иона [Ag(CN)2]– составляет 1,4·10–20. Вычислите концентрацию ионов серебра в 0,050 М растворе K[Ag(CN)2], содержащем, кроме того, 0,010 моль KCNв литре раствора.
6. Можно ли осадить ионы Ni2+ из раствора K2[Ni(CN)4] объемом 1 л и с = 0,10 моль/л, содержащего 0,20 моль KCN (α=80%), если добавить 1,0 · 10–4 моль сульфида аммония? При какой минимальной концентрации сульфида аммония начнет выпадать в осадок? (ПР (NiS) = 2 · 10–28).
Задания для индивидуальной проверки
1. С помощью метода валентных связей определите тип гибридизации атомных орбиталей центрального атома в следующих комплексных ионах: [Zn(NH3)4]2+; [CoF6]3-; [Co(CN)6]3-. Известно, что 1 и 3 – диамагнитные комплексы, а 2 – парамагнитный.
2. Хром образует ряд комплексных соединений: [Cr(H2O)5Cl]Cl2 · H2O; [Cr(H2O)6]Cl3; [Cr(NH3)6][Co(CN)6]; [Co(NH3)6][Cr(CN)6];. Какие из них являются изомерами? Какие типы изомерии здесь представлены?
3. Определите структуру двух изомеров общей формулы Co(NH3)5SO4Br, если известно, что при действии на первый изомер нитрата серебра образуется осадок, а на второй – нет; с первым хлорид бария не образует осадка, а со вторым образует. Измерение электрической проводимости показало, что каждый изомер в растворе диссоциирует на два иона. Назовите данный вид изомерии.
4. Два аммиаката кобальта различаются цветом: один из них – зеленый, другой – фиолетовый. Измерение электрической проводимости показало, что оба изомера диссоциируют в растворе на два иона. Определите вид изомерии. Напишите схемы пространственного строения изомеров, общая формула которых CoCl3 · 4 NH3.
5. Напишите структурные формулы изомеров, в виде которых может существовать глицинат меди (II).
6. Какой тип гибридизации атомных орбиталей центрального атома может иметь место в следующих комплексных ионах [Cu(CN)4]2-; [Cu(NH3)2]1+; [AgBr2]1-; [AuCl4]1-; [Au(CN)2]1-. Укажите электронные конфигурации атомов-комплексообразователей в данных комплексах.
7. За счет каких орбиталей центрального атома происходит образование σ–связей в следующих комплексных ионах: [Mn(CN)6]3- и[ Mn(NH3)6]3+, если известно, что первый – низкоспиновый, а второй – высокоспиновый? К какому из них относится название “внешнеорбитальный” и “внутриорбитальный”?
8. Пользуясь таблицей констант нестойкости, определите, в каких случаях произойдет взаимодействие между растворами электролитов. Напишите для этих случаев молекулярные и ионные формы уравнения.
а) [Cu(NH3)4](NO3)2 + KCN → …;
б) [Ag(NH3)2]Cl + K2S2O3 → …;
в) K2[Cu(CN)4] + Hg(NO3)2 → ….
9. Напишите электронную конфигурацию центрального атома в комплексных ионах:[Fe(CN)6]3-и[Fe(CN)6]4-. За счет каких орбиталей будут образовываться σ–связи с лигандами в первом парамагнитном и во втором диамагнитном комплексе?
Упражнения и задачи
1. Пользуясь таблицей констант нестойкости, определите, в каких случаях произойдет взаимодействие между растворами электролитов. Напишите для этих случаев молекулярные и ионные формы уравнения.
а) [Ag(NH3)2]NO3 + NaNO2 → …;
б) K2[HgBr4] + KCN → …;
в) [Cd(NH3)4]Cl2 + KCN → ….
2. Вычислите концентрацию ионов Cu+ в 1 М растворе тетрацианокупрата (I) калия.
3. Пользуясь таблицей констант нестойкости, определите, в каких случаях произойдет взаимодействие между растворами электролитов. Напишите для этих случаев молекулярные и ионные формы уравнения.
а) K2[HgBr4] + KI → …;
б) K[Ag(CN)2] + NH3 → …;
в) Na3[Ag(S2O3)2] + KCN → ….
4. Какова электронная конфигурация кобальта в следующих комплексных ионах: [Co(C2O4)3]3-; [Co(NH3)6]3+; [CoF6]3-. Известно, что 1 и 3 комплексные ионы – парамагнитны, а 2 – диамагнитен.
5. Определите гибридные орбитали центрального иона и геометрическую структуру комплексов, укажите, какой из комплексов «внутриорбитальный», а какой «внешнеорбитальный»:
а) [Co(NH3)6]3+, - диамагнитный;
б) [Fe(CN)6]3–, - один неспаренный электрон;
в) [Pt(NH3)4]2+, - диамагнитный.
6.Укажите тип гибридизации орбиталей центрального атома и его электронную конфигурацию в следующих комплексах: [AuBr4]1-; [NiCl4]2-; [Co(CN)6]3-, если известно, что первый имеет квадратную форму, второй – тетраэдрическую, а третий – октаэдрическую.
d-ЭЛЕМЕНТЫ VIII В-ГРУППЫ.
СЕМЕЙСТВО ЖЕЛЕЗА И ЕГО СОЕДИНЕНИЯ
Вопросы для самостоятельной подготовки
1. Особенности электронного строения атомов элементов семейства железа. Горизонтальное сходство.
2. Основные степени окисления элементов семейства железа.
3. Характеристика химических свойств железа (простого вещества) и его соединений в разных степенях окисления с точки зрения кислотно-основных и окислительно-восстановительных свойств.
4. Характеристика химических свойств никеля и кобальта и их соединений.
5. Сравнение химических свойств железа, кобальта и никеля.
6. Способы получения и способы очистки железа, кобальта, никеля. Как можно получить химически чистое железо?
7. Применение металлов семейства железа и их соединений.
Задания для индивидуальной проверки
1. К какому классу соединений относится Fe3O4? Напишите графическую формулу.
2. Какие свойства проявляют соединения железа (II) в окислительно-восстановительных реакциях? В какой среде они ярче выражены? Напишите соответствующие уравнения реакций.
3. Какие степени окисления возможны и характерны для железа, кобальта и никеля? Приведите примеры соединений.
4. В одинаковой ли степени выражены основные свойства оксида и гидроксида железа (II) и (III)? Чем это объясняется и как влияет на степень гидролиза солей?
5. Растворы FeCl3за счет гидролиза имеют желто-коричневую окраску. Почему при нагревании раствора окраска становится более темной и, наоборот, светлеет при добавлении кислот?
6. Получите феррит NaFeO2 сплавлением: Fe2O3с Na2CO3, Fe(OH)3 с NaOH. Возможны ли аналогичные реакции для соединений железа (II)?
7. Уравнениями реакций покажите, как проходит взаимодействие FeCl3 со щелочью в растворе и в расплаве.
8. Какие две реакции обычно используют для открытия иона Fe3+? Напишите в молекулярной и ионно-молекулярной формах уравнения реакций получения турнбулевой сини и берлинской лазури. Какое практическое значение имеют эти реакции?
9. Как из K4[Fe(CN)6] получить гексацианоферрат (II) водорода (железисто-синеродистую кислоту) H4[Fe(CN)6], которая хорошо растворяется в воде. Почему эта кислота является сильной в отличие от слабой синильной кислоты HCN?
10. Безводные соли никеля имеют желтую окраску, а их растворы – зеленую, которая сменяется синей при добавлении гидрата аммиака. Чем объяснить эти изменения?
11. При нагревании смеси оксидов никеля (II) и железа (III) образуется феррит никеля. Напишите уравнение данной реакции. Составьте аналогичные уравнения для оксидов двух- и трехвалентного железа.
12. Напишите формулы соединений переходного ряда от [Co(NH3)6]Cl3 к K3[Co(NO2)6], последовательно замещая внутреннюю сферу комплекса нитрит-ионами. Какой представитель этого ряда обладает наименьшей молекулярной электропроводимостью? Для каких представителей этого ряда принципиально возможно существование геометрических изомеров?
13. Какие соединения образуют железо, кобальт и никель с оксидом углерода (II)? Как объяснить различный состав этих соединений, исходя из электронных структур незаряженных атомов Fe, Co и Ni?
14. Сульфат железа (III) восстанавливается гидроксиламином, который окисляется при этом в оксид азота (II). Побочный продукт реакции – сульфат гидроксиламина. Напишите уравнение реакции.
15. Что происходит при добавлении раствора Na2CO3: а) к сульфату железа (II) и б) к сульфату железа (III); чем вызывается различие в характере образующихся продуктов реакций? Напишите уравнения реакций?
16. К раствору, содержащему 4,42 г сульфатов железа и алюминия, прибавили избыток раствора едкого натра. Осадок отфильтровали и прокалили. Масса его оказалась равной 0,40 г. Определите массовую долю сульфатов во взятом растворе.
17. Сколько миллилитров 6,00%-ного раствора KBrO3 (ρ = 1,04 г/мл) потребуется для окисления в сернокислом растворе 50,0 мл 0,75 М раствора FeSO4.
18. Чем отличается сульфиды кобальта (II) и никеля (II) от сульфида железа (II) по растворимости в кислотах и как это используется в аналитической химии?
19. Закончите уравнения следующих реакций:
Fe2O3 + KNO3 + KOH → …;
Fe2O3 + KClO3 + KOH → …;
K4[Fe(CN)6] + K2Cr2O7 + H2SO4 → …;
K3[Fe(CN)6] + SnCl2 + HCl → …;
K4[Fe(CN)6] + H2O2 + H2SO4 → …;
K3[Fe(CN)6] + H2O2 + KOH → O2 + …;
K4[Fe(CN)6] +J2 + … → …; (при рН ≈ 8)
K3[Fe(CN)6] + KJ + … → …. (при рН ≈ 1)
Упражнения и задачи
1. Серный колчедан дает в среднем 70% колчеданного огарка, содержащего 2,0% невыгоревшей серы. Определите, какую массу серной кислоты теряет завод ежесуточно из-за неполного выгорания серы, если производственная мощность печей составляет 80 т колчедана в сутки?
2. Вычислите, какие объемы 39,0%-ного раствора HCl(ρ = 1,19 г/мл), и 75,0%-ной азотной кислоты (ρ = 1,445 г/мл), теоретически необходимы для перевода 100 г платины в гексахлороплатинат (IV) водорода, если исходить из предположения, что продуктом восстановления азотной кислоты является эквимолярная смесь NO и NO2? Какова масса образовавшейся H2[PtCl6] · 6 H2O?
3. Образец железной проволоки массой 0,210 г растворен в H2SO4 без доступа воздуха. На окислении полученного сульфата железа (II) израсходовано 33,6 мл раствора KMnO4 с Сэкв = 0,1103 моль(экв)/л. Определите процентное содержание железа в проволоке.
4. Смесь железа и меди обработали концентрированной HNO3. Остаток отфильтровали, промыли водой, высушили, а затем прохлорировали. Получилось 16,25 г хлорида. Фильтрат выпарили, получившуюся соль высушили и прокалили. Масса остатка после прокаливания составила 15,90 г. Определите количественный состав металлов, а также массу оксида марганца (IV) и массу 36,0% HCl, требующихся для получения хлора, если на реакцию расходуется 50,0% полученного хлора.
5. Что происходит со взвесью малорастворимого карбоната железа (II) в воде: а) при насыщении ее оксидом углерода (IV), б) при стоянии на воздухе? Напишите уравнения реакций.
6. Почему при разбавлении водой синий раствор тетратиоцианата кобальта (II) становится розовым? При каких условиях он снова приобретает синий цвет?
d-ЭЛЕМЕНТЫ VII В-ГРУППЫ.
МАРГАНЕЦ, ТЕХНЕЦИЙ, РЕНИЙ И ИХ СОЕДИНЕНИЯ
Вопросы для самостоятельной подготовки
1. Напишите электронную формулу атома марганца. За счёт каких орбиталей марганец образует химические связи?
2. Какова максимальная валентность марганца? Какие степени окисления проявляет марганец в соединениях? Какие из них наиболее характерны? Приведите примеры соединений в различных степенях окисления и дайте им названия.
3. Какое положение в ряду напряжений занимают Mn, Tc, Re? Как это определяет их отношение к кислотам?
4. Как изменяется характер оксидов и гидроксидов. Дайте объяснение.
5. Какие из соединений марганца в химических реакциях играют роль: а) только восстановителя, б) только окислителя, в) и окислителя, и восстановителя? Дайте объяснения.
6. От каких факторов зависит состав продуктов восстановления перманганата калия, если реакция протекает в растворе? Напишите уравнения реакций.
Задания для индивидуальной проверки
1. Какое соединение марганца зеленого цвета можно получить сплавлением Mn(OH)2, MnO2или MnSO4 со смесью KOHи KClO3? Почему и как изменяется окраска полученного соединения после обработки его хлором?
2. На какие продукты разлагается благодаря своей непрочности марганцовистая кислота H2MnO4? К какому типу относится эта реакция.
3. Одинаковый ли продукт образуется при сплавлении MnO2 с Ca(OH)2 или смесью Ca(OH)2 и NaNO3? Покажите уравнениями реакций.
4. Как из минерала пиролюзита получают марганец и перманганат калия?
5. Какое соединение можно получить действием PbO2 на MnSO4, MnO2 в присутствии азотной кислоты? Почему в этой реакции менее удобно пользоваться серной кислотой?
6. Как из KMnO4 получить Mn2O7? Покажите свойства этого оксида уравнениями соответствующих реакций.
7. Как в лабораториях используют KMnO4 для получения кислорода? Предложите способ превращения оставшейся после реакции смеси снова в KMnO4.
8. В водном растворе между MnSO4 иKMnO4возможна реакция обратного диспропорционирования. Какое соединение марганца является в этом случае продуктом реакции, и по какому признаку оно обнаруживается?
9. По каким внешним признакам можно определить, в какой среде проходила реакция восстановления KMnO4? Приведите примеры таких реакций и напишите их уравнения. Чему равна молярная масса эквивалента KMnO4 в каждом из этих случаев?
10. Почему комплексы [MnCl6]2- и [MnCl6]3- имеют одинаковые магнитные свойства? Каким типом гибридизации орбиталей центральных атомов определяется геометрическая форма этих ионов?
11. Является ли аквакомплекс марганца (II) внутри- или внешнеорбитальным? Проявляет ли он в этом отношении сходство с аквакомплексом хрома(III)? Одинакова ли геометрическая конфигурация этих комплексов?
12. Комплекс [Mn(NH3)6]2+ характеризуется большим значением Кнест. Объясните причину уменьшения степени диссоциации комплексного иона в присутствии избытка NH3. Сказывается ли это на величине Кнест. Объясните.
13. Как действуют на марганец разбавленные и концентрированные растворы кислот: HCl, H2SO4, HNO3при комнатной температуре и при нагревании? Напишите уравнения реакций.
14. Закончите уравнения следующих реакций:
Re + HNO3(конц) → HReO4 + …;
NH4ReO4 + H2 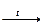 Re + N2 + …;
Re + N2 + …;
TcCl6 + KOH → KTcO4 + TcO2 + …;
MnSO4 + KClO3 + KOH 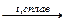 K2 MnO4 + ...;
K2 MnO4 + ...;
CO + KMnO4 + H2SO4кат Ag → …;
Cr2(SO4)3 + KMnO4 + KOH → …;
H2O2 + KMnO4 + H2SO4 → …;
NO2 + KMnO4 + H2O → KNO3 +…;
H3PO3 + KMnO4 + H2SO4 → H3PO4 +…;
MnCl2 + KBrO + KOH → MnO2 +…;
K2MnO4 + Cl2 → …;
K2S + K2MnO4 + H2SO4 → S +….
15. К какому классу соединений относится Mn3O4? Как называется соответствующий минерал?
Упражнения и задачи
1. Определите, какой объем концентрированной соляной кислоты, содержащей 39% HCl(ρ=1,2 г/мл) теоретически необходим для взаимодействия с 0,10 моль KMnO4? Какой объем газа выделится при этом (0°С, 101,3 кПа)?
2. Определите, какая масса йода выделится в сернокислом растворе при взаимодействии раствора KIсо 150 мл 6,00%-ного раствора KMnO4 (ρ = 1,04 г/мл)?
3. Выделение йода из раствора, полученного после выщелачивания золы морских водорослей, производится путем добавления двуокиси марганца и серной кислоты. Определите, какие массы MnO2 и раствора, содержащего 4,5% KI, требуются для получения 1т йода?
4. Вычислите, какой объем H2S (7°С, 96,0 кПа) следует пропустить через 400 мл 6,00%-ного раствора KMnO4 (ρ = 1,04 г/мл), подкисленного серной кислотой, до полного восстановления KMnO4?
5. Для восстановления 80,0 мл раствора KMnO4 (С = 0,0200 моль/л) оказалось достаточным пропустить через раствор 17,9 л газа (0°С, 101,3 кПа), содержащего SO2 и не содержащего других восстановителей. Вычислите массовую долю SO2 в газе.
6. Определите, какую массу FeSO4 · 7 H2O можно окислить в растворе серной кислоты при действии 40 мл раствора KMnO4 (Сэкв = 0,12 моль(экв)/л)?
7. Найдите молярную концентрацию эквивалента для раствора перманганата калия по следующим данным: 20 мл раствора KMnO4 затрачено на титрование раствора щавелевой кислоты, взятого объемом 25 мл. Раствор кислоты был приготовлен в мерной колбе на 100 мл из навески H2C2O4 · 2 H2O массой 0,063 г.
8. Рассчитайте массовую долю H2O2 в растворе (ρ=1,136 г/мл), если при действии перманганата калия на раствор пероксида водорода объемом 100,0 мл выдел
