Порядок выполнения работы. 1. Приготовить 100 мл насыщенного раствора среднерастворимого электролита Ва(ОН)2
1. Приготовить 100 мл насыщенного раствора среднерастворимого электролита Ва(ОН)2, Са(ОН)2, СаСrO4, CaSO4, PbCl2, по заданию преподавателя, а также растворы сильных электролитов KCl, NaCl различной концентрации и электролитов с одноименным ионом по отношению к среднерастворимому электролиту по заданию преподавателя. Значения произведения растворимости, для расчета насыщенной концентрации приведены в таблице 1.
Таблица 1 Произведение растворимости
| Соль | Ва(ОН)2 | Са(ОН)2 | СаСrO4 | CaSO4 | PbCl2 |
| ПР | 5*10-3 | 5,5*10-6 | 7,1*10-4 | 9,1*10-6 | 1,6*10-5 |
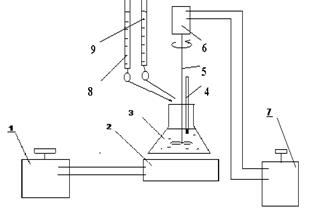
Рисунок 2 Экспериментальная установка для изучения солевого эффекта
2. Поместить раствор в колбу и приливать из бюретки при постоянном помешивании заданный объем электролита с одноименным ионом (желательно анионом).
3. Дождаться созревания осадка (примерно 3-5 мин) и отфильтровать раствор, содержащийся в колбе, через вакуумный фильтр. Оставшийся в колбе осадок смыть на фильтр маточным раствором. Осадок просушить в муфельной печи и взвесить. Результат записать в таблицу 2.
4. Залить в колбу новую порцию электролита и повторить опыт по п.2-3 варьируя количество электролита с одноименным ионом в пределах и с шагом по заданию преподавателя.
5. Повторить исследование с применением нового среднерастворимого электролита.
6. По завершении опытов по высаливанию растворов приготовить насыщенные растворы вышеуказанных солей и изучить влияние сильных электролитов.
7. В колбу со среднерастворимым электролитом добавить навеску того же сухого электролита и приливать из бюретки при постоянном помешивании заданный объем сильного электролита.
8. Дождаться равновесного растворения осадка среднерастворимого электролита и отфильтровать раствор, содержащийся в колбе, через вакуумный фильтр. Оставшийся в колбе осадок смыть на фильтр маточным раствором. Осадок просушить в муфельной печи и взвесить. Результат записать в таблицу 3.
9. Залить в колбу новую порцию электролита и повторить опыт по п.7-8 варьируя количество сильного электролита в пределах и с шагом по заданию преподавателя.
4. Обработка экспериментальных данных, содержание отчета
Обработка результатов опытов по изучению влияния электролитов с одноименным анионом по отношению к среднерастворимому электролиту на растворимость среднерастворимого электролита.
1. Рассчитать массу среднерастворимого электролита для приготовления насыщенного раствора по формуле:
М KtnAnm = ( (n+m) Ö ( ПР KtnAnm / nn * mm ) ) * Mr KtnAnm * Vр-ра (1)
где: ПР KtnAnm – произведение растворимости электролита KtnAnm
n, m – количество катиона и аниона в молекуле электролита
Mr KtnAnm – молекулярная масса электролита
Vр-ра – объем раствора, который необходимо приготовить, л
2. Рассчитать массу электролита оставшегося в растворе ( Мр-р ) как разницу между массой растворенного электролита и электролита, выпавшего в осадок. Рассчитать практическую растворимость среднерастворимого электролита (Ссред. эл. практ ) в присутствии электролита с одноименным анионом как отношение массы вещества, оставшегося в растворе к объему раствора в колбе.
3. Рассчитать мольную концентрацию электролита с одноименным ионом в колбе по формуле:
С‘эл. = V эл. * C эл / (Vсред. эл. + V эл. ) (2)
где: V эл. – объем электролита, прилитого из бюретки, л
Cэл - концентрация электролита в бюретке, моль / л
Vсред. эл. – объем среднерастворимого электролита в колбе, л
4. Построить график зависимости растворимости среднерастворимого электролита в присутствии электролита с одноименным анионом от мольной концентрации электролита с одноименным анионом.
5. Рассчитать произведение растворимости, так как это описано в примере 1.2 ПР’. Используя новое значение произведение растворимости рассчитать теоретическую растворимость в присутствии электролита с одноименным анионом Ссред. эл. теор.. Найти отклонение практической растворимости от теоретической. Результаты записывать в таблицу 2.
Таблица 2
Результаты исследования влияния электролитов с одноименным анионом по отношению к среднерастворимому электролиту на растворимость среднерастворимого электролита.
| среднерастворимый электролит | М KtnAnm , г | V эл, л | Мр-р, г | Ссред. эл. практ , г/л | Ссред. эл. теор. , г/л | С‘эл. , моль/л | ПР’ |
Обработка результатов опытов по изучению влияния сильных электролитов на растворимость среднерастворимого электролита.
6. Рассчитать массу электролита перешедшего из осадка в раствор как разницу масс осадка до приливания сильного электролита и после приливания. Масса среднерастворимого электролита в растворе найти как сумму электролита уже имевшегося в растворе и перешедшего в раствор после приливания сильного электролита.
7. Рассчитать растворимость среднерастворимого электролита как отношение массы электролита в растворе к объему раствора в колбе после приливания сильного электролита Ссред. эл. прак.
8. Рассчитать мольную концентрацию сильного электролита в колбе по формуле:
С‘сил. эл. = V сил. эл. * C сил. эл / (Vсред. эл. + V сил. эл. ) (2)
где: V сил. эл. – объем электролита, прилитого из бюретки, л
Cсил. эл - концентрация электролита в бюретке, моль / л
Vсред. эл. – объем среднерастворимого электролита в колбе, л
9. Построить график зависимости растворимости среднерастворимого электролита в присутствии сильного электролита от мольной концентрации сильного электролита.
10. Рассчитать ионную силу раствора m и произведение растворимости ПР’, так как это описано в примере 1.3. Используя новое значение произведение растворимости рассчитать теоретическую растворимость в присутствии сильного электролита. Найти отклонение практической растворимости от теоретической. Результаты записать в таблицу 3.
11. Используя математический пакет корреляционно-регрессионного анализа построить математическую модель процесса высаливания как зависимость вида Ссред. элпракт. = f (T, С‘эл.)
Таблица 3
Результаты исследования влияния сильных электролитов на растворимость среднерастворимого электролита.
| среднерастворимый электролит | М KtnAnm , г | V эл, л | Мр-р, г | Ссред.эл.практ , г/л | Ссред. эл. теор. , г/л | С‘сил. эл. , моль/л | m | ПР’ |
Контрольные вопросы:
- Что такое солевой эффект ?
- Приведите примеры солевого эффекта ?
- Как объясняется солевой эффект с точки зрения теории электролитов ?
- Как объясняется солевой эффект с точки зрения произведения растворимости ?
- Как рассчитать растворимость вещества в чистой воде, зная произведение растворимости ?
- Как рассчитать растворимость вещества в присутствии сильного электролита без учета активности ?
- Как рассчитать растворимость вещества в присутствии сильного электролита с учетом активности ?
- Выпадет ли осадок при приливании к насыщенному раствору Са(ОН)2 раствора КОН ? Будут ли протекать при этом химические реакции и какие?
- Какие закономерности были получены в ходе исследования и сделаны выводы ?
