Тема 02. Электрохимические системы
Раздел 3. Химические системы
ОК-15 умеет использовать фундаментальные законы природы, законы химии в процессе профессиональной деятельности
БЛОК А
Тема 01. Растворы и дисперсные системы
ОК-15 [3.1.1]
Выбор
Растворами называют …
в- гетерогенные системы, состоящие из нескольких компонентов.
в- гомогенные системы, изолированные от окружающей среды.
в+ гомогенные системы, состоящие из 2-х или более компонентов и продуктов их взаимодействия.
в- гомогенные системы, образующиеся в результате установления химического равновесия между 2-мя реагирующими веществами.
ОК-15 [3.1.2]
Выбор
Концентрация - это количественная мера…
в- описания состава раствора.
в- содержания растворенных веществ в растворе.
в+ содержания растворенного вещества в растворе.
в- описания способа приготовления раствора.
ОК-15 [3.1.3]
Выбор
Математическое выражение закона Рауля для растворов неэлектролитов…
а) в- 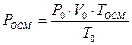 .
.
б) в- 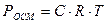 .
.
в) в+ 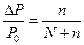 .
.
г) в- 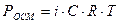 .
.
ОК-15 [3.1.4]
Соответствие
Установите соответствие между веществом и соответствующей дисперсной системой
С1 молоко
О1 эмульсия
С2 цементный раствор
О2 суспензия
С3 табачный дым
О3 аэрозоль
О4 дисперсия
ОК-15 [3.1.5]
Выбор
Коллоидные растворы отличаются от истинных растворов … частиц…
в+ бόльшими размерами
в- различной фазой
в- природой
в- меньшими размерами
ОК-15 [3.1.6]
Выбор
Закон Рауля: при постоянной температуре относительное понижение давления насыщенного пара растворителя над раствором равно …
в- массовой доле растворенного вещества.
в- молярной концентрации растворенного вещества.
в- моляльной концентрации растворенного вещества.
в+ мольной доле растворенного вещества.
ОК-15 [3.1.7]
Выбор
Понижение температуры замерзания раствора прямопропорционально…
в- массовой доле растворенного вещества.
в- молярной концентрации растворенного вещества.
в+ моляльной концентрации растворенного вещества.
в- мольной доле растворенного вещества.
ОК-15 [3.1.8]
Выбор
Осмосом называют процесс…
в- диффузии вещества при растворении.
в- самопроизвольного переноса вещества через полупроницаемую мембрану.
в+ самопроизвольного переноса растворителя через полупроницаемую мембрану.
в- самопроизвольного перемешивания раствора.
ОК-15 [3.1.9]
Соответствие
Установите соответствие между способом выражения концентрации и формулой
С1 молярная концентрация
О1 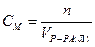
С2 нормальная концентрация
О2 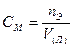
С3 массовая доля вещества
О3 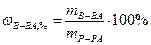
С4 мольная доля
О4 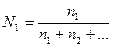
С5 моляльная концентрация
О5 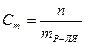
О6 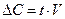
ОК-15 [3.1.10]
Выбор
Показатель кислотности рН раствора вычисляется по формуле…
в- 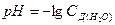 .
.
в- 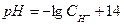 .
.
в+ 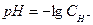 .
.
в- 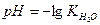 .
.
ОК-15 [3.1.11]
Выбор
Значения рН щелочного раствора…
в- рН < 7.
в- рН = 7.
в+ рН > 7.
в- не имеет рН.
ОК-15 [3.1.12]
Выбор
На величину степени электролитической диссоциации влияют:
в+ температура.
в+ концентрация раствора.
в+ природа растворителя.
в- объем сосуда.
в- цвет вещества.
в+ природа вещества.
ОК-15 [3.1.13]
Выбор
Законы теории растворов применимы к растворам электролитов только при использовании поправочного изотонического коэффициента, потому что…
в- электролиты изменяют электропроводность раствора.
в- электролиты при растворении связывают большее число молекул воды и уменьшают общее число частиц в растворе.
в+ электролиты при растворении диссоциируют на ионы и увеличивают число частиц в растворе.
в- электролиты изменяют структуру воды.
ОК-15 [3.1.14]
Выбор
Ионное произведение воды имеет при 298К значение…
в- 6,2×10-8.
в+ 1×10-14.
в- 1,8×10-16.
в- 14.
в- 16.
ОК-15 [3.1.15]
Соответствие
Соответствие между степенью диссоциации веществ и силой электролита
С1 Na2SO4 ( 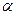 = 90%)
= 90%)
О1 сильный
С2 H2SO3 ( 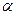 = 25%)
= 25%)
О2 средний
С3 CH3COOH ( 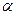 = 2,5%)
= 2,5%)
О3 слабый
С4 C12H22O11 ( 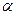 = 0%)
= 0%)
О4 неэлектролит
О5 высококипящее соединение
ОК-15 [3.1.16]
Выбор
Система, в которой твердое вещество распределено в жидкой дисперсионной среде, называется …
в- эмульсия
в- коллоид
в- пена
в+ суспензия
ОК-15 [3.1.17]
Выбор
К электролитам относятся:
в- металлы.
в- неметаллы.
в- оксиды металлов.
в+ основания.
в- оксиды неметаллов.
в+ кислоты.
в+ соли.
в- все органические вещества.
Тема 02. Электрохимические системы
ОК-15 [3.2.1]
Выбор
Стандартным электродным потенциалом называется …
в- потенциал, установившийся на границе металл-раствор при погружении металла в раствор собственной соли с концентрацией ионов металла 1 моль/л.
в- потенциал, установившийся на границе металл-раствор при погружении металла в раствор собственной соли, и измеренный с помощью вольтметра.
в+ потенциал металла, погруженного в раствор собственной соли с концентрацией ионов металла 1 моль/л, и измеренный относительно стандартного водородного электрода при стандартных условиях.
в- потенциал, вычисленный по уравнению Нернста при стандартных условиях.
ОК-15 [3.2.2]
Выбор
Более активными, чем водород, являются металлы, стандартный электродный потенциал 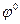 которых…
которых…
в- более положителен, чем у водорода.
в+ более отрицателен, чем у водорода.
в- совпадает с потенциалом водорода.
в- больше, чем потенциал других металлов.
ОК-15 [3.2.3]
Выбор
Величина электродного потенциала зависит от:
в+ природы металла.
в- атмосферного давления.
в+ концентрации ионов металла в растворе.
в+ температуры.
в- величины числа Фарадея.
ОК-15 [3.2.4]
Выбор
Гальваническим элементом называется ….
в- устройство для пропускания электрического тока через раствор или расплав веществ.
в+ устройство для превращения энергии окислительно-восстановительных реакций в электрическую энергию.
в- устройство для превращения энергии электрического тока в химическую энергию.
в- устройство для превращения энергии, выделяющейся при осуществлении реакции нейтрализации, в электрическую энергию.
ОК-15 [3.2.5]
Выбор
Анод гальванического элемента …
в- заряжен положительно.
в+ заряжен отрицательно.
в- нейтрален.
в- знак заряда изменяется при работе элемента.
ОК-15 [3.2.6]
Выбор
Никель ( 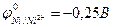 ) будет катодом гальванического элемента в паре с…
) будет катодом гальванического элемента в паре с…
в+ кадмием ( 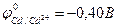 ).
).
в- медью ( 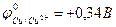 ).
).
в- свинцом ( 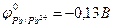 ).
).
в- серебром ( 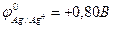 ).
).
ОК-15 [3.2.7]
Выбор
Электродвижущая сила гальванического элемента, составленного из цинка и ртути ( 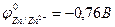 ,
, 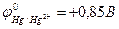 ) , равна…
) , равна…
в- -0,09 В.
в- 0,09 В.
в- 1,52 В.
в+ 1,61 В.
в- 1,7 В.
ОК-15 [3.2.8]
Выбор
Электролизом называется окислительно-восстановительная реакция, …
в- при осуществлении которой возникает электрический ток.
в- протекающая в растворе при пропускании электрического тока.
в+ протекающая на электродах при пропускании электрического тока.
в- при осуществлении которой в растворе образуются катионы и анионы.
ОК-15 [3.2.9]
Выбор
Катод при электролизе…
в- заряжен положительно.
в+ заряжен отрицательно.
в- не имеет заряда.
в- изменяет знак заряда во время электролиза.
ОК-15 [3.2.10]
Выбор
На аноде при электролизе происходит процесс…
в- восстановления.
в+ окисления.
в- нейтрализации.
в- перезарядки.
ОК-15 [3.2.11]
Последовательность
Последовательность восстановления катионов металла на катоде при электролизе
п1+ Au+ ( 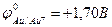 ).
).
п2+ Hg2+ ( 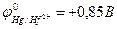 ).
).
п3+ Cu2+ ( 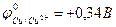 ).
).
п4+ Zn2+ ( 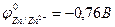 ).
).
ОК-15 [3.2.12]
Выбор
Коррозией называется процесс…
в- гетерогенного превращения металла в окружающей среде.
в+ самопроизвольного разрушения металла, происходящего при взаимодействия с окружающей средой.
в- целенаправленного изменения металла, происходящего при взаимодействия с различными веществами.
в- самопроизвольного восстановления металла, происходящего при взаимодействия с окружающей средой.
ОК-15 [3.2.13]
Выбор
Анодная реакция при коррозии металла в атмосферном воздухе имеет вид…
в+ Me0 – ne = Men+.
в- 2Me0 + O2 + 2H2O = 2Me(OH)2.
в- 2Me0 + O2 = 2MeO.
в- Me0 + 2H+ = Me2+ + H2# .
ОК-15 [3.2.14]
Выбор
Способы защиты от коррозии:
в+ введение ингибиторов.
в+ металлические покрытия.
в- введение катализаторов.
в+ катодная защита.
в+ лакокрасочные покрытия.
в- нагревание металла.
ОК-15 [3.2.15]
Выбор
Анодным покрытием для железа ( 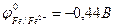 ) может служить…
) может служить…
в+ цинк ( 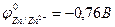 ).
).
в- свинец ( 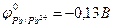 ).
).
в- медь ( 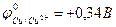 ).
).
в- серебро ( 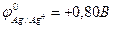 ).
).
ОК-15 [3.2.16]
Выбор
Металлом, который нельзя получить электролизом водного раствора его соли, является…
в- Ag( 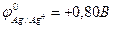 )
)
в- Ni ( 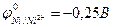 )
)
в- Cu( 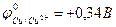 )
)
в+ Na ( 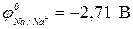 ).
).
ОК-15 [3.2.17]
Выбор
Протекторная защита корпуса стальной цистерны ( 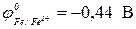 ) может быть осуществлена с помощью:
) может быть осуществлена с помощью:
в- свинца ( 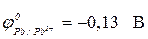 )
)
в+ марганца ( 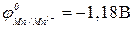 )
)
в+ цинка ( 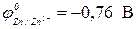 )
)
в- никеля ( 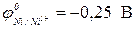 )
)
ОК-15 [3.2.18]
Выбор
Продуктами коррозии оцинкованного железа при повреждении покрытия в кислой среде (раствор HCl) будут ( 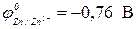 ,
, 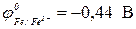 )…
)…
в- Zn и H2
в+ ZnCl2 и H2
в- ZnCl2 и FeCl2
в- FeCl2 и H2
ОК-15 [3.2.19]
Выбор
Катодному процессу при коррозии оцинкованного железа во влажном воздухе при повреждении покрытия соответствует уравнение…
в+ O2 + 2H2O + 4e = 4OH–
в- Fe2+ + 2e = Fe0
в- Zn2+ + 2e = Zn0
в- 2H+ + 2e = H20
ОК-15 [3.2.20]
Выбор
При нарушении цинкового покрытия на железном изделии во влажном воздухе на аноде будет протекать реакция, уравнение которой имеет вид … ( 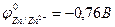 ,
, 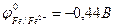 )
)
в- Fe2+ + 2e = Fe0
в- Fe0 – 2e = Fe2+
в+ Zn0 – 2e = Zn2+
в- 2H2O + O2 + 4e = 4OH–
