Проверка домашнего задания. Обобщение и систематизация полученных знаний
Обобщение и систематизация полученных знаний
Выставление оценок
Домашняя работа: Подготовить доклад на тему: Основные приемы фотометрических измерений (метод градуировочного графика, метод молярного свойства и добавок)
СРСП № 28
На тему:Потенциометрия
Цель:
Обучающая– глубокое изучение различных явлений и законов по данной теме
Развивающая – формирование эффективных и устойчивых взаимосвязей между научной и образовательной деятельностью;
Воспитательная – приобщать обучающихся к активности, самостоятельности на занятиях
Ход урока:
1. Организационный этап- 3 минуты
2. Этап подготовки к усвоению материала СРСП -5 минут
3. Проверка домашнего задания- 27 минут
4. Обобщение и систематизация полученныхзнаний - 5 минут
5. Выставление оценок- 5 минут
Метод основан на измерении ЭДС между индикаторным электродом и электродом сравнения: DЕ = Е1 – Е2.
Реальный потенциал, который зависит от температуры, числа электронов, участвующих в электродной реакции, соотношения концентраций окисленной и восстановленной форм, рассчитывают по уравнению Нернста:
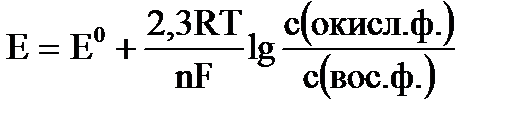 , где
, где
Е0 – стандартный электродный потенциал,
R – универсальная газовая постоянная (8,314 Дж/град),
Т – абсолютная температура (0 0С = 273 К),
n – число электронов,
F – число Фарадея (96500 К).
Рассчитанное значение потенциала по уравнению Нернста относится к водородному электроду сравнения, потенциал которого принят за “0”.
Из-за сложности конструкции водородный электрод не находит практического применения. Поэтому в качестве электродов сравнения применяют хлорсеребряный (+0,22 В) и каломельный (+0,24 В) потенциал которых сохраняет постоянное значение в достаточном интервале температур. Для расчета потенциала индикаторного электрода относительно потенциала электрода сравнения используют соотношение:
Е = Еср + (± Ер)
Пример: Рассчитать значение электродного потенциала процесса восстановления меди (II) до металла при температуре 400С, относительно электрода сравнения (Еср = -0,2 В), если концентрация ионов Cu2+ в растворе составляет
0,001 моль/л, а Е 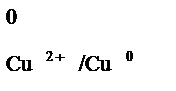 = +0,34 В.
= +0,34 В.
Решение:
Процесс восстановления: Cu2+ + 2ē ® Cu0, значит n = 2, с(ок.ф.) = с(вос.ф.) = 0,001 = 10-3 моль/л, восстановленной формой является Cu0 – твердая фаза, Т = 273 + 40 = 313, тогда:
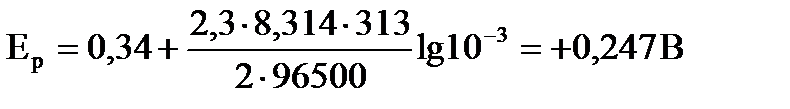
Рассчитаем потенциал относительно потенциала электрода сравнения:
Е = Еср +(± Ер ) = -0,2 +0,247 = +0,047 В.
По данным таблицы 16 выполнить самостоятельно задания.
Таблица 16
Рассчитать значение реального электродного потенциала при заданной температуре и концентрации относительно потенциала электрода сравнения:
