Тема 03. Химическое и фазовое равновесие
ОК-10 [2.3.1]
Выбор
Химическое равновесие - это такое состояние системы, когда…
в- скорость прямой реакции больше скорости обратной реакции.
в- скорость прямой реакции меньше скорости обратной реакции.
в+ скорость прямой реакции равна скорости обратной реакции.
в- реакция необратима.
ОК-10 [2.3.2]
Выбор
Общий вид выражения для константы равновесия системы 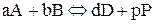 …
…
а) в- 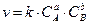 .
.
б) в-  .
.
в) в- 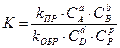 .
.
г) в- 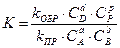 .
.
д) в+ 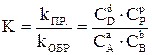 .
.
ОК-10 [2.3.3]
Соответствие
Установите соответствие между воздействием на систему
H2(Г) + S(Т) D H2S(Г); DH < 0
и направлением смещения равновесия.
С1 повышение температуры.
О1 в сторону обратной реакции.
С2 уменьшение концентрации H2S.
О2 в сторону прямой реакции.
С3 увеличение давления.
О3 положение равновесия не изменяется.
О4 сера выпадает в осадок.
ОК-10 [2.3.4]
Выбор
Правило фаз Гиббса…
в+ 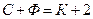 .
.
в-  .
.
в-  .
.
в- 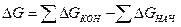 .
.
ОК-10 [2.3.5]
Выбор
Положение химического равновесия зависит от:
в+ температуры.
в+ концентрации реагирующих веществ
в- цвета веществ.
в- перемешивания.
в- катализатора.
в+ давления.
ОК-10 [2.3.6]
Выбор
Смещение положение химического равновесия описывает…
в- закон сохранения массы веществ М.В.Ломоносова.
в+ принцип Ле-Шателье.
в- периодический закон Д.И.Менделеева.
в- правило Вант-Гоффа.
в- уравнение Аррениуса.
в- 1-й закон термодинамики.
ОК-10 [2.3.7]
Выбор
Изменение энергии Гиббса связано с константой равновесия соотношением…
в+  .
.
в- 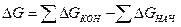 .
.
в-  .
.
в- 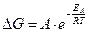 .
.
ОК-10 [2.3.8]
Выбор
Константе равновесия системы CH4(Г) + CO2(Г) D 2CO(Г) + 2H2(Г) соответствует выражение…
в- 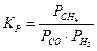 .
.
в+ 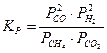 .
.
в- 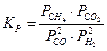 .
.
в- 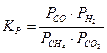 .
.
ОК-10[2.3.9]
Выбор
Принцип Ле-Шателье: если на систему, которая находится в состоянии равновесия, оказать внешнее воздействие, то положение равновесия …
в+ сместится в сторону той реакции, которая ослабляет это воздействие.
в- сместится в сторону той реакции, которая усиливает это воздействие.
в- сместится в сторону прямой реакции.
в- сместится в сторону обратной реакции.
в- система не будет отзываться на оказываемое воздействие.
ОК-10 [2.3.10]
Выбор
Положение равновесия при KP > 1 смещено в сторону реакции…
в+ прямой
в- обратной
в- равновесной
в- обратимой
ОК-10 [2.3.11]
Выбор
Константа равновесия системы CH4(Г) + CO2(Г) D 2CO(Г) + 2H2(Г) …
в- 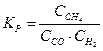 .
.
в- 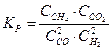 .
.
в+ 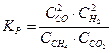 .
.
в- 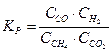 .
.
ОК-10 [2.3.12]
Выбор
Увеличение концентрации NO2 способствует смещению положения равновесия системы 2NO2 D 2NO + O2 …
в- в сторону обратной реакции.
в+ в сторону прямой реакции.
в- не сместит равновесие.
в- уменьшит количество образующихся веществ.
ОК-10 [2.3.13]
Выбор
Увеличение температуры вызовет смещение равновесия системы
N2(Г) + O2(Г) D 2NO(Г); DH = 180 кДж/моль :
в- в сторону обратной реакции.
в+ в сторону прямой реакции.
в- не сместит равновесие.
в+ увеличит количество образующихся веществ.
в- уменьшит количество образующихся веществ.
ОК-10 [2.3.14]
Выбор
Увеличение давления смещает положение равновесия влево в реакциях:
в+ 2NO2(Г) D 2NO(Г) + O2(Г).
в- N2(Г) + O2(Г) D 2NO(Г).
в+ CH4(Г) + CO2(Г) D 2CO(Г) + 2H2(Г).
в- C(Т) + O2(Г) D CO2(Г).
в- O2(Г) + 4HCl(Г) D 2H2O(ПАР) + 2Cl2(Г).
ОК-10 [2.3.15]
Выбор
Уменьшение давления НЕ смещает положение равновесия в реакциях:
в- 2NO2(Г) D 2NO(Г) + O2(Г).
в+ N2(Г) + O2(Г) D 2NO(Г).
в- CH4(Г) + CO2(Г) D 2CO(Г) + 2H2(Г).
в+ C(Т) + O2(Г) D CO2(Г).
в- O2(Г) + 4HCl(Г) D 2H2O(ПАР) + 2Cl2(Г).
ОК-10 [2.3.16]
Выбор
Можно сместить положение равновесия системы N2(Г) + O2(Г) D 2NO(Г); DH >0 в ту же сторону, что и повышение температуры…
в- понижением давления.
в- повышением давления.
в- повышением концентрации NO.
в+ понижением концентрации NO.
