Убыль энергии Гиббса равнa максимальной полезной работе изобарно-изотермического процесса
Лекция № 4. Второе начало термодинамики. Энтропия.
Первый закон термодинамики устанавливает эквивалентность различных видов энергии и форм их передачи. Назначение 2-го закона термодинамики – установление критериев самопроизвольного протекания разнообразных процессов. Закон прошел длительный путь эволюции и сначала был сформулирован как основной закон действия тепловых машин.
1. Теорема Карно (1824) “Размышление о движущей силе огня” – коэффициент полезного действия обратимого цикла, состоящего из 2 изотерм и 2 адиабат, зависит только от разности температур тепловых резервуаров и не зависит от природы рабочего тела
h = (Q1 – Q2 )/Q1 = (T1 –T2)/T1 = 1 – Т2/Т1 . (4.1)
2. Томсон (лорд Кельвин) (1848) ввел понятие абсолютной температуры и (1851) сформулировал 2 закон ТД – невозможно построить периодически действующую тепловую машину, которая только бы черпала тепло из одного резервуара и производила механическую работу, т.е. невозможен вечный двигатель 2-го рода.
3. Клаузиус (1850) дал первую формулировку 2 закона ТД – невозможен самопроизвольный переход теплоты от тела менее нагретого к телу более нагретому. Обе формулировки эквивалентны, одна невозможна без другой. В 1854 г ввел понятие энтропии [S] = Дж/К.
4. Данные формулировки весьма далеки от химии, для решения практических задач в химии используют формулировку второго начала термодинамики, данную Гиббсом: система находится в состоянии равновесия, если ее энтропия при всех возможных изменениях, остается постоянной или уменьшается, т.е.
δS ≤ 0.
В действительности понятия второго закона опираются на молекулярную теорию и имеют статистическийхарактер. Рассмотрим второй закон с этой точки зрения. Статистическая термодинамика начала развиваться с конца XIX века. Основные принципы ее были разработаны в трудах Больцмана, Гиббса, Планка, Эйнштейна, Эренфеста,
Макро- микросостояния системы. Термодинамическая вероятность
Односторонность самопроизвольного протекания процессов является естественным следствием молекулярной природы вещества, из которой, в свою очередь, следует возможность определить состояние системы двумя различными способами.
1 Задаются значения термодинамических параметров (Т, Р, состав и др.), которые являются усредненными, т.е. задается макросостояниесистемы.
2 Задаются координаты и скорости всех составляющих систему частиц, т.е. задается микросостояниесистемы.
Очевидно, что одно и то же макросостояние можно задать большим количеством микросостояний. Число микросостояний, которыми реализуется данное макросостояние, называется термодинамической вероятностью(W). В отличие от математической вероятности, изменяющейся в пределах от нуля до единицы, W ≥ 1. Она является числителем математической вероятности (это отношение числа исходов, благоприятствующих данному событию, к общему числу исходов). Как и математическая вероятность, величина W обладает свойством мультипликативности, т.е. если две системы с термодинамическими
вероятностями W1 и W2 объединяются в одну сложную систему, то для нее W = W1 × W2.
Термодинамическая вероятность – это свойство системы, значит, она не зависит от пути, по которому система пришла в данное состояние. В общем случае, если N частиц, образующих систему, распределены по s состояниям так, что каждому состоянию отвечает
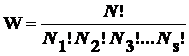
Поскольку в пределах одного какого-либо состояния частицы неразличимы, то из общего числа микросостояний N!, определяемого числом перестановок всех частиц, исключаются перестановки, не задающие новых микросостояний. Из приведенного выражения следует, что значение W тем больше, чем равномернее, а значит, хаотичнее распределение частиц по состояниям. Поэтому термодинамическая вероятность может служить критерием направленности процессов в изолированных системах. С использованием данного понятия можно дать еще одну формулировку второго закона термодинамики (статистическую).
Второй закон: предоставленная самой себе, т.е. изолированная, система переходит из состояния с меньшей термодинамической вероятностью в состояние с большей ее величиной. В состоянии равновесия термодинамическая вероятность максимальна.
Статистический характер второго закона проявляется в том, что он с высокой точностью выполняется лишь для очень большого числа частиц. С уменьшением размеров системы применимость его снижается, поскольку «размываются» границы между более равномерным и менее равномерным распределением частиц (между порядком и беспорядком). Отклонения от равномерного распределения частиц, а, следовательно, и свойств вещества, существуют и в больших системах. Как правило, они кратковременны и (или) сосредоточены в микроскопических объемах. Такие отклонения называются флуктуациями.Их существование в реальных системах показывает, что локальные (во времени и в пространстве) отклонения от второго закона возможны, и закон возрастания термодинамической вероятности выполняется только в среднем для относительно большого промежутка времени. Роль флуктуаций велика при протекании многих процессов, например, при кристаллизации жидкости.
Энтропия
Мы выяснили, что по изменению термодинамической вероятности можно судить о направленности процесса в изолированной системе. Однако на практике использовать этот критерий неудобно по следующим причинам:
а) W принимает очень большие значения;
б) W связана не с термическими характеристиками системы, а с механическими – положениями частиц в пространстве и их скоростями.
В рамках термодинамики необходимо было найти критерий направленности процессов (или равновесия), связанный с термическими величинами. Эту задачу решили, когда введенное одним из основателей термодинамики Р. Клаузиусомпонятие энтропии(S) физик Л. Больцмансвязал с термодинамической вероятностью:
S = klnW. (9)
В этом соотношении k – постоянная Больцмана. Энтропия, как и термодинамическая вероятность, является функцией состояния системы. Она выражается меньшими числами, чем W, и, кроме того, аддитивна:
S1+2 = klnW1+2 = kln(W1W2) = klnW1 + klnW2 = S1 + S2.
Поскольку в изолированной системе в результате самопроизвольного процесса термодинамическая вероятность растет, а при равновесии принимает максимальное значение, то и энтропия ведет себя таким же образом и тоже может служить критерием направленности процессов. Сформулируем второй закон, используя понятие энтропии.
Второй закон: предоставленная самой себе, т.е. изолированная, система переходит из состояния с меньшей энтропией в состояние с большей ее величиной. В состоянии равновесия энтропия системы максимальна.
Энтропия – это количественная характеристика хаотичности системы, или мера беспорядка в ней. Чем хаотичнее расположены частицы, тем больше величины W и S.
Например, при прочих равных условиях можно записать:
Sкристаллической фазы < Sжидкой фазы< Sгазообразной фазы.
Энтропия возрастает в любом процессе, происходящем под влиянием движения частиц, стремящихся к менее упорядоченному распределению в пространстве – расширении газа при уменьшении давления, термическом расширении тел, плавлении, испарении, диссоциации молекул на свободные атомы и др.
Математической записью второго закона термодинамики считают соотношение, которое впервые получил из чисто термодинамических соображений Клаузиус:
ΔS ≥ ∫ (δQ/T)
Здесь знак равенства отвечает обратимому процессу, а знак неравенства – необратимому.
dS = 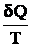
 для обратимых процессов;
для обратимых процессов;
dS > 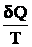 для самопроизвольных процессов.
для самопроизвольных процессов.
dS < 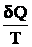 для несамопроизвольных (вынужденных) процессов
для несамопроизвольных (вынужденных) процессов
Заметим, что величина ΔS, как изменение свойства системы, не зависит от пути процесса, в частности от того, обратим он или нет. Теплота же процесса, как и работа, максимальна, если он протекает обратимо, именно этим обусловлен знак неравенства в соотношении (10).
Расчет изменения энтропии в различных процессах.
Изменение энтропии нельзя непосредственно измерить, измерять можно только теплоту. Количество теплоты может быть различным в обратимом и необратимом процессе, но изменение энтропии в них должно быть одинаковым, если одинаковы начальное и конечное состояния
dSобр. = 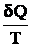 обр.
обр. 
S2 – S1 = dSнеобр. > 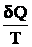 необр Þ
необр Þ 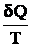 обр.
обр.  >
> 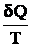 необр. (4.5)
необр. (4.5)
Как и работа, теплота обратимого процесса всегда больше теплоты необратимого при заданных начальном и конечном состояниях.
В термодинамике вводятся функции состояния системы, убыль которых в обратимом процессе, протекающем при постоянстве определённой пары термодинамических параметров, равна максимальной полезной работе и называются они термодинамическими потенциалами. В зависимости от условий протекания процесса различают два ТП.
1) Энергия Гельмгольца.
Преобразуем выражение таким образом, чтобы функции состояния попали в одну сторону неравенства – влево:
dU - TdS £ -dW.
Представим изотермический процесс и проинтегрируем это уравнение
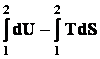 £ -AT Þ DU - TDS £ -AT Þ U2 – U1 – T(S2 – S1) £ -AT.
£ -AT Þ DU - TDS £ -AT Þ U2 – U1 – T(S2 – S1) £ -AT.
(U2 –TS2) – (U1 –TS1) = DW £ - AT. (7.8)
Получили новую функцию состояния, называемую энергией Гельмгольца или изохорно-изотермический потенциал
W º U – TS(7.9)
DW = W2 – W1.
DW £ -AT; -DW ³ AT; -DW= (AT)max (7.10)
Убыль энергии Гельмгольца равна максимальной работе обратимого изотермического процесса. В необратимом процессе работа полученная оказывается меньше убыли энергии Гельмгольца, а затраченная забота больше роста энергии Гельмгольца.
Напишем полный дифференциал энергии Гельмгольца и подставим в него фундаментальное уравнение Гиббса
dW = dU – TdS – SdT Þ dW £ TdS - pdV - dA’ – TdS – SdT
dW £ - SdT - pdV - dA’ .
При Т,V = const в самопроизвольном процессе dA’³0, отсюда критерием на-
правления самопроизвольного процесса будет уменьшение энергии Гельмгольца
dW V,T £ 0при Т,V = const(7.11)
Стабильное равновесие достигается при минимуме энергии Гельмгольца.
dW V,T = 0; (d2W/d Х2) V,T > 0 (7.12)
– условие стабильного равновесия при Т,V = const.
Полный дифференциал энергии Гельмгольца в зaкрытой системе
dW = – SdT – pdV (7.13)
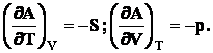 (7.14)
(7.14)
С ростом температуры и объема энергия Гельмгольца всегда падает, так как энтропия и давление системы всегда имеют положительное значение, и производные будут отрицательными.
2) Энергия Гиббса.
Проинтегрируем фундаментальное уравнение Гиббса при T, p = const
dU - TdS + pdV £ - dW’
d(U –TS +PV) £ - dW’
D(U –TS +PV) £ - W’p,T
Новая функция состояния – энергия Гиббса или изобарно-изотермический потенциал
G º U + pV– TS ;(7.15)
DG = G2 – G1.
DG £ -W’p,T; -DG ³ W’p,T; -DG= W’p,T(max) (7.16)
Убыль энергии Гиббса равнa максимальной полезной работе изобарно-изотермического процесса.
