Лабораторная работа №4. ОПРЕДЕЛЕНИЕ МАССЫ БРОМАТА КАЛИЯ В КОНТРОЛЬНОМ РАСТВОРЕ KBrO3
ОПРЕДЕЛЕНИЕ МАССЫ БРОМАТА КАЛИЯ В КОНТРОЛЬНОМ РАСТВОРЕ KBrO3.
Метод титриметрического анализа: редоксиметрия, метод йодометрии.
Тип титрования: прямое титрование.
Цель работы: Познакомиться с методикой определения массы бромата калия в контрольном растворе
Задача:
1.Определить массу бромата калия KBrO3 в контрольном растворе йодометрическим методом анализа по прилагающейся методике.
2. По результатам титрованиярассчитать массу (г) бромата калия KBrO3 в объеме мерной колбы.
Чтобы определить массу бромата калия KBrO3в объеме мерной колбы (г /Vм.к.) необходимо оттитровать аликвотную часть контрольного раствора KBrO3 стандартным раствором тиосульфата натрия Na2S2O3·5H2O, соблюдая условия титрования (температурный режим титрования и среду титрования).
Требования техники безопасности при выполнении работы:
1. Необходимо соблюдать свое рабочее место в чистоте и порядке.
2. При выполнении работы рационально использовать рабочее время.
3. Необходимо соблюдать правила работы со стеклянной посудой.
4. Аликвоту раствора следует отбирать нагнетателем или грушей.
5. Принимать пищу в лаборатории запрещается.
6. По окончании работы необходимо убрать за собой рабочее место.
1.Химическая сущность определения:
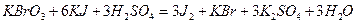
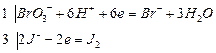
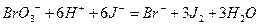
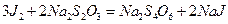
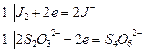
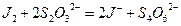
МЭ(KBrO3)= М/6 = 27,83 г/моль
МЭ(Na2S2O3·5H2O) = М = 248,18 г/моль
МЭ(J2) = М/2 = 126,90 г/моль
2.Методика определения массы KBrO3в контрольном растворе.
Химические реактивы:
1.вода дистиллированная;
2. иодид калия, KJ, 10% раствор;
3. крахмал, 1% раствор;
4.серная кислота, H2SO4, 2н раствор;
5.тиосульфат натрия Na2S2O3 · 5H2O, стандартный раствор метода, установленной концентрацией;
6.бромат калия, KBrO3, контрольный раствор;
Посуда и оборудование:
1.коническая колба, емкостью 250-300мл;
2.мерная колба, емкостью 100,00мл;
3.мерный цилиндр;
4.химическая воронка;
5.часовое стекло;
5.промывалка;
3. Методика определения массы KBrO3 в контрольном растворе.
Подготовить чистую мерную колбу. Контрольный раствор KBrO3 получить у лаборанта. Раствор разбавить в мерной колбе до метки холодной дистиллированной водой, закрыть пробкой и тщательно перемешать. Бюретку ополоснуть раствором Na2S2O3 · 5H2O, затем в неё налить раствор до 0 (носик бюретки должен быть заполнен раствором Na2S2O3 · 5H2O). Коническую колбу ополоснуть дистиллированной водой. Пипетку ополоснуть раствором KBrO3.
Пипеткой отобрать аликвоту (10,00 мл) контрольного раствора KBrO3, перенести в коническую колбу, 10мл 2н раствора H2SO4 и 10мл 10% раствора KJ, отмеренные мерным цилиндром. Коническую колбу накрыть часовым стеклом, чтобы предупредить потери иода.
Для завершения реакции смесь оставить на 5 минут в темноте. Затем снять часовое стекло и ополоснуть его над конической колбой дистиллированной водой, собирая промывные воды в коническую колбу. Прибавить в коническую колбу примерно 50мл дистиллированной воды. Оттитровать смесь в конической колбе стандартным раствором Na2S2O3 · 5H2O до светло-жёлтой окраски, затем добавить 1-2мл индикатора крахмала и дотитровать раствор до перехода синей окраски в бесцветную от одной капли раствора Na2S2O3 · 5H2O. Титрование повторить не менее 3-х раз. Вычислить средний объём Na2S2O3 · 5H2O, израсходованный на титрование. По результатам титрования вычислить массу KBrO3 в контрольном растворе.
3.Пример вычисления массы KBrO3 в контрольном растворе по результатам титрования.
Задача. Контрольный раствор KBrO3 разбавили холодной дистиллированной водой в мерной колбе ёмкостью 100,00мл. Аликвоту этого раствора, 10,00мл обработали в кислой среде иодидом калия и оттитровано 10,25мл раствора стандартного раствора Na2S2O3·5H2O (средний объём) с СН(Na2S2O3 · 5H2O) = 0,04905 моль/л. Вычислить массу KBrO3 в контрольном растворе.
| Дано: СН(Na2S2O3 · 5H2O) = 0,04905 моль/л VК = 100 мл VП = 10,00 мл V(Na2S2O3 · 5H2O) = 10,25 мл МЭ(KBrO3)= М/6 = 27,83 г/моль | 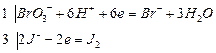 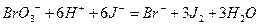 1.найдем по закону эквивалентных отношений концентрацию бромата калия, выраженной через нормальную концентрацию СН: 1.найдем по закону эквивалентных отношений концентрацию бромата калия, выраженной через нормальную концентрацию СН: 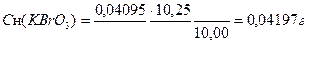 2. найдем массу бромата калия в контрольном растворе, т.е. в объеме мерной колбы 2. найдем массу бромата калия в контрольном растворе, т.е. в объеме мерной колбы 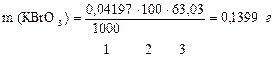 Вопросы к строчке: 1.Сколько моль-экв KBrO3 содержится в 1,00мл раствора? 2.Сколько моль-экв KBrO3содержится в объеме мерной колбы, в 100,00мл раствора? 3.Сколько г KBrO3 содержится в объеме мерной колбы 100,00мл раствора? Вопросы к строчке: 1.Сколько моль-экв KBrO3 содержится в 1,00мл раствора? 2.Сколько моль-экв KBrO3содержится в объеме мерной колбы, в 100,00мл раствора? 3.Сколько г KBrO3 содержится в объеме мерной колбы 100,00мл раствора? |
| m(KBrO3) = ? |
4.Оформление лабораторной работы
4.1.Название лабораторной работы
4.2.Метод анализа:
4.3.Способ титрования:
4.4.Цель работы:
4.5.Задачи работы:
4.6.Химическая сущность (закончить реакцию ОВР, уровнять методом полуреакций):
KBrO3 + Na2S2O3 + H2SO4 =
4.7.Определить молярные массы эквивалентов (по полуреакции):
МЭ(KBrO3)=
МЭ(Na2S2O3·5H2O) =
МЭ(J2) =
4.8.Таблица результатов титрования
| № п/п | V(KBrO3) | V(Na2S2O3· 5H2O) | Vср. Na2S2O3· 5H2O |
| | |||
| | |||
| |
4.9. Вычисление массы бромата калия в контрольном растворе.
Подставляются свои данные, полученные по результатам предыдущих работ и по результатам титрования
| Дано: СН(Na2S2O3 · 5H2O) = Vм.к. = Vпип. = V(Na2S2O3 · 5H2O) = МЭ(KBrO3) = | |
| m(KBrO3) = ? |
Вопросы для самоконтроля.
- Почему можно анализировать бромат калия методом йодометрии? Обоснуйте свой ответ.
- Какой тип титрования применяется в определении?
- Как фиксируется окончание реакции между раствором?
- Почему при фиксировании точки эквивалентности нельзя добавлять сразу индикатор?
- Как правильно отобрать аликвоту контрольного раствора из мерной колбы.
- Как правильно заполнить носик бюретки.
- Зная массу бромата калия в контрольном растворе, в объеме мерной колбы, попробуйте вычислить простой титр этого раствора, нормальную и молярную концентрации, сложный титр бромата калия по тиосульфату натрия.
