Лабораторная работа №4
«Микрометод определения молярной массы вещества криометрически (по Расту)».
1. Определить криоскопическую постоянную для камфоры по понижению температуры плавления раствора нафталина в камфоре, заданного состава, если молярная масса нафталина известна и равна 128,1 г\моль.
а. Капиллярным методом измерить температуру плавления камфоры (t1) и смеси нафталина в камфоре (t2) с массовой долей нафталина (капиллярный метод см. далее)
w = 10%
б. Рассчитать понижение температуры плавления (Dt) смеси нафталина в камфоре по сравнению с камфорой Dt = t1 – t2
в. Рассчитать криоскопическую постоянную для камфоры по формуле:
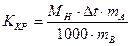 , где
, где
Мн – молярная масса нафталина;
mА – навеска камфоры (масса), взятая для приготовления смеси нафталина в камфоре;
mВ – навеска нафталина.
2. Определить молярную массу бензойной кислоты (С6Н5СООН) по пониженнию температуры плавления раствора бензойной кислоты в камфоре, заданного состава, если криоскопическая постоянная для камфоры известна.
а. Капиллярным методом измерить температуру плавления камфоры (t1) и смеси бензойной кислоты в камфоре (t3) с массовой долей бензойной кислоты w = 5%
б. Рассчитать понижение температуры плавления (Dt¢) смеси бензойной кислоты в камфоре по сравнению с камфорой Dt¢ = t1 – t3
в. Рассчитать молярную массу бензойной кислоты по формуле:
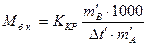 , где
, где
Ккр – криоскопическая постоянная для камфоры;
m¢А – навеска камфоры (масса), взятая для приготовления смеси бензойной кислоты в камфоре;
m¢В – навеска бензойной кислоты.
3. Рассчитать относительную ошибку (a).
Относительную ошибку рассчитать по формуле:
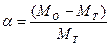 , где
, где
М0 – молярная масса бензойной кислоты, полученная в опыте;
МТ – молярная масса бензойной кислоты, взятая из таблицы и равная 122,1 г\моль.
4. Полученные в работе данные представить в таблице:
| Исследуемая Cистема | Температура исчезновения последнего кристалла, 0С | Температура появления первого кристалла, 0С | Температура плавления |
| Камфора 10% раствор нафталина в камфоре 5% раствор бензойной кислоты в камфоре |
РАСЧЕТЫ ПО ЭКСПЕРИМЕНТАЛЬНЫМ ДАННЫМ.
1) Расчет криоскопической постоянной для камфоры:
mА =
mВ =
Dt =
Мн = 128,1 г/моль
Ккр =
2) Расчет молярной массы бензойной кислоты:
m¢А =
m¢В =
Dt¢ =
Ккр =
Мб.к. =
3) Расчет относительной ошибки опыта:
a =
Примечания:
Микрометод Раста имеет следующие особенности и преимущества:
1. Использование в качестве растворителя камфоры, имеющей высокую температуру плавления (1790С) и высокое значение криоскопической постоянной.
2. Использование обычного термометра с делениями в 0,10 -10 позволяет с высокой точностью определять понижение температуры плавления раствора (Dt) по сравнению с температурой плавления чистого растворителя.
3. Для определения температуры плавления требуетсся небольшая масса образца.
Метод имеет ограничения и недостатки:
1. Метод не применим к веществам, нерастворимым в камфоре, реагирующим с ней химически или разлагающимися при температуре ее плавления.
2. В методе необходимо определять криоскопическую постоянную для камфоры, а не использовать табличное значение этой величины.
Занятие №4
