Флавоноиды различных типов
Полифенольные соединения – самый распространенный класс природных веществ, относящихся к различным группам биологически активных соединений:
1. простые фенолы;
2. полифенольные кислоты;
3. кумарины;
4. ксантоны;
5. танины гидролизуемого и конденсированного типов;
6. флавоноиды различной степени окисленности аромати-ческих колец и кольца С (в том числе флаволигнаны);
7. антрацены различных типов.
Как правило, они содержатся вместе или в различных сочетаниях в составе практически всех растений и являются действующими веществами более 70% лекарственных средств растительного происхождения.
Многообразие флавоноидных соединений связано:
§ с различной степенью окисленности пиранового кольца С
§ с различным расположением кольца В
§
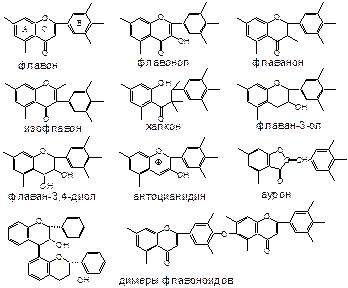 |
с различным числом ОН-групп в ароматических кольцах и с их расположением
Во всех структурах в качестве заместителей описаны: ОН, ОСН3, С-алкильные фрагменты до С5, Cl, SO3H, углеводные (О- и С-) фрагменты и др.
В зависимости от перечисленных признаков, флавоноиды делят более чем на 20 групп. Все они являются полифенолами, кольца А и В сопряжены с С=О группой окисленных форм флавоноидов и изолированы в структурах флаванов. Флаван-3-олы и флаван-3,4-диолы – оптически активны.
Выделение:
Около 2 г измельченного растительного сырья экстраги-руют спиртом этиловым 50-95% или метиловым при нагревании на кипящей водяной бане в течение 1.5-2 часов (соотношение 1:10), фильтруют.
Для качественного анализа отбирают по 1-3 мл фильтрата.
Качественный анализ [1-4,7,10-12,22]:
Все представители этой группы соединений являются полифенолами, поэтому дают все реакции фенольных соедине-ний. Специфика окрашивания связана с расположением и количеством ОН-групп. В зависимости от степени окисленности пропанового звена и характера конденсации колец описаны в большей или меньшей степени специфичные реакции:
q Добавляют раствор аммиака (или выдерживают в парах аммиака) или добавляют 2 н раствор натрия карбоната, появляется, углубляется или меняется естественный цвет анализируемых образцов: углубляется до ярко-желтого (флавоны), желто-зеленого (флавоны, флаваноны), розовая или красная меняется до серо-синей или фиолетовой (антоцианы), желтая или оранжевая меняется до интенсивно-оранжевой или красной (халконы, ауроны), появление темного окрашивания (изофлавоны). В УФ-свете при действии паров аммиака, слабая желто-коричневая флюоресценция меняется на ярко-желтую или желто-зеленую (флавоны, флавонол-3-гликозиды), бледно-желтую (флаваноны), бледно-синюю (катехины).
q Добавляют 1-2 мл раствора натрия молибдата, появляется желтое окрашивание (все фенольные соединения с орто-диоксигруппировкой).
q Реакция Запрометова (см."фенолы"). Добавляют 1-3 капли реактива ванилина появляется розовое или оранжевое окрашивание (пирокатехин и все флавоноиды, имеющие пирокатехиновый фрагмент), красно-фиолетовое окрашивание (флороглюцин и все флавоноиды, имеющие флороглюциновый фрагмент), ярко-желтое окрашивание (флавоны, флавонолы), малиновое (флаван-3,4-диолы, димеры групп А и Б), розовое (эфиры катехинов), ярко-красное (галлокатехины).
q Добавляют 1-3 мл реактива Паули по Кутачеку (см. "фенолы"), появляется красное окрашивание на желтом фоне (флавоноиды, гликозиды, аминокислоты).
q Добавляют 1-3 капли раствора хлорида железа окисного (от 0.1 до 2% водного или 1% спиртового раствора) появляется коричневое окрашивание (флавонолы со свободной 3-ОН группой), зеленое (при наличии свободной 5-ОН группы) и т.д; синие, сине-фиолетовые оттенки (флавоноиды, антрахиноны, фенолы, фенолокислоты, дубильные вещества).
q Реакция Гейдж. Добавляют 1-3 капли 1% спиртового раствора алюминия хлорида, усиливается желтый цвет. При добавлении 2-5% спиртовых растворов алюминия хлорида, появляется окрашивание от бледно-желтого до ярко-желтого (флавоны, флавонолы, халконы, ауроны). При действии 5% раствора алюминия хлорида появляется красное окрашивание (халконы), оранжевое (ауроны), коричнево-желтое (изофлавоны)
q
| |
q Добавляют 1-2 мл реактива Миллона (10 г ртути нитрата закисной растворяют в 8,5 мл кислоты азотной, разбавляют двойным объемом воды, прозрачный раствор сливают) и нагревают 3-5 минут. При этом меняется окрашивание (все полифенолы и их метоксипроизводные).
q Реакция Херхаммера и Миллера. Добавляют 1-2 мл 2% хлорокиси циркония или цирконила хлористого в спирте метиловом, появляется желтое окрашивание (5-оксифлавоны и 5-оксифлавонолы); исчезновение желтого окрашивания от добавления 2-3 капель 5% раствора кислоты лимонной (5-оксифлавоны, 3-гликозиды флавонолов, 3-этерифицированные флавоноиды).
q Добавляют 1-3 капли 0.1 н раствора серебра азотно-кислого и 1-3 капли 5 н аммиака водного (1:1) при комнатной температуре или при нагревании появляется красно-коричневое окрашивание или осадок моментально (орто-диоксизаме-щенные), через 2-3 минуты - пара-диоксизамещенные, только после нагревания - мета-диоксизамещенные.
q Добавляют 3-5 капель раствора бис-диазотированного бензидина, появляется красно-коричневое окрашивание (при наличии свободных орто- и(или) пара-положений, относи-тельно фенольных ОН-групп).
q «Госсипетиновая проба».Добавляют 1-2 мл 2% раст-вора бензохинона в спирте, появляется красное окрашивание (5,8-диоксифлавоноиды, пара-диоксигруппировка полифенолов).
q Добавляют 1-2 мл 1% раствора натрия боргидрида в спирте изопропиловом и 1-2 мл 1% спиртового раствора алюминия хлорида, появляется красное окрашивание (флаваноны, изофлаваноны).
q Реактив Мартини-Беттоло (насыщенный раствор пяти-хлористой сурьмы в четыреххлористом углероде) вызывает желтое или оранжевое окрашивание (флавоны, изофлавоны, флавонолы, флаваноны).
q Добавляют насыщенный раствор сурьмы треххлористой в хлороформе, появляется желтое или красное окрашивание (5-оксифлавоны и 5-оксифлавонолы), зеленое, переходящее в синее (каротиноиды), зелено-бурое окрашивание (тритерпены).
q Добавляют 1-2 мл 5% спиртового раствора 2,4,5-тринитрофенола и несколько капель раствора калия гидроксида, появляется красное окрашивание (катехины).
q Добавляют 1-2 мл водного или спиртового раствора пара-толуолсульфокислоты, появляется красное или оранжевое окрашивание (лейкоантоцианидины).
q Добавляют 1-3 мл свежеприготовленного раствора диазотированного сульфаниламида, появляется оранжевое или красное окрашивание. Если окрашивание появляется сразу (7-оксифлавоны, 7-оксифлавонолы, 7-оксиизофлавоны), если через 1-2 минуты - (7-оксифлаваноны при наличии свободных орто- и(или) пара-положений, относительно ОН-групп).
q Цианидиновая проба (проба Chinoda). Добавляют магний (порошок) в кислоте хлороводородной концентри-рованной, появляется окрашивание от оранжевого до красного (все флавоны, флавонолы, флаваноны). Халконы и ауроны цианидиновую реакцию не дают! Но при добавлении кислоты хлороводородной концентрированной без магния, образуют красное окрашивание за счет образования оксониевых солей.
q Добавляют раствор цинка в 18% кислоте хлороводо-родной или цинка порошок и 18% кислоту хлороводородную, появляются яркие оранжевые или красные оттенки (флавоноиды, дигидрофлавонолы).
q Добавляют 1-2 мл 3-5% водного раствора кислоты борной, выпадают белые осадки (реакция на орто-диоксигруппировку). Если добавляют раствор кислоты борной в ацетоне, появляется ярко-желтое окрашивание (5-оксифлавоны). Добавление лимонной кислоты усиливает окраску, придает ей устойчивость (реакция Вильсона).
q Добавляют 1-2 мл 70% раствора церия сульфата в кислоте серной концентрированной, появляется желто-коричневое окрашивание, при стоянии цвет темнеет и выпадают осадки (бифлавоноиды).
q Добавляют несколько капель кислоты серной концентрированной, появляются окраски от желто-коричневых до красно-коричневых (изофлавоны).
q Добавляют 1-3 мл 10% раствора кислоты щавелевой в смеси ацетон-вода (1:1), появляются яркие окраски растворов (антоцианы, антоцианидины).
q Добавляют 3-5 капель 2% раствора среднего свинца ацетата, появляются осадки от ярко-желтого до оранжево-красного цвета (флавоноиды с орто-диоксигруппировкой), красные и синие (антоцианы). Добавляют 1-3 капли 1% раствора свинца ацетата, появляется красное окрашивание или осадок (флавонолы), желтое (флавоны).
q Реакция Хайса (диазотированный пара-нитроанилин). Добавляют 1-2 капли диазореактива, появляется окрашивание от желтого до коричневого (реакция на свободные орто- и (или) пара-положения относительно имеющихся ОН-групп).
* Окраски и реактив более устойчивы, при добавлении нескольких капель 20% раствора натрия карбоната (реактив по Брею) (флавоноиды, все фенольные соединения, ароматические кислоты).
q Добавляют несколько капель кислоты хлороводородной концентрированной, появляется красное окрашивание (халконы, ауроны).
q На БХ в УФ-свете – голубая флюоресценция. При обработке пятен парами аммиака, в УФ-свете флюоресценция усиливается (изофлавоноиды).
Как уже отмечалось выше, в растительном сырье могут быть различные типы флавоноидных соединений, агликоны, гликозиды, отличающиеся степенью окисленности колец и связанной с этим различной растворимостью в спиртах, водно-спиртовых растворах, ацетоне, водно-ацетоновых смесях и других растворителях.
Кроме того, в любом растении, помимо флавоноидов, присутствуют полифенольные соединения других групп (фенолы, фенолокислоты, антраценовые, дубильные вещества, кумарины), кислоты (алифатические, ароматические, окси-, оксо-, амино-), углеводы, полисахариды и другие водо-, спирто- и ацетонорастворимые вещества.
В связи с этим, для выбора более или менее селективного метода извлечения флавоноидов целесообразен предваритель-ный качественный химический или хроматографический анализ компонентного или группового состава веществ в анализируемом объекте и разделение на группы.
О- и С-гликозиды изофлавонов и флаванонов делят на колонках или пластинах силикагеля и кремневой кислоты в системах БУВ (40:12.5:29 и 4:1:5).
При двумерном хроматографировании в качестве второй подвижной фазы используют 2, 6 или 15% уксусную кислоту.
При наличии значительных количеств флавоноидов в растительных экстрактах удачным может быть вариант колоночной хроматографии с использованием силикагеля, полиамида, целлюлозы, сефадекса, оксида алюминия, магнезола, кизельгура и т.д.
При этом подвижные фазы подбирают исходя из растворимости разделяемой суммы веществ.
Поскольку все типы флавоноидов, как полифенолы имеют сродство к гидроксилсодержащим растворителям, то задачей конкретного исследования является подбор оптимального сорбента и элюентов.
Силикагель используется для разделения изофлавонов, флаванонов, дигидрофлавонолов, метилированных и ацилированных флавонов и флавонолов с использованием в качестве элюентов хлороформа, его смеси с эфиром и(или) этилацетатом, бензолом 1:1, бензол - этилацетат 6:1.
Метилированные флавоны из ацетоновых экстрактов элюируют смесью бензол - гексан 3:1 и хлороформ - метанол 20:0.8, или 99.5:0.5, бензол - хлороформ 5:2, бензол-эфир 5:1. Используя в качестве алюентов этилацетат и его смесь с метанолом 9:1, бензол с метанолом 9:1 на силикагеле можно успешно разделить О- и С-гликозиды. Кислотная (НС1) обработка силикагеля способствует разделению полярных компонентов экстрактов. В системе этилацетат – пиридин – вода – метанол 80:12:10:5 С-гликозиды флавонов располагаются в ряд: 8-С-ксилозил > 8-С-глюкозил > 6-С-ксилозил > 6-С-глюкозилфлавоны; ди-С-гликозиды: 6,8-ди-С-глюкозил > 6-С-глюкозил-8-С-ксилозил > 6-С-ксилозил-8-С-глюкозил > 6,8-ди-С-ксилозилфлавоны.
Магнезол предложен для разделения смеси флавонов, флавонолов, флаванонов и их гликозидов. Например, при использовании в качестве элюента смеси бензол – хлороформ 1:1 и хлороформ можно отделить изофлавоны, а смесью ацетон – эфир 1:1 разделить флаваноны, флавонолы и флобафены.
Оксид алюминия различной степени активности можно использовать для разделения флавоноидов различной кислот-ности и полярности. Кроме того, из растительных экстрактов бензолом и эфиром можно отделить хлорофиллы и ксанто-филлы, а затем бифлавоноиды, 5-окси-, и 5-дезоксифлавоноиды, 3’,4’-, 6,7- и 7,8-диоксифлаваноны и дигидрофлавонолы.
Целлюлоза может быть использована для всех групп флавоноидов и их гликозидов. На колонках целлюлозы Эхтеола лучше делить флавоноиды и их метокси- и(или) ацетоксипроизводные. При этом важен подбор элюентов, препятствующих или способствующих набуханию сорбента. Целлюлоза может быть модифицирована обработкой кислотами, что расширяет возможности разделения.
На колонках с целлюлозой разделяют антоцианины, но состав элюатов должен тщательно контролироваться в присутствии других групп флавоноидов.
Полиамид различных марок широко используется для разделения и очистки всех групп флавоноидов. Полиамиды модифицированных марок требуют работы в определенных интервалах рН, «мокрого» и «сухого» способов заполнения колонок, их размеров и степени измельчения сорбента.
На полиамиде успешно делят моно-, ди- и тригликозиды, антоцианидины с различным числом ОН-групп и их расположением.
Гликозиды изофлавонов, флаванонов, дигидрофлавонолов, флавонов и флавонолов разделяют элюентами: бензол – метанол 3:1, 7:3, 6:4 и 1:1.
Гликозиды флавонов и флавонолов можно делить с использованием водно-метанольных смесей, а смесь моно-, ди- и триметоксипроизводных кемпферола и кверцетина разделяют с использованием сложного элюента: хлороформ – метанол – метилэтилкетон - 2,4-пентадион 20:10:5:1 или более простого сочетания: хлороформ - этилацетат 3:1, хлороформ - метанол 1:3.
Ауроны и халконы между собой разделяют метанолом, а в присутствии бифлавонов и флаванонов лучшее разделение достигается при использовании водно-метанольных смесей.
На величину сорбции флавоноидов, кроме природы разделяемых веществ и характера элюентов, влияет и величина макромолекул полиамидного сорбента.
При этом наличие двойной связи С2=С3 у флавоноидов приводит к значительному повышению сорбционной актив-ности таких соединений по сравнению с соответствующими дигидропроизводными.
Кислотно-основные свойства флавоноидов также сказываются при подборе условий их хроматографического разделения. Так, изучение диоксифлавонов показало, что 3- и 5-оксигруппы по-разному влияют на кислотные свойства 7- и 4’-оксигрупп. Кислотность 3- и 5-оксигрупп в 3,7-; 3,4’-; 5,4’-диоксифлавонах меньше, чем в незамещенных 3- и 5-оксифлавонах, однако, у 5,7-диоксифлавона ионизация 7-ОН группы усиливает кислотные свойства 5-ОН группы по сравнению с соответствующими монооксифлавонами. Ниже приведены значения ΔрКосн для флавоноидов, характеризующие вклад заместителя в изменение основности
Величины вкладов заместителей в ΔрКосн
Некоторых флавоноидов
| соединение | ΔрКосн | |||||
| 7-ОН | 4’-ОН | 5-ОН | 3-ОН | 5-ОСН3 | 3-ОСН3 | |
| флавон | - | - | - | - | - | - |
| 7-окси- | +0.54 | - | - | - | - | - |
| 4’-окси- | - | +0.46 | - | - | - | - |
| 5-окси- | - | - | -1.74 | - | - | - |
| 3-окси- | - | - | - | -1.37 | - | - |
| 5-метокси- | - | - | - | - | +0.11 | - |
| 3-метокси- | - | - | - | - | - | -1.34 |
| 5,4’-диокси- | - | +0.97 | -1.21 | - | - | - |
| 5,7-диокси- | +1.07 | - | -1.21 | - | - | - |
| 3,4’-диокси- | - | +0.55 | - | -1.26 | - | - |
| 3,7-диокси- | +0.56 | - | - | -1.35 | - | - |
| 3-окси-5-метокси- | - | - | - | -0.73 | +0.75 | - |
| 3,5-диокси- | - | - | -0.66 | -0.29 | - | - |
Приведенные данные могут быть полезны при исследо-вании закономерностей хроматографического поведения флаво-ноидов, при подборе условий выделения, разделения и очистки молекул из многокомпонентных растительных экстрактов.
Литературные данные по адсорбционной и распредели-тельной хроматографии, например, на полиамиде затрудняют выявление роли каждого из заместителей в хроматографическом процессе, а описанные выше данные показывают роль каждого заместителя по природе и расположению.
В зависимости от состава элюентов на полиамиде может осуществляться либо адсорбционный (водная система), либо распределительный (неводная система) хроматографический процесс, а адсорбция флавонов обусловлена наличием сопряженной ароматической системы структурных фрагментов молекулы.
По вкладу в адсорбцию гидроксильные группы располага-ются в ряд: 4’-ОН > 3-ОН > 5-ОН > 7-ОН. В этом же ряду происходит уменьшение констант ионизации, за исключением 7-оксифлавона. Кислотные свойства монооксифлавонов умень-шаются в последовательности: 7-ОН > 4’-ОН > 3-ОН > 5-ОН, а кислотность 7- и 4’-ОН групп у производных 5-оксифлавона выше, чем у производных 3-ОН.
Изофлавоноиды делятся в системе хлороформ - метанол 4:1, флаваноны - бензол-уксусная кислота-вода 125:72:3, хлороформ - уксусная кислота – вода 2:1:1 и бензол – пиридин – муравьиная кислота 6:9:5, дигидрофлавонолы – хлороформ-метанол-уксусная кислота 7:1:1, халконы и ауроны в системе: бензол – этилацетат - муравьиная кислота 9:7:4, хлороформ – этилацетат - муравьиная кислота 6:3:1, толуол – этилацетат - муравьиная кислота 5:4:1, антоцианидины и антоцианины: этилацетат - муравьиная кислота - 2 н НС1 или этилацетат – бутанол - муравьиная кислота – вода 5:3:3:1.
Ниже приведены наиболее часто употребляемые системы растворителей, если разделение проводится на закрепленном слое силикагеля «Silufol UV254»:
1. для разделения флавоноидов и отделения их от других групп соединений:
§ бензол – пиридин - муравьиная кислота - вода 36:9:5:1
§ бензол - диоксан - уксусная кислота 90:25:4
§ бензол - ацетон 4:1 и 9:1
§ хлороформ - 3% метанол 1:1
§ хлороформ – уксусная кислота – вода 13:6:1
2. для О-гликозидов флавонов:
§ этилацетат – метилэтилкетон - муравьиная кислота - вода 5:3:1:1
§ метанол - уксусная кислота - вода 18:1:1
§ н-бутанол – этанол – вода 20:5:11
§ бутанол-2 – этилацетат – ДМФА 10:6:3
§ для С-гликозидов флавонов:
§ этилацетат - уксусная кислота - вода 10:2:1
§ этилацетат - метанол 8:2
4. для флавонолов различной степени и характера замещения:
§ толуол – этилформиат - муравьиная кислота 5:4:1
§ этилацетат - муравьиная кислота - вода 70:15:15
§ этилацетат – толуол- метанол 8:6:1
5. для лейкоантоцианидинов – отделение от примесей проводят переосаждением из метанола эфиром, а разделение проводят в системах:
§ этилацетат – хлороформ - муравьиная кислота 3:3:1
§ эфир – этилацетат 1:1
Птерокарпаны и изофлавоны разделяют на силикагеле Merck-60 в системах: бензол – этилацетат – метанол - петролейный эфир 6:4:1:6 или хлороформ – метанол 8:2.
Разделение катехинов и отделение их от полимеров проводят на силикагеле, а из водных растворов - на кожном порошке, десорбируя катехины эфиром и этилацетатом, а полимеры катехинов - ацетоном и 50% ацетоном.
Разделение антоцианов возможно на силикагеле или целлюлозе с использованием в качестве элюентов и растворителей БУВ 4:1:5 или препаративно на бумаге в этой же подвижной фазе.
Порошкообразная целлюлоза по своим хроматографичес-ким свойствам очень похожа на фильтровальную бумагу, однако как сорбент обеспечивает лучшее разделение родственных групп соединений. Смеси целлюлозы с силикагелем, обладая достоинствами каждого, вместе оказались удачными для разде-ления, например, антоцианов, отделения их от фенолкарбо-новых кислот.
Для разделения антоцианов была использована смесь полиакрилонитрила и полиамида 7:2; поливинилпирролидон, содержащий разные количества целлюлозы. Для антоцианов пригодна и микрокристаллическая целлюлоза в тех же системах, что и на бумаге.
Флавоноиды с тремя и более гидроксигруппами рекомен-дуется хроматографировать на полиамиде, а гликозидированные формы флавоноидов - на микрокристаллической целлюлозе, метиловые эфиры флавоноидов лучше разделяются на полиамиде.
Одним из основных методов сравнительного исследования и препаративного выделения флавоноидов различной природы является метод ВЭЖХ.
Так, например, гликозидированные формы флавоноидов предложено делить на колонке, заполненной m-Bondapak С18 или Eclipse XDR-C18, с использованием в качестве подвижной фазы смеси: метанол-вода-уксусная кислота (10:88:2) [123], при расходе подвижной фазы 1-2 мл/мин и использовании УФ-детектора (280 нм).
Разработана методика определения флавоноидных агликонов на той же неподвижной фазе, используя градиентное элюирование смесью: метанол-вода-ацетонитрил состава от (6:90:4) до (17.4:71:11.6) в течение 30 минут. Расход подвижной фазы - 1 мл/мин. УФ-детектор (210 нм) [124]. Была предложена также методика разделения флавоноидов на колонке (100х2.1) с:Pell ODS (30-38 мкм) и колонке (250х4.6) с Pegasil ODS RP С18 (5 мкм) при 320С, градиентном элюировании смесью уксусная кислота-вода (10:90)-(82:18) в течение 47 минут, и от (82:18) до (100:0) за 8 минут. Расход подвижной фазы 0.8 мл/мин. Использовался УФ-детектор (277 нм) [125].
Эффективное разделение изофлавоноидов достигалось на колонке (100х4) с m-Bondasphere RP С18 (5 мкм) в двух вариантах:
А) градиентное элюирование смесью метиловый спирт-тетрагидрофуран-0.5% фосфорная кислота, состав которой в течение 20 минут меняется от (22.5:22.5:55) до (30:30:40) с УФ-детектором (254 нм).
Б) градиентное элюирование смесью изопропиловый спирт-тетрагидрофуран (25:65) А с ацетонитрилом (Б) и 0.5% фосфорной кислотой (С), состав которой (А:В:С) в течение 30 минут менялся от (15:15:83.5) до (0:78:75) при использовании УФ-детектора (254 и 276 нм) [126].
Анализ антоцианов предложено проводить на колонке с Inertsil ODS C18 сорбентом. В качестве подвижной фазы предложены смеси: А(орто-фосфорная кислота-вода 1.5:98.5) и В(орто-фосфорная кислота-уксусная кислота-ацетонитрил-вода 1.5:20:25:53.5) при увеличении содержания В в А от 15 до 35%. Четкого разделения пиков удалось, также, достичь используя подвижную фазу: А(TFA-H2O 0.5:99.5) и В(TFA-MeCN-H2O 0.5:30:69.5) при градиенте концентрации А:В от 7:3 до 5:5. В работе использован УФ детектор (520 нм) [127].
При проведении анализа катехинов, в условиях нормально-фазового процесса, оптимальных результатов удалось достичь, используя колонку с LiChrospher 100 CN (5 мкм) и подвижную фазу: н-гексан-этилацетат (55:45). В ходе анализа использовался УФ-детектор (278 нм) [128].
Хроматографическая система, состоящая из LiChrospher RP С18 в качестве неподвижной фазы и метанол-вода (2:3) в качестве элюентной системы хорошо зарекомендовала себя при разделении и анализе би- и тетрафлавоноидных молекул, определяемых в УФ области при 254 и 280 нм [129].
Тот же самый сорбент был использован для эффективного разделения флаволигнанов растения Hyparrhenia hirta. В качестве элюентных было опробовано несколько различных систем, при этом оптимальной была признана система с линейным градиентом концентрации А: метанол-уксусная кислота вода (18:1:1) в В: 2% уксусная кислота от 25 до 100% за 20 минут при расходе подвижной фазы 1 мл/мин и использовании фотодиодного детектора [129].
Для количественного анализа различных групп флавоно-идов в разные годы использовались гравиметрический, титро-метрический методы, фотоэлектроколориметрия, спектрофото-метрия, денситометрия и др. методы.
Долгие годы использовался хроматоденситометрический метод, сущность которого заключается в выделении и разделении флавоноидов с количественной оценкой плотности каждой окрашенной зоны на хроматограмме.
Метод Лоренца и Арнольда был основан на измерении плотности буро-красной окраски, образующейся при нагревании флавоновых веществ с калия гидроксидом. Однако, эта реакция не специфична, поскольку антраценовые и моносахара в подобных условиях дают такое же окрашивание.
Гудзак для количественного определения пользовался цианидиновой реакцией, основанной на восстановлении флавонов водородом, выделяющимся при взаимодействии магния в спиртовой среде в присутствии соляной кислоты.
Флавоновые вещества, при этом, дают окраску от оранжевой до малиновой, однако, если в растении присутствуют антоцианы или лейкоантоцианы, катехины, конденсированные дубильные вещества, они дают аналогичное окрашивание.
Более надежной представляется реакция с борной кислотой, дающая в растворе сухого ацетона желтое окрашивание при наличии орто-диоксигруппировки в структуре флавоноидных молекул. Лимонная кислота усиливает окраску, придает ей устойчивость, причем определение лучше проводить с сухим сырьем в растворе абсолютированного ацетона, поскольку влага снижает чувствительность реакции. Однако, применение сухого ацетона ограничивает метод, т.к. в нем растворяются только агликоны, гликозиды имеют ограниченную растворимость, а такие, как например, рутин вовсе не растворяются.
Гусева и Нестюк заменили сухой ацетон смешанным растворителем из 96% ацетона и 4% метанола, что не снизило чувствительности и расширило метод по признаку раствори-мости флавоноидов.
Для построения калибровочной кривой они пользовались изокверцитрином, замеряя плотность растворов фотоколори-метрическим методом.
В тех объектах, где преобладают агликоны или гликозиди-рованные формы, а также изофлавоны, ауроны или халконы, для построения калибровочной кривой следует использовать стандартные вещества соответствующей химической природы или эквивалентные по максимуму поглощения растворы неорганических веществ, учитывая коэффициенты пересчета.
Фотоколориметрический метод основан на использовании цветных реакций флавоноидов с солями различных металлов (Al, Ti, Cr, Fe, Sb), с лимонно-борным реактивом, азотнокислым и уксуснокислым уранилом, реакции восстановления Zn или Mg в кислой среде и др.
Учитывая кислотные свойства флавоноидов, использова-лись методы кислотно-основного титрования в неводных растворителях (DMFA, DMSO), полярографии и амперометри-ческого титрования.
Спектрофотометрическое определение флавоноидов прово-дят в экстрактах, растворах или непосредственно с хромато-грамм после закрепления окраски пятен специфическими проявителями.
В таблице приведены lmax для наиболее распространенных флавоноидов и гликозидов в растворах метанола [130], этанола различной концентрации [33]. В скобках даны коэффициенты пересчета, которые могут быть использованы в отсутствие СО при определении содержания флавоноидов с использованием реакции с AlCl3 или без него.
Значения lmax для некоторых флавоноидов
В спиртовых растворах
| Вещества | lmax MeOH абс. | lmax EtOH абс. | MeOH абс. | 50% MeOH | EtOH абс. | 95% EtOH | 50% EtOH |
| +AlCl3 | +AlCl3 | +AlCl3 | +AlCl3 | +AlCl3 | |||
| Апигенин 7-О-гликозид | |||||||
| Лютеолин 7-О-гликозид | 349 (854) 348 (442) | ||||||
| Ориентин-8-С-гликозид | |||||||
| Изо(гомо)- ориентин | |||||||
| Витексин | |||||||
| Изовитексин | |||||||
| Байкалеин 7-О-гликозид | 318-320 | ||||||
| Галангин | |||||||
| Кемпферол 7-О-рамнозид 7-О-рамно-галактозид 3-О-глюкозид (астрагалин) 3-О-арабо-фуранозид (авикулярин) | 358-364 | 372 (545) 364 (374) | 425±5 (870) 400±5 (320) | 415±5 (745) 390±5 (280) | 425±5 (850) 400±5 (305) | 425±5 (850) 395±5 (280) | 415±5 (740) 390±5 (280) |
| Морин | 372-374 | 420±5 (760) | 416±5 (750) | 425±5 (870) | 425±5 (810) | 415±5 (750) | |
| Кверцетин 3-О-рамнозид (кверцетрин) 3-О-глюкозид 7-О-рамнозид 3-О-арабино-зид 3-О-галакто-зид (гиперозид) 3-О-рамно-глюкозид (рутин) | 359-363 | 370 (646) 368 (366) 360 (260) | 460±5 (1000) 435±5 (560) 435±5 (550) 435±5 (425) | 430±5 (770) 415±5 (410) 415±5 (400) 417±8 (305) | 440±5 (900) 420±5 (450) 417±8 (430) 432±8 (400) | 430±5 (856) 405±5 (380) 405±5 (380) 410±5 (280) | 430±5 (755) 412±5 (400) 412±8 (395) 415±5 (280) |
| Мирицетин 3-О-рамнозид | 377 (618) | 450±5 (1005) 420±5 (450) | 440±5 (840) 425±5 (380) | 450±5 (920) 435±9 (465) | 435±5 (840) 415±5 (340) | 440±5 (780) 425±5 (360) | |
| Изосалипур-позид | 315-320 | 370 (564) | |||||
| Рамнетин | |||||||
| Изорамнетин 3-О-галакто-зид | |||||||
| Госсипетин 7-О-глюкозид 8-О-глюкозид | 387-390 |
Как видно, наличие углеводного заместителя в положении 3, приводит к гипсохромному сдвигу lmax на 10-12 нм, в положении 4¢-на 15 нм, в положении 5- на 12-17 нм, в положениях 6,7,8- lmax практически не снижается.
Эти данные могут быть полезны при выборе СО и lmax при спектрофотометрическом и фотоколориметрическом методах определения оптической плотности анализируемых растворов.
В Фармакопейных методиках (ГФ Х, Х1, ч.2) в качестве СО описаны кемпферол, кверцетин, лютеолин, рутин, гиперозид, изокверцетрин, гнафалозид А, авикулярин, изосалипурпозид [7], в научных статьях – эти и другие СО.
Перечень методик мог быть продолжен, однако обзор даже приведенных выше показывает, что все они состоят из 2 частей:
1. Получение извлечений из лекарственного растительного сырья или приготовление растворов препаратов.
2. Измерение оптической плотности полученных извлечений или растворов спектрофотометрическим или фотоколори-метрическим методами, либо непосредственно, либо после разделения компонентов извлечений на колонках полиамида или в тонком слое сорбентов (силикагеля, оксида алюминия).
Другие методики рекомендуют предварительную обработку сырья разнополярными органическими растворителями для отделения части сопутствующих экстрактивных веществ.
В большинстве методик для увеличения селективности определения содержания флавоноидов используется их способность образовывать комплексы с алюминия хлоридом, которые отличаются по интенсивности желтого окрашивания, батохромным сдвигом длинноволнового максимума и устойчивостью, в зависимости от места комплексообразования (3,5; 3’,4’,5’-ОН).
Некоторые авторы используют добавление к раствору равных количеств алюминия хлорида и натрия карбоната или хлорида, но при этом в реакцию комплексообразования могут вступать и другие группы полифенольных соединений с рядовым расположением ОН-групп.
В связи с этим, методы, где используется предварительное отделение части сопутствующих веществ или определение содержания флавоноидов после их хроматографического элюирования с колонок или хроматограмм, отличаются большей точностью, по сравнению с другими [131].
Для сырья и препаратов, где доминируют агликоны флавоноидов, но присутствуют и их гликозидированные формы, определение проводят по методикам:
Метод 1.Около 2 г (точная навеска) измельченного сырья помещают в колбу со шлифом вместимостью 150 мл, прибавляют 30 мл спирта этилового 90%, содержащего 1% кислоты хлороводородной концентрированной или 10% раст-вора кислоты серной, колбу присоединяют к обратному холодильнику, нагревают на кипящей водяной бане в течение 1 часа, охлаждают до комнатной температуры, фильтруют через бумажной фильтр в мерную колбу вместимостью 100 мл. Экстракцию повторяют еще 2 раза указанным выше способом, фильтруют через тот же фильтр в ту же мерную колбу, фильтр промывают спиртом этиловым 90% и доводят объем фильтрата тем же спиртом до метки (раствор А).
В мерную колбу вместимостью 25 мл помещают 2 мл раствора А, прибавляют 1 мл 1% раствора алюминия хлорида в спирте этиловом95% и доводят объем раствора тем же растворителем до метки. Через 20 минут измеряют оптическую плотность раствора на спектрофотометре при длине волны 430 нм в кювете с толщиной слоя 10 мм. В качестве раствора сравнения используют раствор, состоящий из 2 мл раствора А, доведенного спиртом этиловым 95% до метки в мерной колбе вместимостью 25 мл.
Содержание суммы флавоноидов в пересчете на кверцетин и абсолютно сухое сырье в процентах (Х) вычисляют по формуле:
|
764.6 . m . 2 . (100 - W)
где D - оптическая плотность испытуемого раствора;
764.6 - удельный показатель поглощения комплекса кверце-тина с алюминия хлоридом при 430 нм;
W - потеря в массе при высушивании сырья, в процентах;
m - масса навески сырья, в граммах [7,132].
Метод 2 для сырья и препаратов, где доминируют гликозидированные формы флавоноидов.
А) Если имеется СО любого гликозида, его используют в качестве раствора сравнения с определением оптической плотности при одинаковых lmax (указаны в таблице), либо строят калибровочный график по растворам СО.
Около 3 г (точная навеска) измельченного сырья помещают в круглодонную колбу вместимостью 100 мл, прибавляют 50 мл спирта этилового 50%, нагревают на кипящей водяной бане в течение 2 часов, охлаждают, фильтруют.
25 мл фильтрата переносят в мерную колбу вместимостью 100 мл, доводят объем спиртом этиловым 50% до метки, перемешивают.
Оптическую плотность раствора измеряют на спектрофото-метре при длине волны 365 нм в кювете с толщиной слоя 10 мм, используя в качестве раствора сравнения спирт этиловый 50%.
Параллельно измеряют оптическую плотность 0.1% раствора СО гиперозида при длине волны 365 нм.
Содержание суммы флавоноидов в пересчете на гиперозид и абсолютно сухое сырье в процентах (X) вычисляют по формуле:
|
D0 . m . 25 . (100 - W)
где D - оптическая плотность исследуемого раствора;
