Применение первого начала термодинамики к изопроцессам
1) изохронный процесс (V=const). При изохронном процессе газ не совершает работы под внешними телами, т.е. 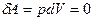 .
.
Из I закона термодинамики: 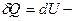 вся теплота, сообщаемая газу, идет на увеличение внутренней энергии.
вся теплота, сообщаемая газу, идет на увеличение внутренней энергии.
Внутренняя энергия: 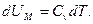 Для произвольной массы:
Для произвольной массы:
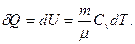 | (1.20) |
2) изобарный процесс (p=const). Работа газа при увеличении объема от V1 до V2:
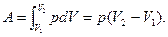 (1.21)
(1.21)
1Если использовать уравнение Клапейрона - Менделеева для двух состояний V2-V1: 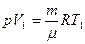 и
и 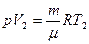 , тогда (1.21) примет вид:
, тогда (1.21) примет вид:
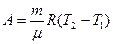 | (1.22) |
Количество теплоты:
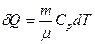 | (1.23) |
Внутренняя энергия:
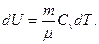 | (1.24) |
3) изотермический процесс(T=const). Внутренняя энергия не изменяется: 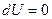 . Из первого закона термодинамики следует:
. Из первого закона термодинамики следует:
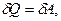 | (1.25) |
т.е. все тепло, полученное системой, расходуется на совершение работы против внешних сил. Работа газа при изотермическом расширении:
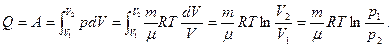 | (1.26) |
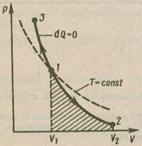 Рис. 1.4. Адиабата и изотерма. Рис. 1.4. Адиабата и изотерма. | 4) адиабатический процесс – проходит без теплообмена с окружающей средой (δQ=0). Из первого закона термодинамики: 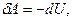 (1.27) т.е. внешняя работа совершается за счет убыли внутренней энергии. Адиабатический процесс описывается уравнением Пуассона: (1.27) т.е. внешняя работа совершается за счет убыли внутренней энергии. Адиабатический процесс описывается уравнением Пуассона: |
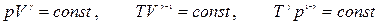 | (1.28) |
Работа при адиабатическом расширении:
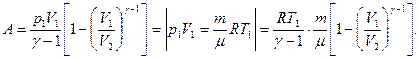 | (1.29) |
Порядок выполнения работы
Упражнение №1
Изотермический процесс
1. Включите компьютер. Загрузите пакет «Открытая физика 2.5» часть 1.
2. Кликните левой кнопкой компьютерной мыши в содержании раздел «Молекулярная физика и термодинамика» на любую строку.
3. В верхнем правом углу расположено меню, которое содержит теорию, вопросы, задачи, задачи с решениями, лабораторные работы, журнал. Кликните мышью раздел «Лабораторные работы» (весы).
4. Перед Вами лабораторная работа №3.1.
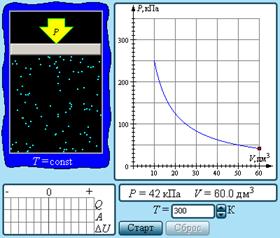 |
5. На рисунке изображен газ, помещенный в цилиндр под поршень. Нажмите «Старт». Пронаблюдайте поведение молекул газа. Нажмите «Стоп». Справа от рисунка находятся параметр – температура, который можно изменять. Выше расположены параметры давление и объем. Под рисунком приведена диаграмма изменения теплоты, работы и внутренней энергии. Справа от рисунка расположена изотерма. При изменении значения температуры, видно, что изотерма меняет свое положение на координатной плоскости и изогнутость.
6. Нажмите кнопку «Сброс». Установите параметры по указанию преподавателя. Нажмите «Старт».
7. Пронаблюдайте процесс расширения и сжатия газа.
8. Повторите моделирование несколько раз (по указанию преподавателя).
9. Зарисуйте рисунок в тетрадь, запишите полученные результаты, либо распечатайте результат на принтере.
10. Ответьте на вопросы и решите задачи, расположенные в правой половине экрана.
11. Дома проработайте модель 3.6 из раздела «Модели».
Упражнение №2
Изохорный процесс
1. Включите компьютер. Загрузите пакет «Открытая физика 2.5» часть 1.
2. Кликните левой кнопкой компьютерной мыши в содержании раздел «Молекулярная физика и термодинамика» на любую строку.
3. В верхнем правом углу расположено меню, которое содержит теорию, вопросы, задачи, задачи с решениями, лабораторные работы, журнал. Кликните мышью раздел «Лабораторные работы» (весы).
4. Перед Вами лабораторная работа №3.2.
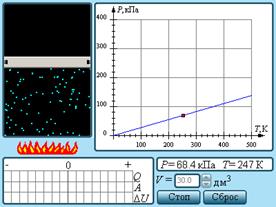 |
5. На рисунке изображен газ, помещенный в цилиндр под поршень. Нажмите «Старт». Пронаблюдайте поведение молекул газа. Нажмите «Стоп». Справа от рисунка находятся параметр – объем, который можно изменять. Выше расположены параметры давление и температура. Под рисунком приведена диаграмма изменения теплоты, работы и внутренней энергии. Справа от рисунка расположена изохора. При изменении значения температуры, видно, что изотерма меняет свое положение на координатной плоскости.
6. Нажмите кнопку «Сброс». Установите параметры по указанию преподавателя. Нажмите «Старт».
7. Пронаблюдайте процесс расширения и сжатия газа.
8. Повторите моделирование несколько раз (по указанию преподавателя).
9. Зарисуйте рисунок в тетрадь, запишите полученные результаты, либо распечатайте результат на принтере.
10. Ответьте на вопросы и решите задачи, расположенные в правой половине экрана.
11. Дома проработайте модель 3.7 из раздела «Модели».
Упражнение №3
Изобарный процесс
1. Включите компьютер. Загрузите пакет «Открытая физика 2.5» часть 1.
2. Кликните левой кнопкой компьютерной мыши в содержании раздел «Молекулярная физика и термодинамика» на любую строку.
3. В верхнем правом углу расположено меню, которое содержит теорию, вопросы, задачи, задачи с решениями, лабораторные работы, журнал. Кликните мышью раздел «Лабораторные работы» (весы).
4. Перед Вами лабораторная работа №3.3.
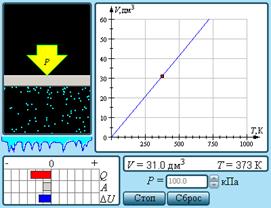 |
5. На рисунке изображен газ, помещенный в цилиндр под поршень. Нажмите «Старт». Пронаблюдайте поведение молекул газа. Нажмите «Стоп». Справа от рисунка находятся параметр – давление, который можно изменять. Выше расположены параметры объем и температура. Под рисунком приведена диаграмма изменения теплоты, работы и внутренней энергии. Справа от рисунка расположена изохора. При изменении значения температуры, видно, что изотерма меняет свое положение на координатной плоскости.
6. Нажмите кнопку «Сброс». Установите параметры по указанию преподавателя. Нажмите «Старт».
7. Пронаблюдайте процесс расширения и сжатия газа.
8. Повторите моделирование несколько раз (по указанию преподавателя).
9. Зарисуйте рисунок в тетрадь, запишите полученные результаты, либо распечатайте результат на принтере.
10. Ответьте на вопросы и решите задачи, расположенные в правой половине экрана.
11. Дома проработайте модель 3.8 из раздела «Модели».
12. Кликните мышью «Журнал». Обнулите результаты в таблице, нажав кнопку «Сброс результатов».
13. Проведите минитестирование. Ответьте на вопросы из раздела «Вопросы» и решите задачи из раздела «Задачи». Результат сообщите преподавателю.
14. Напишите вывод.
3. Контрольные вопросы
1. Дайте определение идеального газа.
2. Сформулируете законы Бойля-Мариотта, Гей-Люссака, Шарля, Авогадро, Дальтона.
3. Уравнение состояния идеального газа. Универсальная газовая постоянная.
4. Внутренняя энергия системы как функция состояния. Количество теплоты.
5. Первое начало термодинамики.
6. Теплоемкость.
7. Уравнения Майера, Пуассона.
8. Применение первого начала термодинамики к изопроцессам.
Лабораторная работа № 7
