Газовая (жидкостная и газоадсорбционная) хроматография
Сущность метода. понятие о теории метода. Параметры удерживания. Параметры разделения (степень разделения, коэффициент разделения, число теоретических тарелок). Методы количественной обработки хроматограмм (абсолютной калибровки, внутренней нормализации, внутреннего стандарта).
Это процесс разделения компонентов смеси, основанный на различии в равновесном распределении компонентов между 2 фазами – газом-носителем (ПФ) и либо твёрдой фазой, либо жидкостью, нанесённой в виде тонкой плёнки на поверхность твёрдого носителя или стенки хроматографической колонки (жидкая неподвижная, жидкая стационарная фаза). В первом случае это газоадсорбционная хроматографией, в втором газожидкостной.
• сущность метода – анализируемая смесь летучих компонентов переводится в пар, который смешивается с потоком инертного газа-носителя, образуя с ним ПФ. Смесь эта проталкивается далее новой порцией непрерывно подаваемого газа-носителя и попадает в хроматографическую колонну, заполненную НФ. Разделяемые компоненты распределяются между ПФ и НФ в соответствии с их коэффициентами распределения К, определяемыми формулой К = с(НФ)/ с (ПФ). Равновесный обмен хроматографируемого вещества между НФ и ПФ осуществляется в результате многократного повторения актов сорбция « десорбция по мере движения ПФ вдоль НФ. . причем поток газа-носителя тянет за собой парообразную смесь вдоль колонны, так что процессы сорбция « десорбция повторяются многократно, с установлением равновесия до тех пор, пока пары веществ не покинут колонну вместе с носителем. Так как сродство различных веществ к НФ различно, то они в процессе сорбция « десорбция задерживаются неодинаковое время. И чем выше температура кипения и относительная растворимость вещества в НФ, тем дольше оно находится в НФ.
Если для 2 компонентов коэффициенты распределения одинаковы, то они не разделяются.
Пары компонентов весте с газом-носителем поступают в детектор хроматографа, генерирующий электрический сигнал, который зависит от концентрации. Сигнал этот записывается в виде хроматограммы.
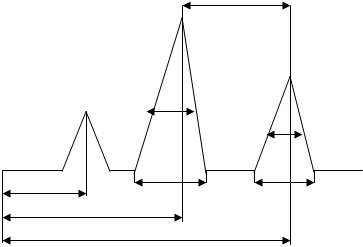
Понятие о теории метода – Хроматограмма – это зарегистрированная во времени последовательность показаний регистратора. Каждому разделённому компоненту смеси соответствует свой пик на хроматограмме. По очи абсцисс откладывается время, по оси ординат – величина аналитического сигнала, которая зависит от концентрации данного компонента в смеси.
Время удерживания – качественная характеристика каждого компонента; измеряется с момента ввода пробы до момента выхода максимума. Оно зависит от природы хроматографируемого вещества и газа-носителя, скорости прохождения ПФ через хроматографическую колонну, от природы и массы НФ, температуры, длины колонны. И чем больше коэффициент распределения хроматографируемого вещества, те больше и время удерживания.
Время выхода – несорбируемого компонента определяется соотношением t = L/n
Где L – длина хроматографической колонки, n - линейная скорость движения потока газа-носителя.
Исправленное время удерживания - t¢ соответственно компонентов 1 и 2
t¢1 = t1 - t0 t¢2 = t2 - t0 это время, в течение которого компонент находится в НФ. Оно пропорционально коэффициенту распределения данного компонента разделяемой смеси.
Относительное время удерживания и относительное исправленное время удерживания определяются по формулам:
t¢ = t t¢r = t - t0
tS t S - t0
Относительное время удерживания меньше зависит от внешних условий чем время удерживания.
Расстояние удерживания: оно пропорционально времени удерживания.
Объём удерживания: она равен объему ПФ, который выносит из колонки все данное вещество. Он зависит от скорости движения ПФ и равен произведению времени удержания на эту скорость: V = t•n
Коэффициент удерживания – это соотношение скорости перемещения данного компонента вдоль хроматографической колонки к скорости движения потока газа-носителя: R = w / n
Коэффициент емкости: он равен соотношению исправленного времени удерживания данного компонента к t0. k = (t - t0) / t0.
Параметры разделения:
Степень разделения: количественно характеризует разделение двух пиков на хроматограмме и рассчитывается по формуле
R S = 2 Dt = Dt
A (1) + a(2) a(1) ½ + a(2) ½
Коэффициент разделения: характеризует селективность НФ по отношению к двум данным компонентам и относительное расположение разделяемых пиков на хроматограмме.
a = t2 -t0 = K2
t1 -t0 K1
Коэффициент разделения и степень разделения связаны соотношением
R = a - 1 • n1/2
a 4
Где n – число теоретических тарелок . теоретическая тарелка это участок зоны внутри колонки, на котором устанавливается равновесное распределение данного веществу между ПФ и НФ, разделяемое вещество как бы распределяется по этим тарелкам.
Рассчитывается по формуле: n = 5,545• (t / a ½ )2
Метода абсолютной градуировки: Готовят серию i- эталонных растворов с точно известной концентрацией определяемого вещества в анализируемом растворе. записывают хроматограммы каждого раствора в одинаковых условиях и проводят измерение площади пика определяемого вещества на каждой хроматограмме и строят градуировочный график в координатах. Потом в тех же условиях хроматографируют пробу неизвестного раствора и проводят сравнение.
Метод внутренней нормализации: На одной и той же хроматограмме измеряют площади всех пиков и определяют их сумму, считая что элюируются все компоненты анализируемой пробы, так что ни один из компонентов не остается прочно связанным в хроматографической колонке. Поскольку согласно формуле S = km площадь пика любого компонента прямо пропорциональна массе этого компонента в разделяемой смеси, то рассчитывают массовую долю в процентах данного компонента
по формуле:
WX = SX • 100%
S Si
Данный метод очень распространен. Пики всех разделяемых компонентов получаются на одной и той же хроматограмме.
Метод внутреннего стандарта: Готовят как правило 5 эталонных смесей, каждая из которых включает точно известную массу определяемого компонента и массу стандарта. В строго одинаковых условиях хроматографируют каждую смесь и на полученных хроматограммах измеряю площади пиков определяемого вещества и площадь стандарта. А так как площадь пика на хроматограмме прямо пропорциональна массе данного вещества: Si = kimi Scn = k2mct
Si = ki mi = k mi
Sст k2 mct mct
Затем к анализируемого раствору содержащему неизвестную массу определяемого вещества, прибавляют точно известную массу стандарта и хроматографируют полученный раствор в тех же условиях, что и эталонные растворы, после чего проводят сравнение площади обоих пиков. По полученным данным вычисляют соотношение Sx/Sст
