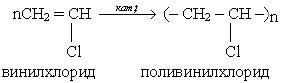Решение: в условии ошибка! Как может из 10 г раствора выделиться 400 г соли! АБСУРД!!! Допустим, что в условии дано 10 кг раствора.
Найдем массу соли в растворе до охлаждения:
m (соли) = 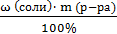 =
= 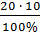 = 2 (кг).
= 2 (кг).
Найдем массу соли после охлаждения:
m' (соли) = m (соли) – m (осадка) = 2 – 0,4 = 1,6 (кг).
Найдем массу раствора после охлаждения:
m' (р-ра) = m (р-ра) – m (осадка) = 10 – 0,4 = 9,6 (кг)
Находим новую массовую долю:
ω (соли) = 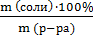 =
= 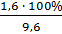 = 16,67 (%).
= 16,67 (%).

Решение: в железо-никелевом акккумуляторе анодом служит железо, катодом – гидроксид никеля (III). В качестве электролита используют раствор КОН.
При разрядке аккумулятора происходит окисление железа и восстановление гидроксида никеля (III):
А: Fe – 2e- + 2OH- → Fe(OH)2
K: 2Ni(OH)3 + 2e- → 2Ni(OH)2 + 2OH-
При зарядке протекают противоположные процессы.

Решение: из закона Фарадея выразим молярную массу эквивалента кадмия:
m (Cd) = 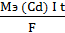
MЭ (Cd) = 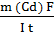 =
= 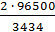 = 56 (г-экв./моль).
= 56 (г-экв./моль).

Решение: цинк и железо – более активные металлы, чем медь, поэтому они будут вытеснять ее из раствора соли:
Zn – 2e- → Zn2+
Cu2+ + 2e- → Cu0
Суммарно:
Zn + Cu2+ = Cu + Zn2+
Fe – 2e- → Fe2+
Cu2+ + 2e- → Cu0
Суммарно:
Fe + Cu2+ = Cu + Fe2+
Если соединить проводником концы пластинок, образуется гальванический элемент, в котором цинк будет анодом, железо – катодом:
А: Zn0 – 2e- → Zn2+
K: Cu2+ + 2e- → Cu0
На катоде будет осаждаться медь, а материал анода будет растворяться.

Решение: очень важное свойство вольфрама – тугоплавкость. Благодаря этому он применяется в качестве нити накаливания в осветительных приборах. Также применяется в качестве электродов при аргонодуговой сварке. Также на основе вольфрама делают износостойкие сплавы, применяемые в контактной части рубильников, выключателей и т.п.

Решение: определим массы металлов, входящих в состав сплава:
m (Sn) = n (Sn) ∙ M (Sn) = 0,3 ∙ 119 = 35,7 (г).
m (Cd) = n (Cd) ∙ M (Cd) = 0,1 ∙ 112 = 11,2 (г).
m (Zn) = n (Zn) ∙ M (Zn) = 0,2 ∙ 65 = 13 (г).
m (Al) = n (Al) ∙ M (Al) = 0,4 ∙ 27 = 10,8 (г).
Находим общую массу сплава и массовые доли металлов:
m (сплава) = m (Sn) + m (Cd) + m (Zn) + m (Al) =
= 35,7 + 11,2 + 13 + 10,8 = 70,7 (г).
ω (Sn) =  =
=  = 50,5 (%).
= 50,5 (%).
ω (Cd) = 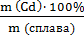 =
= 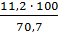 = 15,8 (%).
= 15,8 (%).
ω (Zn) = 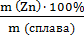 =
=  = 18,4 (%).
= 18,4 (%).
ω (Al) = 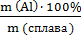 =
= 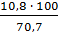 = 15,3 (%).
= 15,3 (%).

Решение: особенной устойчивостью к повышенным температурам обладают оксиды титана, особенно TiO2. Его применяют в качестве добавки в керамику, которая идет на производство температуростойких кондесаторов.

Решение: рабочим телом для активных оптических квантовых генераторов (лазеров) является кристалл рубина в виде стержня цилиндрической формы, со строго параллельными тщательно отшлифованными торцами (образуют зеркальный резонатор). Один торец покрыт толстым слоем серебра и непрозрачен для света. Толщину покрытия другого торца подбирают таким образом, чтобы оно было полупрозрачным для испускаемого лазером излучения. Длина стержня ограничена. Использование рубина длиной более 30 см не целесообразно, т.к. усложняется накачка атомов и фокусировка излучения.
Сам рубин состоит из оксида алюминия (Al2O3), в котором небольшая часть атомов алюминия (≈ 0,05%) замещена на Cr3+. Именно наличие катионов хрома придает этому материалу специфические свойства, нашедшие применение в лазерной технике.

Решение: уравнение получение поливинилхлорида: