Молекулярная физика и термодинами ка
Основные формулы
Количество вещества (число молей) системы:
n = N/NA ,
где N– число (молекул, атомов, ионов и т. п.), составляющих тело (систему); NA– постоянная Авогадро (NА=6,02×1023 моль-1). Молярная масса вещества
М = m/n,
где m – масса тела; n – количество вещества этого тела.
Относительная молекулярная масса вещества
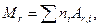
где ni – число атомов i-ro химического элемента, входящих в состав молекулы данного вещества; Аr,i– относительная атомная масса этого элемента. Количество вещества – число структурных элементов (молекул, атомов, ионов и т. п.), содержащихся в теле или системе. Количество вещества выражается в молях. Моль равен количеству вещества системы, содержащей столько же структурных элементов, сколько содержится атомов в углероде-12 массой 0,012 кг. Атомные массы приводятся в таблице Д. И. Менделеева. (См. также табл. 6 приложения).
Связь молярной массы М сотносительной молекулярной массой вещества.
М = Mrk,
где k=10-3 кг/моль.
Количество вещества смеси газов
n=n1+n2+…+ nn=N1/NA+ N2/NA+…+ Nn/NA
или
n=m1/M1+ m2/M2+…+ mn/Mn
гдеn i – количество вещества,. Ni - число молекул, mi - масса, Mi - молярная масса i-гoкомпонента смеси.
Уравнение Менделеева – Клапейрона (уравнение состояния идеального газа)
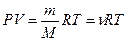 ,
,
где т – масса газа, М – молярная масса газа, R – универсальная газовая
– 35 –
постоянная 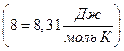 , n – количество вещества, Т – абсолютная термодинамическая температура.
, n – количество вещества, Т – абсолютная термодинамическая температура.
Опытные газовые законы, являющиеся частными случаями уравнения Менделеева – Клапейрона для изопроцессов:
а) закон Бойля – Мариотта (изотермический процесс: T=const, m=const)
pV = const, или для двух состояний газа p1V1=p2V2
б) закон Гей-Люссака (изобарный процесс: р = const, m=const)
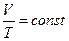
 или для двух состояний
или для двух состояний 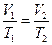
в) закон Шарля (изохорный процесс: V=const, m=const)
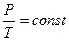 , или для двух состоянии
, или для двух состоянии 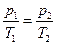
г)объединенный газовый закон (m=const)
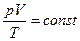 , или
, или 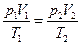
где p1, V1, T1 – давление, объем и температура газа в начальном состоянии; р2, V2, Т2 – те же величины в конечном состоянии.
Закон Дальтона, определяющий давление смеси газов, p=p1+p2+…+pn,
где pi– парциальные давления компонентов смеси, п — число компонентов смеси.
Парциальным давлением называется давление газа, которое производил бы этот газ, если бы только он один находился в сосуде, занятом смесью.
Молярная масса смеси газов
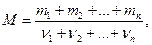
где mi – масса i-гo компонента смеси; 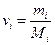 – количество вещества i-гo компонента смеси; п – число компонентов смеси.
– количество вещества i-гo компонента смеси; п – число компонентов смеси.
Массовая доля i-го компонента смеси газа (в долях единицы или процентах)
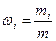
где m– масса смеси. Концентрация молекул
– 36 –
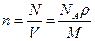
где N– число молекул, содержащихся в данной системе, r – плотность вещества, V– объем системы. Формула справедлива не только для газов, но и для любого агрегатного состояния вещества.
Основное уравнение кинетической теории газов
р = 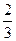 п <e> ,
п <e> ,
где <e> – средняя кинетическая энергия поступательного движения молекулы.
Средняя кинетическая энергия поступательного движения молекулы
<e>= 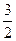 kT
kT
где k– постоянная Больцмана 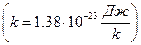 .
.
Средняя полная кинетическая энергия молекулы
<ei> = 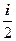 kT
kT
где i – число степеней свободы молекулы.
Зависимость давления газа от концентрации молекул и температуры
р = nkT.
Скорости молекул:
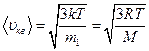 – средняя квадратичная;
– средняя квадратичная; 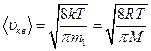 – средняя арифметическая;
– средняя арифметическая; 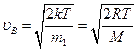 – наиболее вероятная,
– наиболее вероятная,
где mi – масса одной молекулы. Относительная скорость молекулы 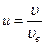 ,
,
где  – скорость данной молекулы.
– скорость данной молекулы.
Удельные теплоемкости газа при постоянном объеме (cV) и постоянном давлении (cр)
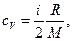
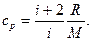
Связь между удельной с и молярной Степлоемкостями
– 37 –
С = сМ.
Уравнение Майера
Cp – Cv = R.
Среднее число столкновений молекул за 1 секунду определяется формулой:
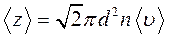 ,
,
где 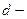 диаметр молекул,
диаметр молекул, 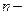 концентрация молекул,
концентрация молекул, 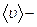 средняя арифметическая скорость.
средняя арифметическая скорость.
Средняя длина свободного пробега молекул 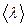 можно вычислить по формуле:
можно вычислить по формуле:
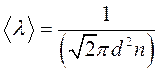
Внутренняя энергия идеалыюго газа
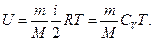
Первое начало термодинамики
Q=DU+A,
где Q–теплота, сообщенная системе (газу) ; DU – изменение внутренней
энергии системы; A– работа, совершенная системой против внешних сил. Работа расширения газа:
1) вобщем случае: 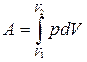
2) A = p(V2 – V1 )–при изобарном процессе;
3) при изотермическом процессе: 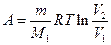
4) при адиабатном процессе: 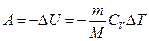
Уравнения Пуассона, связывающие параметры идеального газа при адиабатном процессе:
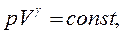
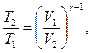
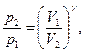
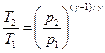
– 38 –
КПД цикла:
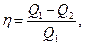
где Q1 – теплота, полученная рабочим телом от теплоотдатчика; Q2 – теплота, переданная рабочим телом теплоприемнику.
Термический КПД цикла Карно (идеального теплового двигателя):
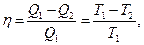
где T1и T2–термодинамические температуры теплоотдатчика и тепло-приемника.
Коэффициент поверхностного натяжения:
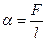 или
или 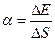
где F– сила поверхностного натяжения, действующая на контур l, ограничивающий поверхность жидкости, DЕ – изменение свободной энергии поверхностной пленки жидкости, связанное с изменением площади DS поверхности этой пленки.
Формула Лапласа, выражающая давление р, создаваемое сферической поверхностью жидкости:
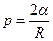 ,
,
где R – радиус сферической поверхности.
Высота подъема жидкости в капиллярной трубке
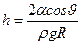 ,
,
где q – краевой угол (q=0 при полном смачивании стенок трубки жидкостью; q=p при полном несмачивании); R – радиус канала трубки; r – плотность жидкости, g– ускорение свободного падения.
Высота подъема жидкости между двумя близкими параллельными друг другу плоскостями
– 39 –
где d– расстояние между плоскостями.
Примеры решения задач
Пример 1. Определить для серной кислоты: 1) относительную молекулярную массу Мr; 2) молярную массу М.
Решение. 1. Относительная молекулярная масса вещества равна сумме относительных атомных масс всех элементов, атомы которых входят в состав молекулы данного вещества, и определяется по формуле
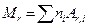 (1)
(1)
где ni – число атомов i-го элемента, входящих в молекулу; Ar,i– относительная атомная масса i-гo элемента.
Химическая формула серной кислоты имеет вид H2SO4. Так как в состав молекулы серной кислоты входят атомы трех элементов, то стоящая в правой части равентсва (1) сумма будет состоять из трех слагаемых и эта формула примет вид
Мr=n1Ar,1+ п2Аr,2+п3Аr,3 (2)
Из формулы серной кислоты далее следует, что n1=2 (два атома водорода), n2=1 (один атом серы) и nз=4 (четыре атома кислорода). Значения относительных атомных масс водорода, серы кислорода найдем в таблице Д. И. Менделеева или табл. 6 приложения:
Ar,1= 1, Ar,2 = 32, Аr,3= 16.
Подставив значения n1 и Ar,i в формулу (2), найдем относительную молекулярную массу серной кислоты:
Мr= 2 1+1×32+4×16=98.
2. Зная относительную молекулярную массу Мr, найдем молярную массу серной кислоты по формуле
М = Mrk, (3)
где k=10-3 кг/моль.
Подставив в (3) значения величин, получим M=98×10-3 кг/моль.
– 40 –
Пример 2. Определить молярную массу М смеси кислорода массой m1=25 и азота массой m2=75г.
Решение. Молярная масса смеси М есть отношение массы смеси m к количеству вещества смеси n:
M = m/n. (1)
Масса смеси равна сумме масс компонентов смеси:
т = m1+m2
Количество вещества смеси равно сумме количеств вещества компонентов:
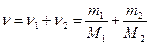
Подставив в формулу (1) выражения m и n, получим
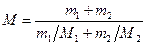 (2)
(2)
Молярные массы кислорода M1и азота М2 равны:
М1 = 32×10-3 кг/моль; М2 = 28×10-3 кг/моль.
Подставим значения величин в (2) и произведем вычисления:
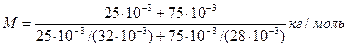 = 28,9×10-3 кг/моль.
= 28,9×10-3 кг/моль.
Пример 3. Определить число Nмолекул, содержащихся в объеме
V=1 мм3 воды, и массу m1 молекулы воды. Считая условно, что молекулы воды имеют вид шариков, соприкасающихся друг с другом, найти диаметр d молекул.
Решение: Число Nмолекул, содержащихся в некоторой системе массой m, равно произведению постоянной Авогадро NAна количество вещества n:
N = n / na
Так как n=m/M, где М — молярная масса, то 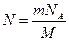
Выразив в этой формуле массу как произведение плотности на объем V, получим N =rVNA/M.
– 41 –
Произведем вычисления, учитывая, что M=18×10-3 кг/моль (см. табл. 6 приложения):
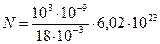 молекул = 3,34×1019 молекул
молекул = 3,34×1019 молекул
Массу m1 одной молекулы можно найти по формуле
m1 =m/na(1).
Подставив в (1) значения М и NA, найдем массу молекулы воды:
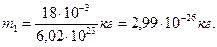
Если молекулы воды плотно прилегают друг к другу, то можно считать, что на каждую молекулу приходится объем (кубическая ячейка) V1=d3, где d — диаметр молекулы. Отсюда
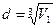 (2)
(2)
Объем V1найдем, разделив молярный объем Vmначисло молекул в моле, т.е. на na:
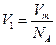 (3)
(3)
Подставим выражение (3) в (2):
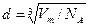 ,где Vm=M/r. Тогда
,где Vm=M/r. Тогда
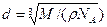 (4)
(4)
Проверим, дает ли правая часть выражения (4) единицу длины:
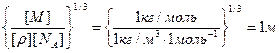
Произведем вычисления:
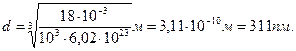
– 42 –
Пример 4. В баллоне объемом 10 л находится гелий под давлением р1= 1 МПа и при температуре Т1=300К. После того как из баллона было взято m=10г гелия температура в баллоне понизилась до T2 = 290К. Определить давление р2гелия, оставшегося в баллоне.
Решение. Для решения задачи воспользуемся уравнением Менделеева - Клапейрона, применив его к конечному состоянию газа:
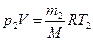 (1)
(1)
где т2 — масса гелия в баллоне в конечном состоянии; M — молярная масса гелия; R— молярная газовая постоянная.
Из уравнения (1) выразим искомое давление:
P2= m2RT2/(MV). (2)
Массу т2 гелия выразим через массу т1, соответствующую начальному состоянию, и массу т гелия, взятого из баллона:
m2=ml - т. (3)
Массу т1гелия найдем также из уравнения Менделеева — Клапейрона, применив его к начальному состоянию:
m1 = MP1V/(RT1). (4)
Подставив выражение массы т1 в (3), а затем выражение т2 из(2) в (3), найдем
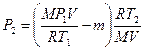
или
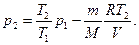 (5)
(5)
Проверим, дает ли формула (5) единицу давления. Для этого в ее правую часть вместо символов величин подставим их единицы. В правой части формулы два слагаемых. Очевидно, что первое из них дает единицу давления, так как состоит из двух множителей, первый из которых (Т2/Т1) — безразмерный, а второй — давление. Проверим второе слагаемое:
– 43 –
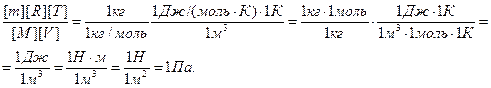
Паскаль является единицей давления. Произведем вычисления по формуле (5) , учитывая, что М= 4×10-3 кг/моль (см. табл. 6 приложения):
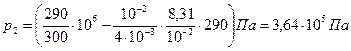 = 0,364 МПа.
= 0,364 МПа.
Пример 5.Баллон содержит т1 = 80 г кислорода и m2 = 320 г аргона. Давление смеси р=1МПа, температура Т = 300 К. Принимая данные газы за идеальные определить объем V баллона.
Решение. По закону Дальтона, давление смеси равно сумме парциальных давлений газов, входящих в состав смеси. По уравнению Менделеева — Клапейрона, парциальные давления р1 кислорода и р2 аргона выражаются формулами:
P1 = m1RT/(M1V), p2 = m2RT/(M2V).
Следовательно, по закону Дальтона, давление cмеси газов
p=p1+p2, или 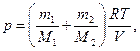
откуда объем баллона
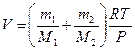 (1)
(1)
Произведем вычисления, учитывая, что M1=32×10-3 кг/моль, M2=40×10-3 кг/моль (см. табл. 6 приложения):
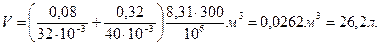
Пример 6. Найти среднюю кинетическую энергию <eвр> вращательного движения одной молекулы кислорода при температуре Т=350 К, а также кинетическую энергию Eк вращательного движения всех молекул кислорода массой m = 4 г.
– 44 –
Решение. На каждую степень свободы молекулы газа приходится одинаковая средняя энергия <ei> = ½ kT,
где k— постоянная Больцмана; Т — термодинамическая температура газа. Так как вращательному движению двухатомной молекулы (молекула кислорода - двухатомная) соответствуют две степени свободы, средняя энергия вращательного движения молекулы кислорода
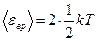 , (1)
, (1)
Кинетическая энергия вращательного движения всех молекул газа
Ек= <eвр>N(2)
Число всех молекул газа
N=NAn, (3)
NA — постоянная Авогадро; n — количество вещества.
Если учесть, что количество вещества n = т/М, где m — масса газа; М — молярная масса газа, то формула примет вид
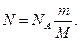
Подставив выражение N в формулу (2), получаем
Ек= NAm <eвр>/M (4)
Произведем вычисления, учитывая, что для кислорода M=32×10-3 кг/моль (см. табл. 6 приложения):
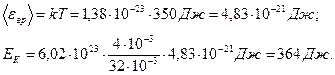
Пример 7. Вычислить удельные теплоемкости при постоянном объеме сV и при постоянном давлении cp неона и водорода, принимая эти газы за идеальные.
Решение. Удельные теплоемкости идеальных газов; выражаются формулами
– 45 –
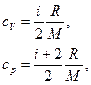
где i — число степеней свободы молекулы газа; М — молярная масса. Для неона (одноатомный газ) i=3 и М=20×10-3 кг/моль (см. табл. 6 приложения).
Произведем вычисления:
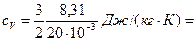 6,24×102 Дж/(кг×К);
6,24×102 Дж/(кг×К);
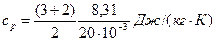 =1,04×103 Дж/(кг×К).
=1,04×103 Дж/(кг×К).
Для водорода (двухатомный газ) i=5 и M=2×10-3 кг/моль. Тогда
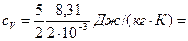 1,04×104 Дж/(кг×К);
1,04×104 Дж/(кг×К);
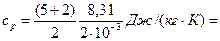 1,46×104 Дж/(кг×К)
1,46×104 Дж/(кг×К)
Пример 8. Вычислить удельные теплоемкости cV и сp смеси неона и водорода, если массовые доли неона и водорода составляют w1=80% и w2=20%. Значения удельных теплоемкостей газов взять из предыдущего примера.
Решение. Удельную теплоемкость cV смеси при постоянном объеме найдем следующим образом. Теплоту необходимую для нагревания смеси на DТ выразим двумя способами:
Q=cV(m1+m2)DT,
Q=(cV,1m1+cV,2m2)DT,
где cV,1 — удельная теплоемкость неона; cV,2 — удельная теплоемкость водорода.
Приравняв правые части (1) и (2) и разделив обе части полученного равенства на DТ, получим сV(m1+m2)=cV,1m1+cV,2m2. Отсюда
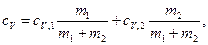
или
сV=cV,1w1+cV,2w2,
где 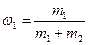 и
и 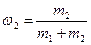 .
.
– 46 –
Рассуждая так же, получим формулу для вычисления дельной теплоемкости смеси при постоянном давлении:
cp=cp,1w1+cp,2w2
Произведем вычисления:
cV=(6,24×102×0,8+1,04×104×0,2)Дж/(кг×К)=2,58×103Дж/(кг×К) =2,58 кДж/(кг×К);
Cp=(l,04×103×0,8+1,46×104×0,2)Дж/(кг×К)=3,75×103 Дж/(кг×К)=3,75 кДж/(кг×К).
Пример 9. Кислород массой m=2кг занимает объем V1=1м3 и находится под давлением p1=0,2МПа. Газ был нагрет сначала при постоянном давлении до объема V2=3м3, а затем при постоянном объеме до давления р3=0,5МПа. Найти изменение DU внутренней энергии газа, совершенную им работу А и теплоту Q, переданную газу. Построить график процесса.
Решение. Изменение внутренней энергии газа
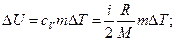 (1)
(1)
где i— число степеней свободы молекул газа (для двухатомных молекул кислорода i=5); DT=T3 -Т1 — разность температур газа в конечном (третьем) и начальном состояниях.
Начальную и конечную температуру газа найдем из уравнения Менделеева — Клапейрона pV= 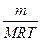 , откуда
, откуда
T=pVM/(mR).
Работа расширения газа при постоянном давлении выражается формулой
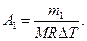
Работа газа, нагреваемого при постоянном объеме равна нулю:
A2=0.
Следовательно, полная работа, совершаемая газом,
А=А1+А2=А1.
Согласно первому началу термодинамики, теплота переданная газу, равна сумме изменения внутренней энергии DU и работы А:
– 47 –
Q=DU+A.
Произведем вычисления, учтя, что для кислорода M=32×10-3 кг/моль (см. табл. 6 приложения):
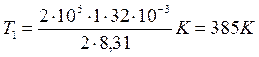 ;
;
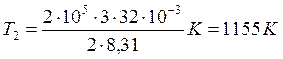 ;
;
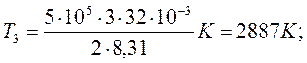
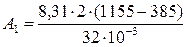 Дж = 0,400×106 Дж = 0,4 МДж;
Дж = 0,400×106 Дж = 0,4 МДж;
A=A1=0,4 МДж;
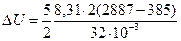 Дж=3,24×106Дж=3,24МДж;
Дж=3,24×106Дж=3,24МДж;
Q=(3,24+0,4)МДж=3,64МДж.
График процесса приведен на рис. 7.
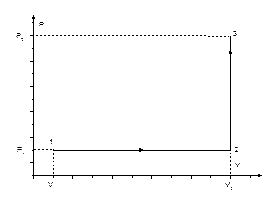
Рис. 7
Пример 10. В цилиндре под поршнем находится водород массой m=0,02кг при температуре T1=300K. Водород сначала расширился адиабатно, увеличив свой
– 48 –
объем в n1=5 раз, а затем был сжат изотермически, причем объем газа уменьшился в n2=5 раз. Найти температуру в конце адиабатного расширения и работу, совершаемую газом при этих процессах. Изобразите процесс графически.
Решение. Температуры и объемы газа, совершающего адиабатный процесс, связаны между собой соотношением
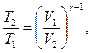 или
или 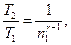
где g — отношение теплоемкостей газа при постоянном давлении и постоянном объеме; n1=V2/V1.
Отсюда получаем следующее выражение для конечной температуры:
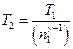
Работа А1 газа при адиабатном расширении может быть определена по формуле
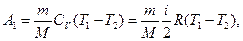
где СV — молярная теплоемкость газа при постоянном объеме. Работа А2 газа при изотермическом процессе может быть выражена в виде
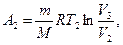 или
или 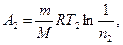
где n2= V2/Vз.
Произведем вычисления, учитывая, что для водорода как двухатомного газа g=1,4, i=5 и М=2×10-3кг/моль: 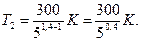
 Так как 50,4=1,91 (находится логарифмированием), то
Так как 50,4=1,91 (находится логарифмированием), то 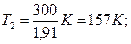
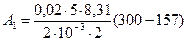 Дж = 29,8 кДж;
Дж = 29,8 кДж;
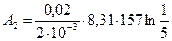 Дж=-21 кДж.
Дж=-21 кДж.
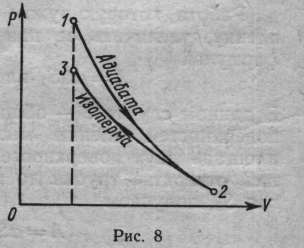
Знак минус показывает, что при сжатии работа газа совершается над газом внеш
– 49 –
ними силами. График процесса приведен на рис. 8.
Пример 11. Тепловая машина работает по обратимому циклу Карно. Температура теплоотдатчика Т1=500 К. Определить термический КПД h цикла и температуру Т2 теплоприемника тепловой машины, если за счет каждого кило джоуля теплоты, полученной от теплоотдатчика, машина совершает работу А=350Дж.
Решение. Термический КПД тепловой машин показывает, какая доля теплоты, полученной от теплоотдатчика, превращается в механическую работу. Термический КПД выражается формулой
h=A/Q1,
где Q1 — теплота, полученная от теплоотдатчика, А - работа, совершенная рабочим телом тепловой машины. Зная КПД цикла, можно по формуле
h=(T1 – T2)/T1 определить температуру охладителя Т2:
Произведем вычисления:
h = 350/1000 =0,35; T2 = 500( 1 - 0,35) К = 325 К.
Пример 12. Найти добавочное давление внутри мыльного пузыря диаметром d=10 cм. Какую работу нужно совершить, чтобы выдуть этот пузырь?
Решение. Пленка мыльного пузыря имеет две сферические поверхности: внешнюю и внутреннюю. Обе поверхности оказывают давление на воздух, заключенного внутри пузыря. Так как толщина пленки чрезвычайно мала, то диаметры обеих поверхностей практически одинаковы. Поэтому добавочное давление
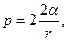
где 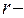 радиус пузыря. Так как r=d/2, то p = 8a/d.
радиус пузыря. Так как r=d/2, то p = 8a/d.
Работа, которую нужно совершить, чтобы, растягивая пленку, увеличить ее поверхность на DS, выражается формулой A = aDS, или A = a(S — So). В данном случае S — общая площадь двух сферических поверхностей пленки мыльного пузыря; So — общая площадь двух поверхностей плоской пленки, затягивавшей отверстие трубки до выдувания пузыря. Пренебрегая So, получаем
A=aS=2pd2a.
Произведем вычисления:
– 50 –
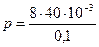 Па = 3,2 Па;
Па = 3,2 Па;
A=2×3,14×(0,1)2×40×10-3 Дж = 2,5×10-3 Дж = 2,5 мДж.
Контрольная работа 2
Таблица вариантов
| Вариант | Номера контрольных работ | |||||||
201.Определить количество вещества v и число Nмолекул кислорода массой m=0,5 кг.
202.Сколько атомов содержится в ртути: 1) количеством вещества n = 0,2 моль; 2) массой m=1 г?
203.Вода при температуре t=4°C занимает объем V=1см3. Определить количество вещества n и число Nмолекул воды.
204.Найти молярную массу Ми массу mм одной молекулы поваренной соли.
205.Определить массу mM одной молекулы углекислого газа.
206.Определить концентрацию пмолекул кислорода, находящегося в сосуде вместимостью V=2л. Количество вещества n кислорода равно 0,2моль.
207.Определить количество вещества n водорода, заполняющего сосуд объемом V=3л, если концентрация молекул газа в сосуде n=2×1018 м-3.
– 51 –
208.В баллоне вместимостью V=3л содержится кислород массой m=10г. Определить концентрацию молекул газа.
209.Определить относительную молекулярную массу Мr. 1) воды; 2) углекислого газа; 3) поваренной соли.
210.Определить количество вещества n и число N молекул азота массой т = 0,2 кг.
211.В цилиндр длиной l=1,6м, заполненный воздухом при нормальном атмосферном давлении р0, начали медленно вдвигать поршень площадью основания S= 200 см2. Определить силу F, действующую на поршень, если его остановить на расстоянии l1=10см от дна цилиндра.
212.В баллоне находится газ при температуре Т1=400К. До какой температуры Т2надо нагреть газ, чтобы его давление увеличилось в 1,5 раза?
213.Баллон вместимостью V=20л заполнен азотом при температуре 7=400 К. Когда часть газа израсходовали, давление в баллоне понизилось на Dp = 200кПа. Определить массу m израсходованного газа. Процесс считать изотермическим.
214.В баллоне вместимостью V=15л находится аргон под давлением р1=600кПа и при температуре T1 = 300 К. Когда из баллона было взято некоторое количество газа, давление в баллоне понизилось до p2= 400кПа, а температура установилась Т2=260 К. Определить массу mаргона, взятого из баллона.
215.Два сосуда одинакового объема содержат кислород. В одном сосуде давление р1 = 2 МПа и температура T1 = 800K, в другом р2 = 2,5 МПа, T2 = 200К. Сосуды соединили трубкой и охладили находящийся в них кислород до температуры T=200 К. Определить установившееся в сосудах давление р.
216.Вычислить плотность r азота, находящегося баллоне под давлением р=2МПа и имеющего температуру Т =400 К.
217.Определить относительную молекулярную массу Мrгаза, если при температуре T=154К и давлении р=2,8МПа он имеет плотность r=6,1 кг/м3.
218.Найти плотность азота r при температуре Т=400К и давлении р=2МПа.
219.В сосуде вместимостью V=40 л находится кислород при температуре T=300К. Когда часть газа израсходовали, давление в баллоне понизилось на
– 52 –
Dр=100кПа. Определить массу тизрасходованного кислорода. Процесс считать изотермическим.
220.Определить плотность r водяного пара, находящегося под давлением р=2,5кПа и имеющего температуру Т=250 К.
221.Определить внутреннюю энергию Uводорода, а также среднюю кинетическую энергию <e> молекулы этого газа при температуре Т = 300К, если количество вещества n этого газа равно 0,5 моль.
222.Определить суммарную кинетическую энергию EK поступательного движения всех молекул газа, находящегося в сосуде вместимостью V=3л под давлением p=540 кПа.
223. Количество вещества гелия n= 1,5 моль, температура Т= 120 К. Определить суммарную кинетическую энергию Eк поступательного движения всех молекул этого газа.
224. Молярная внутренняя энергия Umнекоторого двухатомного газа равна
6,02 кДж/моль. Определить среднюю кинетическую энергию <eвр> вращательного движения одной молекулы этого газа. Газ считать идеальным.
225. Определить среднюю кинетическую энергию <eвр> одной молекулы водяного пара при температуре Т =500 К.
226.Определить среднюю квадратичную скорость <vкв> молекулы газа, заключенного в сосуд вместимостью V=2л под давлением р=200кПа. Масса газа m=0,3г.
227.Водород находится при температуре T=300 К. Найти среднюю кинетическую энергию <eвр> вращательного движения одной молекулы, а также суммарную кинетическую энергию Eк всех молекул этого газа; количество водорода n=0,5моль.
228.При какой температуре средняя кинетическая энергия <eп> поступательного движения молекулы газа равна 4,14×10-21 Дж?
229.В азоте взвешены мельчайшие пылинки, которые движутся так, как если бы они были очень крупными молекулами. Масса каждой пылинки равна 6×10-10г. Газ находится при температуре T=400 К. Определить средние квадратичные скорости
– 53 –
<vкв> а также средние кинетические энергии <eп> поступательного движения молекулы азота и пылинки.
230.Определить среднюю кинетическую энергию <eп> поступательного движения и <eвр> вращательного движения молекулы азота при температуре Т= 400К. Определить также полную кинетическую энергию Eк молекулы при тех же условиях.
231.Определить молярную массу М двухатомной газа и его удельные теплоемкости, если известно, что разность ср— сVудельных теплоемкостей этого газа равна 260 Дж/(кг×К).
232..Найти удельные сри сV, а также молярные Сp и СVтеплоемкости углекислого газа.
233.Определить показатель адиабаты g идеального газа, который при температуре Т=350К и давлении р = 0,4 МПа занимает объем V = 300л и имеет теплоемкость CV=857 Дж/К.
234. В сосуде вместимостью V=6л находится при нормальных условиях двухатомный газ. Определить теплоемкость СVэтого газа при постоянном объеме.
235.Определить относительную молекулярную массу Мrи молярную массу Мгаза, если разность его удельных теплоемкостей ср— cV=2,08 кДж/(кг×К).
236.Определить молярные теплоемкости газа, если его удельные теплоемкости cV=10,4 кДж/(кг×К) и ср= 14,6 кДж/(кг×К).
237. Найти удельные cVи сри молярные СVи Сp теплоемкости азота и гелия.
238. Вычислить удельные теплоемкости газа, зная что его молярная масса М=4×10-3 кг/моль и отношения теплоемкостей Ср/СV=1,67.
239. Трехатомный газ под давлением р=240кПа и температуре t=20°Cзанимает объем V=10л. Определить теплоемкость Срэтого газа при постоянном давлении.
240. Одноатомный газ при нормальных условиях занимает объем V=5л. Вычислить теплоемкость этого газа при постоянном объеме.
241. Найти среднее число <z> столкновений за время t=1с и длину свободного пробега 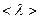 молекулы гелия, если газ находится под давлением р=2кПа при температуре T =200 К.
молекулы гелия, если газ находится под давлением р=2кПа при температуре T =200 К.
– 54 –
242.Определить среднюю длину свободного пробега 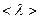 молекулы азота в сосуде вместимостью V=5л. Масса газа m = 0,5г.
молекулы азота в сосуде вместимостью V=5л. Масса газа m = 0,5г.
243. Водород находится под давлением р=20мкПа и имеет температуру T=300К. Определить среднюю длину свободного пробега 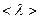 молекулы такого газа.
молекулы такого газа.
244. При нормальных условиях длина свободного пробега 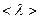 молекулы
молекулы
водорода равна 0,160 мкм. Определить диаметр dмолекулы водорода.
245. Какова средняя арифметическая скорость 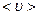 молекул кислорода при нормальных условиях, если известно, что средняя длина свободного пробега
молекул кислорода при нормальных условиях, если известно, что средняя длина свободного пробега 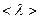 молекулы кислорода при этих условиях равна 100 нм?
молекулы кислорода при этих условиях равна 100 нм?
246. Кислород находится под давлением р=133нПа при температуре T=200К. Вычислить среднее число <z> столкновений молекулы кислорода при этих условиях за время t= 1 с.
247. При каком давлении рсредняя длина свободного пробега 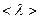 молекул азота равна 1м, если температура газа t=10°С?
молекул азота равна 1м, если температура газа t=10°С?
248. В сосуде вместимостью V=5л находится водород массой m=0,5г. Определить среднюю длину свободного пробега 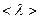 молекулы водорода в этом сосуде.
молекулы водорода в этом сосуде.
249. Средняя длина свободного пробега 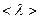 молекулы водорода при некоторых условиях равна 2мм. Найти плотность r водорода при этих условиях.
молекулы водорода при некоторых условиях равна 2мм. Найти плотность r водорода при этих условиях.
250. В сферической колбе вместимостью V=3л, содержащей азот, создан вакуум с давлением р=80мкПа. Температура газа T=250К. Можно ли считать вакуум в колбе высоким? Примечание. Вакуум считается высоким, если длина свободного пробега молекул в нем много больше линейных размеров сосуда.
251Определить количество теплоты Q, которое надо сообщить кислороду объемом V=50л при его изохорном нагревании, чтобы давление газа повысилось на Dр=0,5МПа.
251.При изотермическом расширении азота при температуре T=280К объем его увеличился в два раза. Определить: 1) совершенную при расширении газа работу A; 2) изменение DU внутренней энергии; 3) количество теплоты Q, полученное газом. Масса азота m=0,2кг.
252.При адиабатном сжатии давление воздуха было увеличено от р1=50кПа до
- 55 -
р2=0,5МПа. Затем при неизменном объеме температура воздуха была понижена до первоначальной. Определить давление р3газа в конце процесса.
254.Кислород массой m=200г занимает объем V1=100л и находится под давлением р1=200кПа. При нагревании газ расширился при постоянном давлении до объема V2=300л, а затем его давление возросло до р3=500кПа при неизменном объеме. Найти изменение внутренней энергии DU газа, совершенную газом работу A и теплоту Q, переданную газу. Построить график процесса.
255.Объем водорода при изотермическом расширении при температуре T=З00К увеличился в п=3раза. Определить работу А, совершенную газом, и теплоту Q, полученную при этом. Масса тводорода равна 200 г.
256.Азот массой m=0,1кг был изобарно нагрет от температуры T1=200К до температуры T2=400К. Определить работу А, совершенную газом, полученную им теплоту Qи изменение DU внутренней энергии азота.
257.Во сколько раз увеличится объем водорода, содержащий количество вещества n=0,4моль при изотермическом расширении, если при этом газ получит количество теплоты Q=800Дж? Температура водорода T=300К.
258.Какая работа Асовершается при изотермическом расширении водорода массой m=5г, взятого при температуре T=290К, если объем газа увеличивается в три раза?
259.Какая доля w1количества теплоты Q, подводимого к идеальному двухатомному газу при изобарном процессе, расходуется на увеличение DU внутренней энергии газа и какая доля w2 — на работу Арасширения? Рассмотреть три случая, если газ: 1) одноатомный; 2)двухатомный; 3) трехатомный.
260.Определить работу А, которую совершит азот, если ему при постоянном давлении сообщить количество теплоты Q=21кДж. Найти также изменение DU внутренней энергии газа.
261.Идеальный газ совершает цикл Карно при температурах теплоприемника T2=290К и теплоотдатчика Т1=400К. Во сколько раз увеличится коэффициент полезного действия h цикла, если температура теплоотдатчика возрастет до Т1= 600 К?
– 56 –
262.Идеальный газ совершает цикл Карно. Температура Т1теплоотдатчика в четыре раза (n = 4) больше температуры теплоприемника. Какую долю wколичества теплоты, полученного за один цикл от теплоотдатчика, газ отдаст теплоприемнику?
263.Определить работу А2изотермического сжатия газа, совершающего цикл Карно, КПД которого h=0,4, если работа изотермического расширения равна A1=8Дж.
264..Газ, совершающий цикл Карно, отдал теплоприемнику теплоту Q2=14кДж. Определить температуру Т1теплоотдатчика, если при температуре теплоприемника T2=280К работа цикла A=6кДж.
265.Газ, являясь рабочим веществом в цикле Карно, получил от теплоотдатчика теплоту Q1=4,38кДж и совершил работу А=2,4 кДж. Определить
температуру теплоотдатчика, если температура теплоприемника T2 =273 К.
266. Газ, совершающий цикл Карно, отдал теплоприемнику 67% теплоты, полученной от теплоотдатчика. Определить температуру T2 теплоприемника, если температура теплоотдатчика Т1=430 К.
267. Во сколько раз увеличится коэффициент полезного действия h цикла Карно при повышении температуры теплоотдатчика от Т1=380К до Т2=560 К? Температура теплоприемника T2 = 280 К.
268. Идеальная тепловая машина работает по циклу Карно. Температура теплоотдатчика Т1 = 500 К, температура теплоприемника T2 = 250К. Определить термически КПД h цикла, а также работу А1рабочего вещества при изотермическом расширении, если при изотермическом сжатии совершена работа A2=70Дж.
269. Газ, совершающий цикл Карно, получает теплоту Q1=84кДж. Определить работу Агаза, если температура Т1теплоотдатчика в три раза выше температуры T2 теплоприемника.
270.В цикле Карно газ получил от теплоотдатчика теплоту Q1=500Дж и совершил работу A=100Дж. Температура теплоотдатчика Т1=400К. Определить температуру Т2теплоприемника.
271.Найти массу m воды, вошедшей в стеклянную трубку с диаметром канала
– 57 –
d=0,8мм, опущенную в воду на малую глубину. Считать смачивание полным.
272.Какую работу Анадо совершить при выдувании мыльного пузыря, чтобы увеличить его объем от V1=8см3 до V2=16см3? Считать процесс изотермическим.
273.Какая энергия Евыделится при слиянии двух капель ртути диаметром d1=0,8мм и d2=1,2мм в одну каплю?
274.Определить давление р внутри воздушного пузырька диаметром d=4мм, находящегося в воде у самой ее поверхности. Считать атмосферное давление нормальным. Пространство между двумя стеклянными параллельными пластинками с площадью поверхности S=100см2 каждая, расположенными на расстоянии l = 20 мкм друг от друга, заполнено водой. Определить силу F, прижимающую пластинки друг к другу. Считать мениск вогнутым с диаметром d, равным расстоянию между пластинками.
275.Глицерин поднялся в капиллярной трубке диаметром канала d=1 мм на высоту h=20мм. Определить поверхностное натяжение aглицерина. Считать смачивание полным.
276.В воду опущена на очень малую глубину стеклянная трубка с диаметром канала d=1мм. Определить массу т воды, вошедшей в трубку.
277.На сколько давление рвоздуха внутри мыльного пузыря больше нормального атмосферного давления ро, если диаметр пузыря d=5мм?
278.Воздушный пузырек диаметром d=2,2 мкм находится в воде у самой ее поверхности. Определить плотность r воздуха в пузырьке, если воздух над поверхностью воды находится при нормальных условиях.
279.Две капли ртути радиусом r=1,2мм каждая слились в одну большую каплю. Определить энергию Е, которая выделится при этом слиянии. Считать процесс изотермическим.
– 58 –
ПРИЛОЖЕНИЯ
- Основные физические постоянные (округленные значения).
| Физическая постоянная | Обозначение | Значение |
| Нормальное ускорение свободного падения | G | 9,81м/c2 |
| Гравитационная постоянная | Γ | 6,67×10-11м3/(кг×с2) |
| Постоянная Авогадро | NA | 6,02×1023 моль-1 |
| Универсальная газовая постоянная | R | 8,31 Дж/(моль×К) |
| Молярный объем идеального газа при нормальных условиях (стандартный объем) | Vm | 22,4×10-3 м3/моль |
| Постоянная Больцмана | K | 1,38×10-23Дж/K |
- Некоторые астрономические величины
| Наименование | Значения |
| Радиус Земли | 6,37×106 м |
| Масса Земли | 5,98×1024 кг |
| Радиус Солнца | 6,95×108 м |
| Масса Солнца | 1,98×1030 кг |
| Радиус Луны | 1,74×106 м |
| Масса Луны | 7,33×1022 кг |
| Расстояние от центра Земли до Центра Солнца | 1,49×1011 м |
| Расстояние от центра Земли до центра Луны | 3,84×108 м |
