Биотрансформация и биодеградация органических соединений
Лекция №5
БИОТРАНСФОРМАЦИЯ И БИОДЕГРАДАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Все органические соединения, взаимодействующие с живыми организмами, могут подвергаться процессам биотрансформации (изменение отдельных фрагментов молекулы) и биодеградации (разрушению до простых молекул типа CO2, H2O, NH4, CH4 и т.д.). Предметом данной лекции являются процессы биотрансформации приводящие к образованию полезных для человека продуктов (лекарств, химических веществ или полупродуктов), и процессы биодеградации токсичных отходов в живой природе.
Содержание
1.Биотрансформация органических соединений. 2
1.1.Процессы микробной химии. 4
1.2.Методы микробной трансформации органических соединений. 8
1.2.2.Трансформация суспензиями неразмножающихся клеток. 10
1.2.3.Трансформация осуществляемая спорами грибов и актиномицетов. 11
1.2.4.Непрерывные методы культивирования. 11
1.2.5.Кометаболизм.. 12
1.2.6.Применение поврежденных и дезинтегрированных клеток. 13
1.2.7.Ингибирование определенных участков метаболитических путей. 14
1.2.8.Применение мутантов с блокированным синтезом определенных ферментов. 14
1.2.9. Конструирование штаммов с повышенной способностью к трансформации. 15
1.2.10.Ферментные препараты и иммобилизованные ферменты.. 15
1.2.11.Иммобилизация клеток. 16
1.2.12.Политрансформации. 17
1.3.Микроорганизмы трансформирующие органические соединения. 18
1.4.Примеры трансформации органических соединений. 19
2.Биодеградация токсичных соединений. 25
2.1.Деградация ксенобиотиков с помощью микроорганизмов. 27
2.2. Использование методов генной инженерии для биодеградации ксенобиотиков. 32
Процессы микробной химии
Хотя любое превращение, осуществляемое ферментами микроорганизмов в процессах метаболизма, в принципе может быть использовано как трансформация, т. е. для препаративного получения его продуктов, в настоящее время реализована и практически используется лишь незначительная их часть. Но число процессов, позволяющих препаративно получить продукты ферментативных реакций и описанных в настоящее время, составляет несколько тысяч. Эти процессы очень разнообразны по природе исходных субстратов, использованным микроорганизмам, типу и количеству участвующих ферментов, характеру превращения органических соединений. Только часть из них осуществляется отдельными ферментами и может рассматриваться как ферментативные реакции. Значительная часть процессов микробной химии состоит из нескольких таких реакций, например приведенное выше окисление п-ксилола в п-толуиловую кислоту. Поэтому чаще говорят не о реакциях, а о процессах микробиологической трансформации. Классификации моноферментных процессов микробной трансформации, построенные на основе химических механизмов реакций или номенклатуры участвующих ферментов, сложны и насчитывают десятки различных типов. Более широко распространена классификация микробных трансформаций по типу химического превращения субстрат- продукт. Она отражает суммарное превращение исходного соединения, но не механизм процесса. Поэтому, например, все превращения альдоз в кетозы относят к типу «изомеризация», хотя у разных микроорганизмов в этом случае могут быть ответственны ферменты различных классов — соответствующая изомераза или две последовательно действующие оксидоредуктазы. Обычно выделяют класс процессов «дезаминирование», несмотря на то, что за них могут быть ответственны как окислительные, так и гидролитические ферменты. К типу «окисления» относят как моноферментные реакции, так и процессы, осуществляемые несколькими ферментами и т. д. В связи с этим классификация микробных трансформаций по типу превращения субстрат — продукт является искусственной и чисто прагматической, хотя и широко распространена. В настоящее время выделяют следующие типы процессов микробной трансформации: 1) окисление, 2) восстановление, 3) декарбоксилирование, 4) дезаминирование, 5)образование гликозидов, 6) гидролиз, 7) метилирование, 8) этерификация, 9) дегидратация, 10) диспропорцирование, 11) конденсация, 12) аминирование, 13) ацети-лирование, 14) амидирование, 15) нуклеотизация, 16) галогенирование, 17) деметилирование, 18)асимметризация, 19) рацемизация, 20) изомери-зация.
Наиболее изученный и широко используемый в промышленности процесс-реакции окисления. Они объединяют гидроксилирование неакти-вированного углерода в sp3-гибридном состоянии (введение спиртовой группы ОН), окисление непредельных С=С связей, гидроксилирование ароматического кольца, дегидрирование, β-окисление жирных кислот, окисление спиртовой или альдегидной групп и т.д. Характерным примером таких реакций является дегидрирование стероидов с целью получения антивоспалительных стероидных препаратов преднизона, преднизолона и их производных:
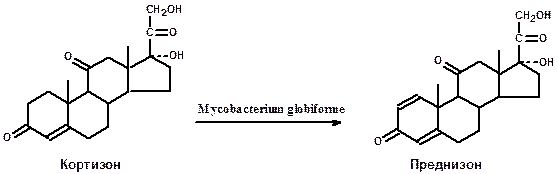
Микробное восстановлениеимеет преимущества перед многими химическими реакциями такого типа. Например, селективность действия микробных ферментов позволяет восстановить определенную кето-группу стероидов (химическим путем это невозможно). В синтезе стероидов эта особенность микроорганизмов используется очень широко, например, для восстановления 14а- или 17(3-кетогрупп) секостероидов ряда эстрана:
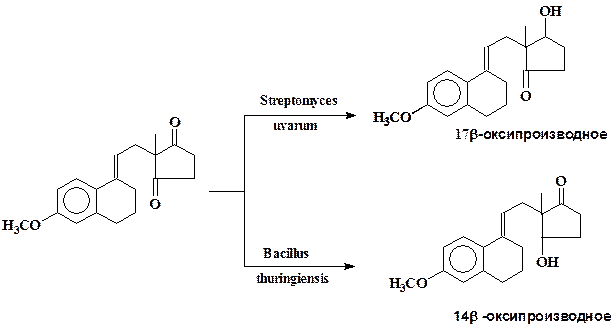
Известные примеры ферментативного декарбоксилированияв основном относятся к декарбоксилированию а-кетокислот и аминокислот (кетоглутаровая кислота до янтарной, аспарагиновая кислота до аланина).
Микробное дезаминированиеимеет большое значение для превращений аминокислот, пуриновых и пиримидиновых оснований и нуклеотидов.
Аминированиеописано для многих соединений, имеющих олефиновую двойную связь или кетогруппу (фумаровая кислота – аспарагиновая кислота, кетоглутаровая кислота - глутаминовая кислота). Аминирование может также происходить путем замещения атома водорода или оксигруппы, например, у гетероциклических оснований.
Все эти реакции играют ключевую роль в клеточном синтезе различных аминокислот. Особенно большое значение имеет процесс аминирования фумаровой и а-кетоглутаровой кислот. Микробный процесс по сравнению с химическим протекает в «мягких» условиях с хорошим выходом продукта и для аспарагиновой кислоты реализован в промышленном масштабе (Япония, США).
Реакции амидированияредко встречаются в микробной химии. Один из таких примеров — образование биотинамида из биотина.
Реакции гидролизачрезвычайно широко распространены в микробной химии. Они включают гидролиз эфиров, амидов и других соединений. Наиболее часто эти реакции используют в антибиотической промышленности и при производстве стероидов. Современное производство пенициллинов основано на синтезе различных производных 6-аминопенициллановой кислоты (6-АПК). Кислоту получают из бензилпенициллина ферментативным гидролизом:
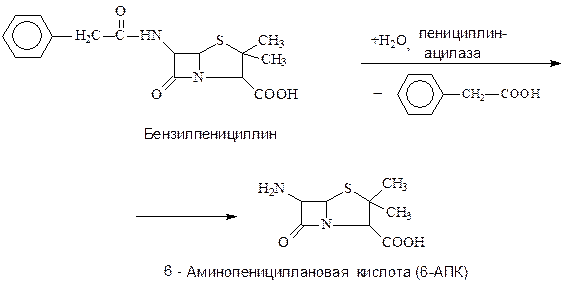
Реакции конденсации— синтез молекул органических веществ из двух или более фрагментов с помощью различных микробных ферментов. Реакции широко применяются при получении новых антибиотиков — производных пенициллина и цефалоспорина, которые синтезируют на базе 6-аминопенициллановой и 7-аминоцефалоспорановой кислот ферментативным и химическим способами.
Большое значение имеет синтез аминокислот из предшественников. Конденсацией пирокатехина и его функциональных производных с аланином и серином удалось получить L-диоксифенилаланин— (ДОФА) — ценный лекарственный препарат, применяемый при болезни Паркинсона:
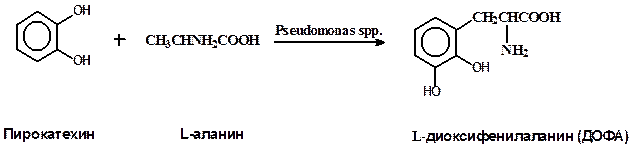
Реакции нуклеотидации – синтез различных нуклеотидов микроорганизмами из гетероциклических оснований или нуклеозидов. Они включают образование рибозидов и их фосфорилирование. В зависимости от условий различные микроорганизмы могут синтезировать нуклеозиды, их моно-, ди- и трифосфаты (АМФ, АДФ,АТФ и др.).
Реакция галогенированияредко встречается в микробном мире, но имеет особое значение, так как селективное галогенирование химическим путем – одна из самых сложных проблем химии. Она дает возможность получать галогенированные производные стероидов и других лекарственных препаратов. Наиболее изучен процесс галогенирования ферментом мицелия гриба Caldariomyces fumago, получившим название хлорпероксидазы. Фермент катализирует хлорирование кетокислот, циклических дикетонов, бромирование тиазолов, анизола, стероидов и т. д.
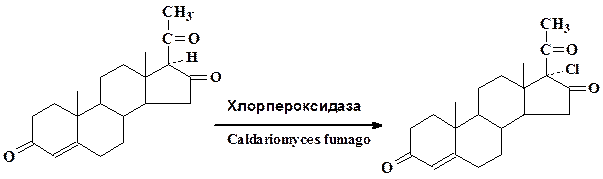
Расщепление рацемических соединений на оптические антиподышироко используется в промышленности для получения стереоизомеров. Эти процессы основаны на стереоспецифичности ферментов, например ацилаз. Ацилазы используют для разделения смесей DL-аминокислот, которые вначале ацилируют, а ацильные производные подвергают гидролизу с помощью этих ферментов, получая L-аминокислоты. Аналогичным путем происходит разделение некоторых терпенов, например dl-изопулегола:
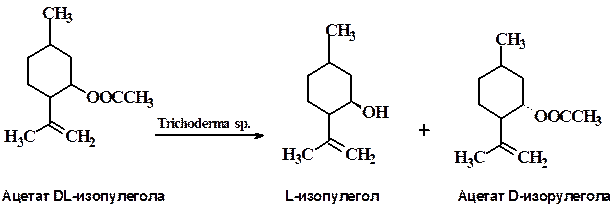
Реакции изомеризацииимеют большое практическое значение. На их использовании основан, например, такой важный промышленный процесс, как получение фруктозы из глюкозы:
Кометаболизм
Кометаболизм— процессы трансформации или полного разложения органических соединений, осуществляемые микроорганизмами сопряженно с метаболизмом других субстратов – косубстратов,которые не являютсяростовыми. Так, упомянутое выше окисление нокардиями п-ксилола или 3-метилпиридина в соответствующие кислоты без косубстратов на питательной среде, содержащей такие соединения, как глюкоза и ацетат, происходит медленно. В присутствии же ксилозы или глицерина активность трансформации резко возрастает. Важно отметить, что глюкоза и ацетат являются оптимальными ростовыми субстратами для культур, осуществляющих описываемые процессы, в то время как ксилоза лишь частично окисляется, но не используется ими в качестве источника углерода, а глицерин поддерживает лишь медленный рост. Таким образом,оптимальные ростовые субстраты - глюкоза и ацетат- не стимулируют трансформацию и, следовательно, не являются косубстратами.
При использовании метода растущих культур накопление продуктов трансформации на средах с глюкозой и ацетатом, но без косубстратов, происходит лишь в связи со значительным увеличением массы клеток в культуре, которые имеют низкую удельную активность. В вариантах же с глицерином или ксилозой даже при медленном росте или в его отсутствие удельная активность трансформации значительно выше, что и стимулирует значительное накопление продуктов даже при низкой плотности клеточной культуры. Такие процессы и называют кометаболизмом; он обнаруживается при сравнении удельных скоростей процессов трансформации на различных средах.
Механизм сопряжения между трансформацией и метаболизмом косубстрата, приводящего к интенсификации первого процесса, изучены слабо. По всей вероятности такое сопряжение заключается в использовании в первом процессе каких-то метаболитов, образующихся во втором процессе и обеспечивающих первый энергией и (или) кофакторами. Поэтому кометаболизм играет важную роль в тех случаях, когда в метаболической системе микроорганизма отсутствует или недостаточно совершенна координация метаболических путей. Именно поэтому условия кометаболизма бывают, необходимы микроорганизму для превращения необычных для него субстратов (например, упомянутых выше п-ксилола и 3-метилпиридина).
Поскольку косубстрат играет в процессе кометаболизма специфическую и вполне определенную роль, правильный его выбор имеет важнейшее значение. В некоторых случаях, когда ферментативный механизм трансформации известен, выбор косубстрата не составляет труда. Так, для интенсификации процесса восстановления карвона в дигидрокарвон культурой Pseudomonas ovalisв качестве косубстрата был выбран этанол потому, что данный микроорганизм имеет активную НАД-зависимую алкогольдегидрогеназу, окисляющую этанол в ацетальдегид; последняя обеспечивает трансформацию карвона восстановительными эквивалентами (НАД*H):
C2H5OH + HAD ----- CH3COH + НАД*H
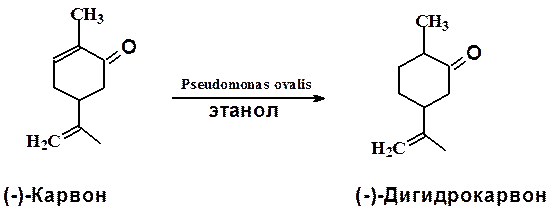
В случаях, когда механизм процесса неясен, косубстраты приходится подбирать путем проверки разных соединений. Окислительные процессы кометаболизма иногда называют соокислением (под таким названием они были описаны впервые американским микробиологом Фостером), восстановительные — совосстановлением.
Иммобилизация клеток
Наряду с успешной иммобилизацией многих ферментов и применением этого метода в промышленности исследователи столкнулись с рядом трудностей, характерных для работы с ферментами, зависимыми от кофакторов, а также в тех случаях, когда трансформации осуществляются несколькими ферментами. Были предприняты попытки использовать активность «сложных» ферментов и ферментных комплексов путем иммобилизации клеток. Иммобилизация клеток позволяет эксплуатировать отдельные ферменты, а также их системы, что затруднительно при работе с иммобилизованными ферментами. Обмен иммобилизованных клеток отличается от метаболизма интактных микроорганизмов, что может быть использовано в целях регуляции трансформации. Эффективность процессов, осуществляемых иммобилизованными клетками, в ряде случаев выше их эффективности, как у свободных микроорганизмов, так и у иммобилизованных ферментов. Для иммобилизации клеток используются почти все методы, применяемые для иммобилизации ферментов, но наиболее распространенным в настоящее время является включение в полиакриламидный (ПААГ) и каррагенановый гели.
Получение аминокислот и органических кислот с использованием клеток, иммобилизованных в полиакриламидный и каррагенановый гели — один из примеров, демонстрирующих возможности и перспективы метода. Клетки Е. coli, иммобилизованные в ПААГ, осуществляли превращение фумаровой кислоты в аспарагиновую. При этом активность иммо-билизованных клеток сохранялась при 37°С в присутствии ионов Mg++ в течение 40 сут. при скорости протока 0,5 мл/ч через колонку размером 10х100 см, причем выход аспартата достигал 95 %. Процесс был успешно применен в промышленном масштабе. Ежесуточный выход кислоты при использовании промышленной колонки 1900 кг или 57,6 т/мес, время полужизни и активность клеток свыше 120 сут. Позже был разработан более экономичный способ иммобилизации клеток в каррагенан. Продуктивность иммобилизованных в каррагенан клеток в 15 раз превышала таковую для иммобилизованных в ПААГ, время полужизни их также увеличилось до 2 лет. Преимущества метода были так велики перед существовавшим ранее, что фирма “Танабе” в 1979 г. заменила им промышленное получение L-acnaрагиновой кислоты. Такой же процесс был осуществлен в Советском Союзе.
Получение L-яблочной кислоты из фумаровой с помощью иммобилизованных в каррагенан клеток Brevibacterium [iuvum— второй пример промышленного использования ферментативной активности микроорганизмов для биоконверсии органических соединений.
Пристального внимания заслуживает и метод иммобилизации смешанных культур. Так, осуществлена трансформация сорбозы в 2-кето-L-гулоновую кислоту смесью иммобилизованных в ПААГ клеток Gluconobacter melanogenusIFO 3293 и Pseudomonas syringaeNRRL B-865. Первая бактерия окисляла сорбозу в сорбозон, а вторая, обладая активной сорбозоноксидазой, образовывала 2-кето-L-гулоновую кислоту.
Политрансформации
Трансформация сложных органических молекул часто предполагает более чем одну ферментативную реакцию. В ряде случаев для получения практически ценных продуктов требуются весьма существенные перестройки молекулы субстрата, которые могут включать различные процессы, например окисление и гидролиз или окисление, восстановление и гидролиз и т. д. Эти задачи могут быть решены разными путями.
Примеры трансформации органических соединений
Способность клеток микроорганизмов к сложнейшим процессам биотрансформации наиболее полно реализовалась при получении промышленно важных стероидов. Использование абсолютной субстратной специфичности и стереоспецифичности биологических катализаторов, присущих целым клеткам микроорганизмов, позволило разработать условия осуществления множества химических реакций для структурных перестроек стероидов. В результате были получены новые соединения с лучшими фармакологическими свойствами.
Биотрансформация стероидов обычно заключается в селективном воздействии на одно из положений стероидного скелета. Первый промышленный процесс микробной биотрансформации стероидов основывался на технологии направленного гидроксилирования (11-α-гидроксилирование) прогестерона:
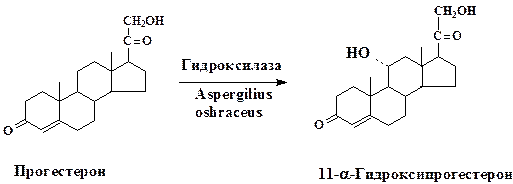
Значимость разработанной микробной трансформации определяется тем, что процессы гидроксилирования кортикостерона и его производных лежат в основе промышленного получения многих ценных продуктов: противовоспалительных и противоопухолевых препаратов, трансквилизато-ров, анестезирующих средств, половых гормонов и пр.
В качестве типичного примера микробиологической трансформации рассмотрим подробнее превращение гидрокортизона в преднизолон культурой Mycobacterium globiforme для которой характерны окислительно-восстановительные превращения стероидной молекулы(микроорганизм применяется в промышленности для получения стероидных гормонов):
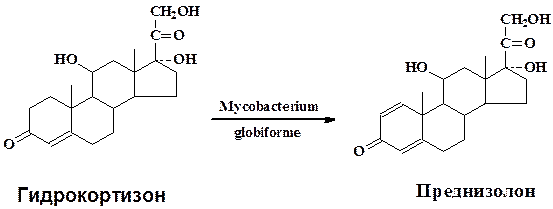
Культуру Mycobacterium globiforme предварительно выращивают на питательной среде содержащей кукурузный экстракт 1,0 г, глюкозу 1 г, агар-агар 3,0 г, на 1 л водопроводной воды при рН среды 6,8-7,2 в течени 4-5 сут. Затем водной суспензией клеток засевают колбы с жидкой средой того же состава, разлитой по 50 мл в медицинские качалочные колбы. Одновременно с бактериальной суспензией вносят в качестве индуктора ацетат кортизона (10 мг в 1 мл метанола на 50 мл среды). Через 24 ч (при сухой биомассе 1,6—2,5 мг/мл) в культуральную жидкость вносят водную суспензию тонкоизмельченного гидрокортизона до величины частиц менее 5мкм. Трансформацию проводят при 28-30 °С на качалке с 200—220 об/мин в течение 18—24 ч. Культуральную жидкость (300 мл) экстрагируют три раза этилацетатом (по 1л), объединенный экстракт упаривают до 300 мл, добавляют 0,3 г активированного угля, кипятят 5-10 мин, уголь отфильтровывают, промывают горячим этилацетатом и растворитель отгоняют до 45 мл. Раствор охлаждают 16 ч при 0 °С для полного выделения преднизолона. Осадок отфильтровывают, промывают охлажденным этилацетатом, высушивают при 60-70 °С. Выход преднизолона 85 % от теоретического, в качестве примесей образуется 20β-оксипроизводное преднизолона (0,5 %) и исходный гидрокортизон – 6-8 %.
При использовании иммобилизованных в полиакриламидный гель клеток Mycobacterium globiforme реакционную смесь, содержащую 0,1 г/л гидрокортизона в фосфатном буфере (рН 7,0), пропускали через колонку, содержащую гранулы геля. Скорость потока через колонку 1,3 мл/ч на 1 мл геля (SV), температура 20-22 °С. Выделение стероидов проводили по методике, описанной выше. При таких условиях наблюдалось количественное превращение субстрата в течение 9-10 сут, через 15 сут активность снижалась на 50%, через 20 сут обнаруживалось лишь 5-7 % превращенного субстрата.
Разработка крупномасштабного производства преднизолона путем биотрансформации стероидов позволила снизить стоимость этого препарата в 200 раз.
Важнейший источник стероидных гормонов - культуры клеток растений. Так, культура клеток диоскореи дельтовидной (Dioscorea deltoided)корневого происхождения продуцирует фитостерин диосгенин и его гликозидные производные (сапонины). Существенно, что способность к сверхсинтезу фуростаноловых гликозидов ряда штаммов диоскореи, например штамма ДМ-ОГ, стабильно поддерживалась в течение 27 лет. Таким образом, культивирование клеток растений in vitro представляет собой новое решение проблемы промышленного получения вторичных метаболитов.
Биотрансформация стероидов с использованием культур растительных клеток имеет целый ряд преимуществ перед микробиологической трансформацией. Так, если трансформация в положения 3 и 5 характерна практически для всех используемых культур (микроорганизмы, растительные клетки), то реакции Iβ-, 4β-, I2β- (дигитоксин в дигоксин), 16β-гидроксилирования и изомеризации 17β-лактонного кольца, осуществляются только некоторыми культурами растительных клеток, и сильно, зависят от происхождения ткани и условий трансформации.
Изучение биотрансформации малоиспользуемого в терапии сердечного гликозида дигитоксина в ценные гликозиды (дигоксин, пурпурео-гликозид А и др.) проводилось на клеточных линиях Digitalis. Высокий выход конечных продуктов был достигнут при селекции специализированных линий и оптимизации условий роста в специальных аппаратах.
Процесс биотрансформации дигитоксина протекал в две стадии. После 10-дневной инкубации клеток Digitalis lanata в “ростовой” питательной среде (Мурасиге - Скуга) культуру переносили в "продукционную” среду (8% раствор глюкозы) с субстратом для биотрансформации- дигитоксином. В этих условиях весь дигитоксин в течение 2 дней трансформировался в дигоксин.
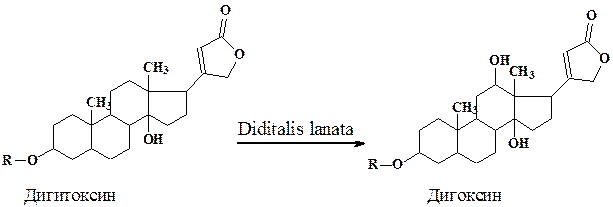
Дальнейшие успехи в производстве стероидных препаратов связывают с применением иммобилизованных клеток, использованием оптимального сочетания биологических и химических превращений, а также с совершенствованием технологии очистки получаемых соединений.
Так, в настоящее время разработаны промышленные способы получения ценных карденолидов, основанные на иммобилизации растительных клеток Digitalis в специальных биокатализаторах.
В последнее время сильно возрос интерес к использованию микроорганизмов для избирательной биотрансформации гетероциклических соединений.
Среди гетероциклических соединений наиболее широко изучены процессы окисления пиридинов в пиридоны, селективное окисление боковых алкильных групп в различных гетероциклах, энантиоселективное цис-дигидроксилирование бензотиофенов и бензофуранов.
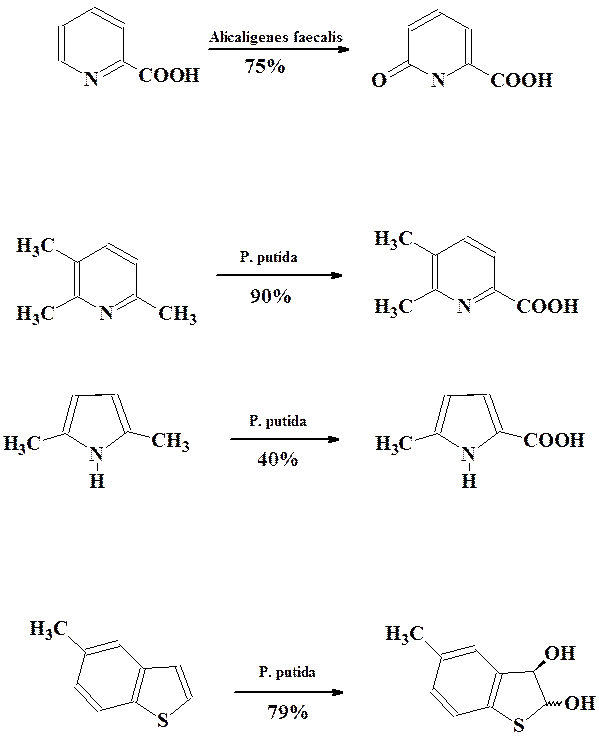
Поразительным примером возможностей микробной биотрансформа-ции является катализируемое ферментами введение аминокислотных фрагментов в 4-, 5-, 6-, 7-азаиндолы при алкилировании их серином.
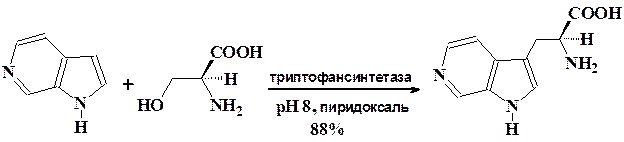
Учеными фирмы “Сетус корпорепйшин” предложен оригинальный ферментативный способ синтеза различных окисей алкенов (эпоксидов), являющихся исходным соединением для синтеза различных пластмасс и производных диолов (антифриз, тормозная жидкость и т.д). В настоящий момент окиси алкенов получают химическим путем. Процесс протекает под высоким давлением, является взрывоопасным и требует большого количества дорогостоящего серебряного катализатора.
Ферментативный синтез окисей алкенов из алкенов, протекающей в водной среде, основан на 3 ферментах: глюкозозо-2-оксидазе из базидомицета Oudemansiella mucida, галопероксидазе из гриба Caldariomyces или других источников и эпоксидазе из Flavobacterium. На первом этапе синтеза глюкозозо-2-оксидаза вызывает образование перекиси водорода (Н2О2) из глюкозы, которая служит и субстратом, и источником энергии. На втором этапе, катализируемом галопероксидазой, перекись водорода взаимодействует с вводимыми в реакционную среду алкеном и галогенид-ионом (ионом фтора, хлора или брома) с образованием соответствующего β-алкангалогенгидрина. На последнем этапе водород гидроксильной (Н+) группы и галогенид-анион отщепляются под действием эпоксидазы, в результате чего получается окись соответствующего алкена.
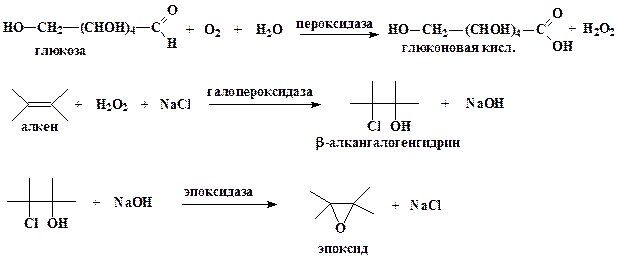
Ферментативный путь синтеза окисей алкенов весьма выгоден с экономической и экологической точек зрения по сравнению с химическим, поскольку источником галогенид-иона может служить обычная соль, такая как хлорид натрия, а в химическом синтезе используют элементарный хлор. Не нужен и серебряный катализатор. При использовании ферментативного метода в качестве побочного продукта с высоким выходом из глюкозы образуется глюконовая кислота, которая в свою очередь является очень ценным продуктам.
Другое преимущество ферментативного способа синтеза окисей алкенов – его гибкость: изменяя субстрат на который действует галопероксидаза, можно синтезировать различные окиси алкенов. Еще одно достоинство этого метода состоит в том, что он не дает отходов: галоген можно опять использовать в новом цикле синтеза. Перспективным является увеличение активности ферментов за счет их иммобилизации или модификации активных центров с использованием методов генной инженерии.
Лекция №5
БИОТРАНСФОРМАЦИЯ И БИОДЕГРАДАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Все органические соединения, взаимодействующие с живыми организмами, могут подвергаться процессам биотрансформации (изменение отдельных фрагментов молекулы) и биодеградации (разрушению до простых молекул типа CO2, H2O, NH4, CH4 и т.д.). Предметом данной лекции являются процессы биотрансформации приводящие к образованию полезных для человека продуктов (лекарств, химических веществ или полупродуктов), и процессы биодеградации токсичных отходов в живой природе.
Содержание
1.Биотрансформация органических соединений. 2
1.1.Процессы микробной химии. 4
1.2.Методы микробной трансформации органических соединений. 8
1.2.2.Трансформация суспензиями неразмножающихся клеток. 10
1.2.3.Трансформация осуществляемая спорами грибов и актиномицетов. 11
1.2.4.Непрерывные методы культивирования. 11
1.2.5.Кометаболизм.. 12
1.2.6.Применение поврежденных и дезинтегрированных клеток. 13
1.2.7.Ингибирование определенных участков метаболитических путей. 14
1.2.8.Применение мутантов с блокированным синтезом определенных ферментов. 14
1.2.9. Конструирование штаммов с повышенной способностью к трансформации. 15
1.2.10.Ферментные препараты и иммобилизованные ферменты.. 15
1.2.11.Иммобилизация клеток. 16
1.2.12.Политрансформации. 17
1.3.Микроорганизмы трансформирующие органические соединения. 18
1.4.Примеры трансформации органических соединений. 19
2.Биодеградация токсичных соединений. 25
2.1.Деградация ксенобиотиков с помощью микроорганизмов. 27
2.2. Использование методов генной инженерии для биодеградации ксенобиотиков. 32
