Біохімічні форми глікогенозів.
Біосинтез глікогену
У незначній мірі біосинтез глікогену (глікогенез) відбувається майже у всіх тканинах організму, проте найбільше він виражений у печінці та м'язах. Цей процес розпочинається із глюкозо-6-фосфату, що утворюється із глюкози вгексокіназній або глюкокіназній реакції. Частина глюкози, що поступає в організм із їжею, спочатку поглинаєтьсяеритроцитами, які використовують її для отримання енергії у процесі молочнокислого бродіння. Утворений лактат у гепатоцитах перетворюється до глюкозо-6-фосфату в процесі глюконеогенезу.
Метаболічні шляхи біосинтезу та розпаду певних сполук зазвичай відрізняються принаймні деякими із реакцій. Метаболізм глікогену був першим відкритим прикладом цього важливого принципу. 1957 року Луїс Лелуар встановив, що в процесі глікогенезу використовується не глюкозо-1-фосфат, а уридиндифосфатглюкоза.
Глюкозо-6-фосфат спершу перетворюється до глюкозо-1-фосфат під впливом фосфоглюкомутази. Продукт цієї реакції стає субстратом для ферменту УДФ-глюкозофосфорилази, яка каталізує реакцію:
Глюкозо-1-фосфат + УТФ → УДФ-глюкоза + ФФн.
Оскільки пірофосфат відразу розщеплюється неорганічною пірофосфатазою, то рівновага реакції сильно зміщена в сторону утворення УДФ-глюкози. Остання є субстратом для глікогенсинтази, що переносить залишок глюкози на нередукуючий кінець молекули глікогену.
Утворення бічних гілок забезпечує гілкозил-(4→6)-трансглікозилаза (розгалужуючий фермент). Вона відщеплює від гілки, що містить більше 11 мономерних одиниць 6—7 останніх і переносить їх на C6 гідроксильну групу залишку глюкози у більш внутрішньому положенні на тій самій або іншій гілці. Таким чином відбувається галуження, необхідне для кращої розчинності глікогену, та доступу більшої кількості ферментів синтезу та розщеплення до нередукуючих кінців.
Глікогенсинтаза може синтезувати глікоген тільки за умови наявності праймера — готового полімеру глюкози із принаймні шістьма мономерними одиницями. Утворення молекул глікогену de novo можливе тільки завдяки білкуглікогеніну, що виступає одночасно і «затравкою», на якій збираються нові гілки глікогену і ферментом, що каталізує початок утворення перших із них.
Глікогенез та глікогеноліз мають складну систему регулювання на кількох рівнях. Багато із ферментів, що беруть участь у цих процесах є алостеричними і можуть змінювати свою активність пристосовуючись до потреб клітини. Кількість запасів глікогену також регулюється на гормональному рівні для підтримання гомеостазу цілого організму.
3.Регуляція глюконеогенезу
У клітинах печінки здійснюється координована регуляція гліколізу і глюконеогенезу відповідно до фізіологічних потреб усього організму. Система контролю включає субстрати і проміжні продукти процесів, регуляторні ферменти та їх ефектори, гормони. Підкреслимо, що регуляторними ферментами глюконеогенезу і гліколізу є ті, що каталізують незворотні реакції і не беруть участі у протилежному процесі. Наприклад, піруваткарбоксилаза (активатор – ацетил-КоА) і фруктозодифосфатаза – (активатор – цитрат, інгібітори – АМФ і фруктозо-2,6-дифосфат). На рис. 12 показані регуляторні пункти гліколізу і глюконеогенезу та контрольні чинники.
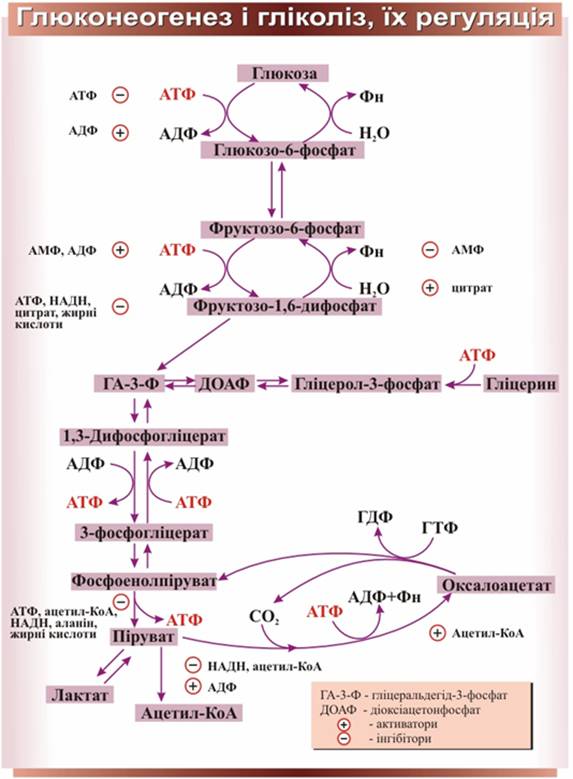
Рис. 12. Регуляція гліколізу і глюконеогенезу в печінці
Деякі ефектори одночасно впливають на активність регуляторних ферментів в обох процесах. Так, ацетил-КоА служить активатором піруваткарбоксилази і інгібітором піруваткінази. Крім того, ацетил-КоА є інгібітором піруватдегідрогеназного комплексу і, сповільнюючи розпад пірувату до ацетил-КоА, сприяє переходу пірувату в глюкозу. АМФ інгібує фруктозо-дифосфатазу і разом з тим активує відповідний фермент гліколізу – фосфофруктокіназу. Навпаки, цитрат – активатор фосфатази й інгібітор кінази.
Глюконеогенез стимулюється не тільки активаторами піруваткарбоксилази і фруктозодифосфатази, а й інгібіторами регуляторних ферментів гліколізу (АТФ, аланін, жирні кислоти). Таким чином, коли в клітині є достатня концентрація палива для циклу лимонної кислоти (ацетил-КоА, оксалоацетату, цитрату, жирних кислот, аланіну) чи висока концентрація АТФ і низькі –АДФ та АМФ, посилюється біосинтез глюкози і гальмується гліколіз. У протилежній ситуації стимулюється гліколіз і гальмується глюконеогенез.
На глюконеогенез впливають такі гормони, як глюкагон й інсулін підшлункової залози та глюкокортикоїди кори надниркових залоз. При голодуванні глюкагон посилює розпад жирів у жировій тканині. Жирні кислоти надходять у печінку, де розпадаються до ацетил-КоА. Швидкість окиснення ацетил-КоА в циклі лимонної кислоти відстає від швидкості його утворення, і підвищений рівень ацетил-КоА в клітині активує піруваткарбоксилазу. В результаті посилюється глюконеогенез.
Глюкагон започатковує глюконеогенез ще одним способом – через фруктозо-2,6-дифосфат. Цей регуляторний компонент відкритий у 1980 р. Утворюється фруктозо-2,6-дифосфат із фруктозо-6-фосфату при дії фосфофруктокінази ІІ, а розщеплюється фруктозо-2,6-дифосфатазою:
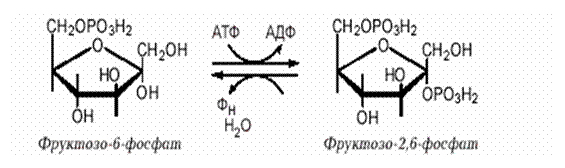
Фруктозо-2,6-дифосфат активує фермент гліколізу фосфофруктокіназу і гальмує активність ферменту глюконеогенезу фруктозо-1,6-дифосфатази. Утворення фруктозо-2,6-дифосфату пригнічується глюкагоном, який шляхом цАМФ-залежного фосфорилювання інактивує фосфофруктокіназу ІІ й активує фруктозо-2,6-дифосфатазу. Таким чином, при голодуванні глюкагон знижує внутрішньоклітинну концентрацію фруктозо-2,6-дифосфату, що викликає стимуляцію глюконеогенезу і гальмування гліколізу. Підвищення швидкості глюконеогенезу в печінці призводить до того, що глюкоза надходить у кров і потрапляє в інші органи, насамперед у мозок.
Субстратами глюконеогенезу служать амінокислоти, оскільки під час голодування в крові низьке співвідношення інсулін/глюкагон гальмує синтез білків і стимулює їх катаболізм, зокрема в м’язах, що забезпечує постачання амінокислот у печінку. При тривалому голодуванні зростає секреція корою надниркових залоз глюкокортикоїдів, які посилюють у печінці синтез ферментів глюконеогенезу (фосфоенолпіруват-карбоксикінази, глюкозо-6-фосфатази) й амінотрансфераз – ферментів, які каталізують перетворення глюкогенних амінокислот у піруват і оксалоацетат. У м’язах та інших тканинах глюкокортикоїди гальмують синтез білків. У результаті стимуляції глюконеогенезу глюкокортикоїди збільшують концентрацію глюкози в крові й синтез глікогену в печінці. Інсулін протидіє стимулюючій дії глюкагону і глюкокортикоїдів на глюконеогенез.
5. Аглікогенози – спадкові хвороби накопичення глікогену, молекулярною основою яких є генетичні дефекти, що призводять до порушення утворення ферменту глікогенсинтази.
Внаслідок недостатності глікогенсинтази гепатоцити не здатні утворювати резерви глікогену, концентрація якого всередині клітин значно зменшена. Внаслідок відсутності глікогенових резервів хворі при аглікогенозах, як і при глікогенозах, страждають від глибокої гіпоглюкоземії, особливо натщесерце, після значної перерви з часу надходження харчової глюкози. Гіпоглюкоземія при аглікогенозах може супроводжуватися важкою комою внаслідок енергетичного голодування головного мозку. Такі хворі звичайно вмирають у ранньому дитячому віці.
При нестачі глікогенсинтази в печінці значно знижується вміст глікогену, в проміжках між споживанням їжі швидко настає зменшення концентрації глюкози в крові, а після надходження значної кількості вуглеводів спостерігається тривала гіперглікемія. Нестача ферментів розпаду глікогену зумовлює його накопичення в тканинах. При цьому структура глікогену може бути нормальною або, при відсутності альфа‑(1®6)-глюкозидази, аномальною, з дуже короткими боковими гілками. У хворих спостерігаються характерні для кожного типу клінічні симптоми: збільшення печінки (тип І, ІІІ, VI), м’язова слабість (тип V), затримка розумового розвитку і корчі внаслідок виражених гіпоглікемій (тип І). Нестача глікозил-(4®6)-трансферази також призводить до аномальної структури глікогену – з довгими малорозгалуженими ланцюгами. І хоч при цьому типі глікогенозу (IV) кількість глікогену може бути зниженою чи нормальною, але внаслідок, вірогідно, реакції організму на саме таку структуру молекул глікогену настають печінкова недостатність і смерть у ранньому віці. Рання смерть спостерігається і при глікогенозі типу ІІ (хворобі Помпе), коли відсутній фермент лізосомальфа-глюкозидаза. В нормі під дією цього ферменту розпадається тільки 1-3 % глікогену клітин печінки, м’язів, серця. При відсутності альфа-глюкозидази глікоген накопичується у вакуолях цитоплазми клітин.
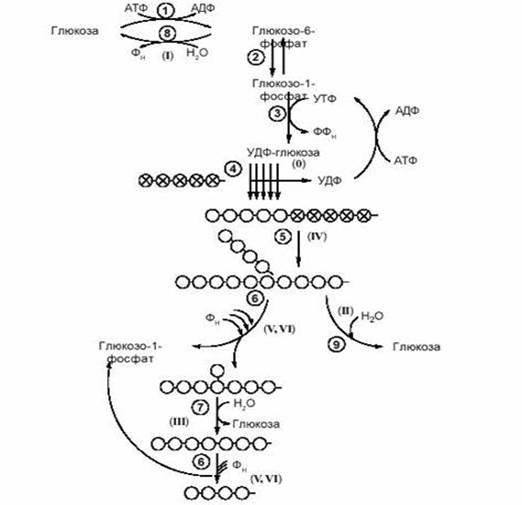
Рис. 6.Схема метаболізму глікогену.
Ферменти: 1 – гексокіназа (глюкокіназа);
2 – фосфоглюкомутаза;
3 – глюкозо-1-фосфатуридилтранфераза;
4 – глікогенсинтаза; 5 – глікозил-(4→6)-трансфераза;
6 – глікогенфосфорилаза; 7 – α-(1→6)-глюкозидаза;
8 – глюкозо-6-фосфатаза; 9 - α-1,4-глюкозидаза лізосом.
Римськими цифрами вказано типи глікогенозів.
За клінічними ознаками розрізняють три основні форми глікогенозів: 1) печінкову; 2) м’язову; 3) генералізовану.
Печінкова форма.
Ознаки з’являються на першому році життя, починаючи з 8-9 місяця, коли відзначаються рідкі напади гіпоглікемії. Вони характеризуються тимчасовою втратою свідомості, клонічними судомами кінцівок. Напади починаються до їжі або вранці, їх появі можна запобігти прийманням солодкої води. Характерний зовнішній вигляд дітей: маленький зріст, великий живіт, худі кінцівки, «лялькове обличчя». Відзначається збільшення печінки. Найбільш небезпечний вік – перші 4-5 років. Інфекційні захворювання ускладнюють перебіг патологічного процесу. З віком стан хворого поліпшується завдяки розвитку компенсаторних механізмів обміну. Інтелект, як правило, не порушений. При гістохімічному дослідженні печінки виявляють сильне розростання колагенової сполучної тканини, печінкові клітини багаті на глікоген, містять багато ліпідів.
М’язова форма.
Симптоми захворювання з’являються з 7-10 років. Хворі стають малорухливими, швидко втомлюються при фізичному навантаженні. М’язова слабкість прогресує, з’являються болі в працюючих м’язах, серцебиття, задуха. Усі ці симптоми розвиваються до 25-35 років. Зовнішній вигляд хворих не змінений. Симптомів зміни печінки і нирок немає. При огляді виражена атрофія м’язів та їх гіпотонія. При гістохімічному дослідженні видно м’язові волокна з дегенерацією, аж до некрозу. Вони містять вакуолі, наповнені глікогеном. Прогноз захворювання сприятливий, але відомі летальні наслідки в 20-30 років.
Генералізована форма.
При цій формі захворювання практично в усіх органах і тканинах накопичується велика кількість глікогену. Клініка її не схожа на клініку печінкової і м’язової форм, вона різноманітна, має прогресуючий перебіг.
Біохімічні форми глікогенозів.
1-й тип (хвороба Гірке) викликаний відсутністю активності специфічної глюкозо-6-фосфатази в печінці і слизовій кишківника. Успадковується за аутосомно-рецесивним типом. Порушується одна з головних функцій печінки – підтримання гомеостазу глюкози крові і порушений процес утворення глюкози з амінокислот. Водночас у гепатоцитах знаходять багато ліпідів. Клінічна картина дуже типова для печінкової форми глікогенової хвороби. Особливістю є те, що у дітей 5-7 років бувають геморагічні висипання і кровотечі, пов’язані з порушенням функції тромбоцитів. Іншою особливістю є підвищення у крові сечової кислоти, симптомокомплекс подагри розвивається у більш пізньому віці. Часто відзначається збільшення нирок.
Діагностувати захворювання можна за допомогою введення мічених атомів глюкози. Остаточний діагноз ставлять за результатами біопсії печінки: наявність у клітинах великої кількості нормального за структурою глікогену, що є специфічною ознакою цього захворювання. Хворим рекомендують уникати вживання продуктів, які містять сахарозу і лактозу.
2-й тип (хвороба Помпе) - хвороба має найбільш несприятливий перебіг, при цьому в усіх органах відсутні лізосомна альфа-глюкозидаза і гамма-амілаза, що призводить до накопичення глікогену в усіх тканинах і насамперед інтенсивно працюючих м’язах (серце). Хвороба з’являється на першому році життя у вигляді симптомокомплексу серцевої недостатності. Відзначається збільшення серця, печінки, гіпертрофія м’язів, збільшення язика. Дитина часто збуджена, але її спонтанні рухи поступово стають обмеженими, сухожилкові рефлекси до 4-5-місячного віку зникають.
Прогнознесприятливий – дитина гине до кінця 1-го року життя. При патологоанатомічному дослідженні зміни виявляють у всіх органах і тканинах. Генетично захворювання вважається аутосомно-рецесивним. Частіше хворіють хлопчики. Ефективного лікування не існує. Можлива пренатальна діагностика цього захворювання методом амніоцентезу (дослідження клітин шкіри плоду).
3-й тип (хвороба Корі) викликаний відсутністю або зниженням активності аміло-1,6-глюкозидази. При ньому страждають печінка, серце і кісткові м’язи.
Клінічна картина відноситься до печінкової форми захворювання і подібна до такої при І типі глікогенозу. Прогноз, як правило, сприятливий. Захворювання найбільш небезпечне в 4—5 років, коли часті напади гіпоглікемії. У більш зрілому віці симптоми захворювання згладжуються. Лікування дає хороші результати при застосуванні багатої на білки дієти з частими прийомами їжі, щоб утворення глюкози йшло обхідним шляхом за допомогою трансамінування амінокислот.
4-й тип (хвороба Андерсена) викликаний відсутністю ферменту амілотрансглюкозидази. Замість глікогену в уражених органах синтезується полісахарид, подібний до амілопектину. Хвороба з’являється з першого року життя і подібна за клінікою до цирозу печінки. Фермент відсутній у печінці, нирках, селезінці, серцевому і кістковому м’язах. Смерть настає на першому році життя.
5-й тип (хвороба Мак-Ардля) характеризується дефіцитом фосфорилази тільки в м’язах. Захворюванняуспадковується за аутосомно-рецесивним типом. Клініка типова для м’язової форми глікогенозу.
4. 
7. Мукополисахаридо́зы сокращённо МПС, или англ. MPS (отмукополисахариды + -ōsis) — группа метаболических заболеванийсоединительной ткани, связанных с нарушением обмена кислыхгликозаминогликанов (GAG, мукополисахаридов), связанных недостаточностью лизосомных ферментов обменагликозаминогликанов. Заболевания вызваны наследственными аномалиями обмена, проявляются в виде лизосомной болезни накопления: различных дефектов костной, хрящевой, соединительной тканей.
В зависимости от недостаточности одного из ферментов лизосом, накапливаются мукополисахариды одного из трёх классов: гепаран-, дерматан- или кератансульфаты[13].
Ревмати́зм (ще ломець; дав.-гр. ῥεῦμα - потік, течія, розтікання по тілу —захворювання імунно-запального характеру, пов'язане із стрептококовоюінфекцією. Проявляється перш за все ураженням серця (із виникненням вад), суглобів, рідше — нервової системи та інших внутрішніх органів. Хвороба перебігає із рецидивами та загостреннями, яким за 1-2 тижні передує гострий тонзиліт або тонзилофарингіт, особливо на фоні втоми чи переохолодження.
Ревматизм (ревматична гарячка, хвороба Буйо—Сокольського) — системне запальне захворювання сполучної тканини з переважною локалізацією процесу в серцево-судинній системі та частим ураженням інших органів і систем, зокрема суглобів. Розвивається у зв'язку з гострим інфекційним ураженням (бета-гемолітичним стрептококом групи А). На сьогодні виділяють гостру ревматичну гарячку (ГРГ) і хронічну ревматичну хворобу серця (ХРХС), при цьому загальну назву «ревматизм» у сучасній медичній термінології практично вже не використовують.
Клінічні форми та органні ураження[ред. • ред. код]
Найтиповіший прояв ревматизму є ураження серця. Можуть уражатися будь-які оболонки серця та їхні поєднання:
· ревматичний міокардит (найчастіша форма ревмокардиту)
· ендокардит
· ендоміокардит
· перикардит
· панкардит
До ревматичного процесу можуть долучатися
· судини з розвитком ревматичного вісцеріту (особливо нефриту), а також менінгіту, енцефаліту, периферійногоартеріїту (часто судин кінцівок);
· суглоби (ревматичний поліартрит);
· шкіра (ревматичні вузлики, кільцева або вузлувата еритема, кропивниця, тощо);
· легені та плевра (ревматична пневмонія, плеврити).
У дітей, особливо у дівчат, ревматизм може перебігати за типом «нервової форми» — малої хореї.
Профілактика ревматизму та його загострень полягає перш за все в укріпленні захисних сил організму (фізкультура, спорт, загартування, тощо). Необхідне покращення житлових умов хворих, зменшення скупчення людей, що попереджує поширення стрептококової інфекції. Слід проводити ретельне адекватне лікування ангін та інших загострень інфекції у носоглоточній ділянці з тривалим застосуванням антибактеріальних засобів. Недолікована ангіна основний фактор виникнення ревматизму. Застосовується річна медикаментозна профілактика загострень ревматизму. При цьому хворому вводять 1 раз на місяць в/м 1 500 000 ОД біциліну-5. Хворим на ревматизм слід уникати перевтоми та переохолоджень, адже є велика ймовірність повторної ревматичної атаки.
