Опыт 3. Изменение электрической проводимости раствора в результате смещения ионного равновесия
Напишите уравнение диссоциации серной кислоты:
H2SO4 _______________
Степень накала лампы 0,02 М раствора серной кислоты ____.
Напишите уравнение диссоциации гидроксида бария:
Ba(OH)2 ____________.
Степень накала лампы 0,02 М раствора гидроксида бария______________________________
При добавлении фенолфталеина к раствору гидроксида бария раствор окрашивается в___________________цвет. При добавлении серной кислоты к гидроксиду бария цвет раствора_______________________, а степень накала лампы_________________________. В момент исчезновения окраски индикатора (в точке эквивалентности) электрическая проводимость раствора_________________________ .
Напишите ионообменную реакцию в молекулярной и ионной формах:
H2SO4 + Ba(OH)2_
_____________________
____________________.
При добавлении к раствору избытка серной кислоты электрическая проводимость раствора_______.
Вывод:(как изменяется электрическая проводимость при связывании ионов)______________________
__________________.
Опыт 4. Влияние одноименного иона на степень диссоциации слабого электролита (смещение равновесия диссоциации)
А. Напишите уравнения диссоциации:
NH4OH ______________
NH4Cl _____________________
КД (NH4OH) = ______________________________.
При добавлении фенолфталеина к раствору аммиака наблюдается _______________________окрашивание. В присутствии хлорида аммония цвет раствора __________________________.
Вывод:(как изменяется степень диссоциации слабого электролита исходя из принципа Ле Шателье и константы диссоциации)__
_______________________________
____________________.
Б. Напишите уравнения диссоциации
CH3COOH ___________
CH3COONa __________
КД (CH3COOH) =
_____________________
При добавлении метилового оранжевого к раствору уксусной кислоты наблюдается _______________окрашивание. В присутствии ацетата натрия цвет раствора ___________________ ___________________.
Вывод:(как изменяется степень диссоциации слабого электролита исходя из принципа Ле Шателье и константы диссоциации)___
__________________.
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РФ
ФГБОУ ВПО «Уфимский государственный нефтяной технический университет»
Кафедра «Прикладная химия и физика»
Дисциплина «Химия»
ОТЧЕТ
по лабораторной работе №___
На тему: «Приготовление водных растворов»
Выполнил
студент группы__________ ______________ И.О. Фамилия
(Подпись, дата)
Принял
преподаватель кафедры ПХиФ ______________ И.О. Фамилия
(Подпись, дата)
Цель работы:
-освоить навыки приготовления растворов заданной концентрации и методики их количественного анализа.
Теоретическая часть
Количественный состав растворов выражается концентрацией. Концентрацией раствора называется___________
_________.
Массовая доля растворённого вещества – ___________
___________________
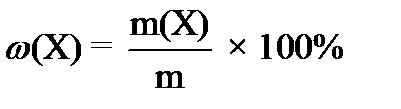 ,
,
где ω (Х) – ____
m(X) –______________ m – ________________.
Молярная концентрация - ________________________
____________________
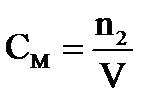
где n2 – _________
V − ________________.
Нормальная концентрация - _____________________
_____________________
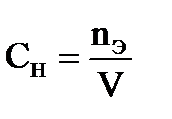
где nЭ – _________
V − ________________.
Моляльная концентрация – _______________________
_____________________
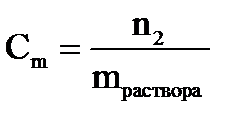
где n2 – __________
mраствора − ____________.
Мольная доля – ______________________________
_________
Экспериментальная часть
