Опыт 1. Приготовление раствора заданной концентрации
Опыт 1.Взаимодействие оксидов с водой
Напишите уравнения реакций (где возможно) взаимодействия оксидов BaO; CuO; FeO; Fe2O3 с водой. Если реакция прошла, определите среду получившегося раствора с помощью универсального индикатора.
1._______________________
2._______________________
3.________________________
4. _________________________
Запишите наблюдения:
1.______________________
2.______________________
3. ______________________
4._______________________
Вывод: (как взаимодействуют оксиды металлов с водой)
__________________________
Опыт 2. Свойства оксидов.
Испытать действие разбавленной соляной кислоты на оксиды из опыта 1.
Что наблюдаете?
1.________
2._________
3._________
4._________
Напишите уравнения реакций
1.____________
2.___________
3.___________
4.____________
Вывод: (как реагируют оксиды металлов с водой)
Опыт 3. Получение оснований
Напишите уравнение реакции взаимодействия натрия с водой
_____________
Что наблюдаете при добавлении фенолфталеина?
_____.
Вывод: (какой способ получения основания использовали)___
_______Опыт 4. Свойства оснований
Реактивы: NaOH; Cu(OH)2; Al(OH)3
В каждую пробирку добавьте воду и фенолфталеин.
Запишите наблюдения.
1.______________________________
2.______________________________
3._____________________________.
Вывод: _____
_________________
Опыт 5. Свойства кислот
Напишите уравнение реакций взаимодействия карбоната кальция с соляной кислотой
_____________
Запишите наблюдения: _________________________.
Вывод: _____
_____________
Опыт 6. Получение и свойства амфотерных гидроксидов
Напишите уравнения реакций получения гидроксида цинка (II) и уравнения, доказывающие его амфотерность:
1.____________
2.____________
3.____________
Запишите наблюдения:
1.____________
2.____________
3.____________
Вывод:(каким способом получали гидроксид и какие свойства амфотерных гидроксидов наблюдали)__________________
Лабораторная работа №2.
Лабораторная работа. Приготовление раствора заданной концентрации.
Цель работы:
-освоить навыки приготовления растворов заданной концентрации и методики их количественного анализа.
Теоретическая часть
Количественный состав растворов выражается концентрацией. Концентрацией раствора называется___
_____________
Массовая доля растворённого вещества
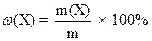 ,
,
где ω (Х) – ____
m(X) –_____________m – _____________
Молярная концентрация -
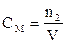
где n2 – _________
V − _________
Молярная концентрация эквивалента (нормальная концентрация) - _____________________
_____________

где nЭ – _________
V − _____________
Экспериментальная часть
Опыт 1. Приготовление раствора заданной концентрации
Приготовьте 250 мл________5________ % раствора хлорида натрия из концентрированного раствора и воды.
Ход работы:
1. Определите ареометром плотность исходного концентрированного раствора:
_____________
2. Определите по таблице процентную концентрацию исходного раствора, отвечающую найденной плотности (если величина процентной концентрации не числится в таблице, то необходимо воспользоваться методом интерполяции):
_______
3. Определите плотность приготовляемого_________% раствора хлорида натрия по таблице:
_____________
4. Вычислите вес приготовляемого раствора крестом:

 ______ ( _____ - 0 )
______ ( _____ - 0 )
 ….
….
 0 _____ ( ______ - ____)
0 _____ ( ______ - ____)
5. Рассчитайте, какое весовое количество исходного раствора хлорида калия нужно для приготовления заданного раствора:
_____________
_____________
6. Пересчитайте полученную величину навески на объем:
_____________
7. Рассчитайте нужный объем воды:
_____________
8. Отмерьте мерным цилиндром вычисленные объёмы концентрированного раствора и воды, слейте их, тщательно перемешайте жидкость и определите ареометром плотность полученного раствора:
_____________
Определите расхождение найденной и заданной плотностей в процентах:
_____________
Вывод:(укажите относительную ошибку эксперимента)____
__________________________
Лабораторная работа №3.
Растворы электролитов.
Цель работы:
-изучить электрическую проводимость растворов электролитов и зависимость её от различных факторов;
- научиться предсказывать направление обменной реакции в растворах электролитов.
Теоретическая часть
Электролиты-_____________
Процесс распада молекул вещества на ионы под действием растворителя называется____
Основания – это электролиты, которые при диссоциации образуют только один вид анионов – ___
NaOH ______
NH4OH _____.
Кислоты – это электролиты, которые при диссоциации образуют только один вид катионов – ___________
HCl _______
HNO3 ______
H2SO4 _____
H3PO4 _____.
Амфотерные гидроксиды диссоциируют в водном растворе как по типу кислоты, так и по типу основания. При их диссоциации одновременно образуются ионы:_____________________
К ним относятся гидроксиды цинка Zn(OH)2, алюминия Al(OH)3, хрома (III) Cr(OH)3, свинца (II) Pb(OH)2 и др..
Например, при диссоциации Zn(OH)2 в водном растворе одновременно присутствуют:
___________H2ZnO2 º Zn(OH)2 _____________.
Средние соли – это электролиты, при диссоциации которых в водных растворах образуются ионы _____________
Na2SO4 _____________________________
Ca3(PO)4 ___________________________.
Кислые соли при растворении в воде образуют ионы_
KHSO3 _____________________________,сложный анион диссоциирует частично:
HSO3- ________________________
Основные соли при диссоциации образуют анионы_______________________и сложные катионы, состоящие и_________:
Al(OH)2Cl ___________________________,
Сложный катион диссоциирует частично:
Al(OH)2+ _____________________________
AlOH2+ _______________________________.
Двойные соли диссоциируют на два катиона__________________________и анион ________________________________:
KAl(SO4)2 _____________________________
Na2NH4PO4 ___________________________.
Сложные соли диссоциируют на катион ________________и анионы_________________
ZnClNO3 = ______________________________
AlSO4Cl = _______________________________.
Степень диссоциации (a)показывает_______________
Степень диссоциации зависит от различных факторов:
_____________
_____________
Для сильных электролитов a > 30%, для средних электролитов a_______, для слабых электролитов a_________.
Константа диссоциации для равновесия, которое устанавливается в растворе слабого электролита:
AmBn = m An+ + n Bm-

___________.
Равновесия в слабых электролитах подчиняются закону _____________________________.
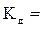
___________.
Между ионами электролитов в растворе действуют силы_____________________________. В связи с этим состояние ионов описывают активностью - условной (эффективной) концентрацией ионов:
а = ______________________________.
