Класс: Лигазы (синтетазы)
К ним относятся ферменты, которые катализируют реакции соединения двух молекул сопряжённые с гидролизом АТФ. Играют ключевую роль в процессе биосинтеза, обеспечивая за счёт энергии освобождающейся при гидролизе АТФ, протекание таких реакций, которые сами по себе были бы невозможны. Примером могут служить аминоацил-тРНК-синтетазы.
Каждый из перечисленных шести классов ферментов также по признаку специфичности разбивают на подклассы иподподклассы,которым присваиваются порядковые номера в соответствие с Международной классификацией.
Например,гидролазы, расщепляющие эфиры карбоновых кислот, относятся к классу 3, подклассу 3.1, то есть гидролазы, действующие на сложноэфирные связи, и подподклассу 3.1.1. (гидролазы эфиров карбоновых кислот). Внутри подподкласса каждый фермент имеет свой порядковый номер. Так липаза, гидролизующая жиры (триацилглицерины), имеет номер 3.1.1.3.
Номенклатура ферментов
Для ферментов, как и многих органических веществ употребляется несколько типов наименований: тривиальные, рациональные и системные.
Тривиальные названия давали ферментам первооткрыватели, например, пепсин, трипсин и др. Согласно рациональной номенклатуре, простой фермент называют исходя из названия субстрата с добавлением окончания –аза (амилаза, уреаза и др.).
По системной номенклатуре, утвержденной в 1961 г., называние фермента складывается из научного названия субстрата, типа катализирующей реакции и окончания -аза.
Например, фермент уреаза, осуществляющий гидролиз мочевины (карбамида),
называют 
 карбамидамидогидролазой
карбамидамидогидролазой
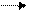 H2N-C-NH2 + HOH 2NH3 + CO2
H2N-C-NH2 + HOH 2NH3 + CO2
║
O
Если в реакции участвуют донор и акцептор какой-либо группы, например аминогруппы -NH2, то называю сначала донор, затем акцептор, тип каталитической реакции и добавляется –аза.
Например, фермент катализирующий реакция переаминирования глутаминовой и пировиноградной кислот, называется глутаматпируватаминотрансфераза:
COOH COOH COOH COOH
 |  | ||||||
 |  | ||||||
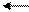
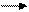 CH-NH2 + C=O C=O + CH-NH2 -
CH-NH2 + C=O C=O + CH-NH2 -
 |  |  | |||||
 | |||||||
|
|
|
 |
|
В биохимии часто вместо полного названия кислот используют названия анионов этих кислот (лактат – анион молочной кислоты, , глутамат – глутаминовой, , пируват - пировиноградной).
Как было показано выше, действие сложных ферментов обеспечивается за счёт кофакторов.
КОФАКТОРЫ
Различают две группы кофакторов – неорганические и органические.К первым относятся ионы металлов (Mg+2, Mn+2, Ca+2), а также некоторые неорганические анилоны (Cl-). Ионы двухвалентных металлов могут быть очень прочно связаны с белковой молекулой, выполняя роль простетической группы.
Органические кофакторы называются коферментами.Они, как правило, представляют собой небелковые вещества. Большинство коферментов не синтезируются в организме млекопитающих, и должны поступать с растительной пищей. Однако в организм поступают не сами коферменты, а их предшественники – витамины, являющиеся незаменимыми пищевыми факторами, которые в клетке модифицируются.
Витамины представляют собой очень разную в химическом отношении группу органических соединений, поэтому с точки зрения химической структуры им нельзя дать общего определения. Единственная классификация витаминов основана на их отношению к воде
Известно 13 витаминов:
ВОДОРАСТВОРИМЫЕ
| ВИТАМИНЫ | КОФЕРМЕНТЫ |
| Тиамин (В1) | Тиаминпирофосфат |
| Рибофлавин (В2) | Флавинмононуклеотид (флавиндинуклеотид) |
| Никотиновая кислота (В5) | Никотинамидадениннуклеотид |
| Пантотеновая кислота (В3) | Коэнзим (кофермент А) |
| Пиридоксин (В6) | Пиридоксальфосфат |
| Биотин Н | Биоцитин |
| Аскорбиновая кислота | Не известно |
ЖИРОРАСТВОРИМЫЕ
| ВИТАМИНЫ | КОФЕРМЕНТЫ |
| Витамин А | Ретинол |
| Витамин Д | Не известно |
| Витамин Е | Не известно |
| Витамин К | Не известно |
Общим для всех витаминов является их абсолютная необходимость для организмов в качестве составной части пищи дополнительно к белкам, жирам, углеводам и минеральным веществам. Поскольку они не синтезируются гетеротрофными организмами, то их недостаток сопровождается возникновением патологических явлений. В количественном отношении потребность в витаминах ничтожна: к 66 граммам сухих питательных веществ нужно 0,1-0,2 грамма витаминов. Отсюда ясно, что витамины в организме выполняют каталитические функции. Во многих случаях они являются составными частями ферментов, необходимыми для их функционирования.
К числу реакций, требующих участия коферментов, относятся окислительно-восстановительные реакции, реакции переноса групп, изомеризации, а также реакции, катализируемые лигазами (лигазозависимые). Без участия коферментов протекают реакции расщепления, например гидролитические реакции, катализируемые пищеварительными ферментами.
Ниже приведены важнейшие органические коферменты, их активные группы, тип реакции, в которой участвует кофермент, а также витамины, входящие в их состав.
