Уравнению Михаэлиса-Ментен соответствует формула
-v=k. CA.CB
-v= A. e-E/RT
-v=k.C2
+ 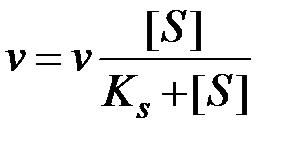
#
Укажите неверное утверждение. Катализаторы-
-обладают специфической избирательностью
-способны снижать энергию активации
-способны изменять скорость реакции
+способны изменяться в конце реакции
#
Период полупревращения рассчитывают по формуле
-∆τ=∆c/∆v
+τ=ln2/k
-τ=H/U
-τ=2,3 lg2 k
#
Укажите наиболее правильное определение «катализаторами называют вещества, которые
+ускоряют протекание химической реакции
-замедляют скорость реакции
-изменяют скорость термодинамически возможной реакции
-снижают энергию активации
-остаются неизменными в конце реакции
#
Приведенная графическая зависимость соответствует
| τ |
| С |
-изменению концентрации исходного вещества с течением времени
+изменению концентрации продукта реакции с течением времени
-реакции первого порядка
-реакции нулевого порядка
#
Приведенная графическая зависимость соответствует
| τ |
| С |
+изменению концентрации исходного вещества с течением времени
-изменению концентрации продукта реакции с течением времени
-реакции нулевого порядка
-реакции второго порядка
#
Протекание простой химической реакции:
2СО(Г)+ О2(Г) → 2СО2 (Г)
описывается следующим кинетическим уравнением:
-V= k·C(CO)
+V = kC2 (CO)•C(O2)
-V = к С2(СО)
-V = к С (СО)• С(O2)
#
Простая реакция Ств + СО2 г → 2СО
описывается следующим кинетическим уравнением:
-V= k (CO2)
-V = kC2 (CO)
-V = kC(C)•C(CO2)
-V = kC(C)•C(CO2)C2(CO)
#
Как изменится скорость прямой реакции, если
концентрацию SO2 увеличить в 3 раза? 2SO2 + О2 → 2SO3
-увеличится в 3 раза
-увеличится в 27 раз
+увеличится в 9 раз
-уменьшится в 3 раза.
#
Биологическими катализаторами являются:
-аминокислоты
-полисахариды
+ферменты
-углеводы
#
Ферменты-катализаторы это:
-микроорганизмы
+белки
-неорганические соединения;
-плесень
-амины
#
Выберите неверное утверждение:
-ферменты-это белки
-ферменты-это биологические катализаторы
+ферменты могут катализировать любую реакцию
-пепсин-это фермент
-уреаза-это фермент
#
Как изменится скорость химического взаимодействия 2Н2 + О2, если концентрацию водорода повысить в 2 раза?
-увеличится в 2 раза
-увеличится в 16 раз
-уменьшится в 4 раза
+увеличится в 4 раза.
#
Функция ферментов в живом организме заключается в:
-транспорте оксигенов
+катализе биохимических реакций
-обеспечении иммунитета
-обеспечении энергией
-замедлении биохимических реакций
Химическое равновесие
#
При установлении в системе состояния химического равновесия
-все исходные вещества превращаются в продукты
-протекает только прямая реакция
-протекает только обратная реакция
+прямая и обратная реакции протекают с одинаковой скоростью
#
Направление смещения химического равновесия при изменении внешних условий определяется
-правилом Зайцева
-принципом Паули
+принципом Ле Шателье
-правилом Хунда
#
При повышении температуры положение химического равновесия смещается в сторону реакции, протекающей
-с выделением теплоты
+с поглощением теплоты
-с уменьшением объема
-с увеличением объема
#
При понижении давления положение химического равновесия смещается в сторону
-экзотермической реакции
-эндотермической реакции
-реакции, протекающей с уменьшением объема
+реакции, протекающей с увеличением объема
#
Положение химического равновесия в эндотермической реакции 2HBr(г)→H2(г)+Br2(г) сместится вправо при повышении
-давления
+концентрации HBr
-концентрации H2
-концентрации Br2
#
Положение химического равновесия в экзотермической реакции
2CO(г) + O2(г) → 2CO2(г) сместится влево при
+понижении давления
-повышении давления
-выводе углекислого газа из реакционной смеси
-повышении концентрации кислорода в газовой смеси
#
Реакция, для которой при повышении давления положение равновесия смещается вправо
-2HBr(г) → H2(г) + Br2(г)
+3H2(г) + N2(г) → 2NH3(г)
-2HCl(г) → H2(г) + Cl2(г)
-N2(г) + O2(г) → 2NO(г)
#
Реакции, положение равновесия в которых смещается при повышении давления вправо
-2HBr(г) → H2(г) + Br2(г)
-N2(г) + O2(г) → 2NO(г)
-2HCl(г) → H2(г) + Cl2(г)
+2NO(г) + O2(г) → 2NO2(г)
#
Введение катализатора в равновесную систему
-смещает равновесие в сторону экзотермической реакции
-смещает равновесие в сторону эндотермической реакции
-смещает равновесие в сторону увеличения количества газообразных веществ
+не оказывает влияния на положение системы, находящейся в состоянии химического равновесия
#
Понижение температуры будет смещать положение равновесия в том же направлении, что и повышение давления, для реакций
-CO(г) + H2O(г) → CO2(г) + H2(г) (эндотермический процесс)
+2SO2(г) + O2(г) → 2SO3(г) (экзотермический процесс)
-N2(г) + O2(г) → 2 NO(г) (эндотермический процесс)
-3O2(г) →2O3(г) (эндотермический процесс)
#
Какие факторы способствуют смещению равновесия вправо в системе
СаСО3 (ТВ) ↔ СаО + СО2 (∆Н>0)?
+повышение температуры
-катализаторы
-повышение давления
-увеличение концентрация СО#
#
Определите знак изменения ∆Н прямой реакции: 2Н2О ↔2Н2 + О2,
если при повышении температуры равновесие сместится вправо.
-∆Н = 0
-ΔН < 0
+ΔН > 0
#
В какую сторону сместится равновесие химической реакции: N2 (Г) + О2 (Г) ↔ 2NO, если увеличить давление
-в сторону прямой реакции
-в сторону обратной реакции
+смещения равновесия не произойдет.
#
Какое воздействие на систему 4НС1 + О2↔ 2С12 + 2Н2О (∆Н<0)
приведет к смещению равновесия влево
-увеличение концентрации О2
-увеличение давления
+увеличение концентрации С12
-уменьшение температуры.
#
Какой из указанных факторов вызовет в системе С + О2↔ СО2( ΔН <О)
смещение равновесия вправо
+уменьшение концентрации СО2
-увеличение концентрации СО2
-увеличение температуры
-увеличение давления
#
Константа равновесия не зависит от:
-температуры
-природа растворителя
-природы реагентов
+концентрация реагентов
#
Как влияет катализатор на смещение химического равновесия
-усиливает прямую реакцию
+не влияет
-уменьшает прямую реакцию
#
В плазме крови существует равновесие: CO2+H2O«H2CO3 .Как изменится концентрация угольной кислоты при насыщении крови в капиллярах тканей углекислым газом
-уменьшается
-не изменяется
+увеличивается
#
Образование почечных камней происходит при нарушении в системе, контролирующей содержание Са2+ и Мg2+ в биологических жидкостях. Это приводит к смещению равновесия Ca3(PO-2(ТВ) «3Сa2+(p-p) +2PO43- Укажите, в каком направлении смещается равновесие при введении в систему хлорида кальция
-не сместится
+влево
-вправо
#
При понижении давления равновесие смещается в сторону:
-экзотермической реакции
-эндотермической реакции
+увеличения числа молекул
-уменьшения числа молекул
