Раздел 1. Теоретическая часть
Новосибирск - 2015
Содержание
Введение…………………………………………………………………………...3
Раздел 1. Теоретическая часть…………………………………………….….4
Раздел 2. Расчет дефлаграционного и детонационного горения газовоздушных смесей....................................................................................13
Заключение……………………………………………………………………….18
Список литературы. ……………………………………………………………..1
Введение
Горение – сложный физико-химический процесс превращения компонентов горючей смеси в продукты сгорания с выделением теплового излучения, света и лучистой энергии.
Газовоздушная смесь (ГВС) – смесь горючего газа с воздухом, в которой содержание горючего газа соответствует концентрационному пределу распространения пламени, т.е. находится в интервале от НКПР (нижнего концентрационного предела распространения пламени) до ВКПР (верхнего концентрационного предела распространения пламени).
Газовоздушные смеси образуются на ряде производств в нормальных или аварийных условиях и могут стать источником очень мощных взрывов. Наиболее опасны взрывы смесей с воздухом углеводородных газов (метана, пропана, бутилена, бутана, этилена и др.), а также паров воспламеняющихся жидкостей. Взрывы ГВС могут происходить во внутренних полостях оборудования и трубопроводов, в помещениях (зданиях) в результате утечки газа, в емкостях для хранения и транспортировки взрыво- и пожароопасных веществ (резервуарах, газгольдерах, цистернах, грузовых отсеках танкеров) или на открытом пространстве при разрушении газопроводов, разливе и испарении жидкостей. Взрывы горючих газов с воздухом с тяжелыми последствиями происходят на шахтах.
Дефлаграционное горение – это такой режим горения, при котором пламя распространяется с дозвуковой скоростью. При детонации пламя распространяется со сверхзвуковой скоростью, например, в воздухе – со скоростью более 300 м/с.
Для дефлаграционного горения характерна передача тепла от слоя к слою, а пламя, возникающее в нагретой с активными радикалами и продуктами реакции смеси, перемещается в направлении исходной горючей смеси. Это объясняется тем, что пламя выделяет непрерывный поток тепла и химически активных частиц, в результате чего фронт пламени перемещается в сторону горючей смеси.
Раздел 1. Теоретическая часть
Суммарная протяженность магистральных продуктопроводов и газопроводов в России составляет более 130 тыс. километров. При аварийной разгерметизации отдельных их участков последствия могут быть очень трагичными.
В ночь с 3 на 4 июня 1989 г. на перегоне между станциями Казаяк и Улу-Теляк, на 1710 километре Куйбышевской железной дороги оказались два поезда с 1284 пассажирами, которые пострадали от взрыва газовоздушной смеси, образовавшейся при аварийной разгерметизации магистрального продуктопровода. На месте аварии было найдено 258 погибших. На 250 га образовались сплошные завалы леса.
Горение - быстро протекающая химическая реакция (чаще всего окисление), сопровождающаяся выделением большого количества теплоты и обычно ярким свечением (пламенем).
Для горения необходимо наличие 3-х факторов:
1) окислителя (обычно О2, также Сl, F, Br, I, NOX)
2) горючего вещества
3) источника загорания (т.е. начало импульса).
В зависимости от свойств и состава горючего вещества различают:
А. Гомогенное горение(одинаковый агрегатный состав, например, газы)
Б. Гетерогенное горение (например, твердое вещество и жидкость).
В зависимости от скорости распространения пламениразличают:
А. Дефлаграционное (свойственно пожарам)~h 10 м/с
Б. Взрывное ~h×100 м/с
В. Детонационное ~ 1000 м/с ¸ 5000 м/с
В зависимости от условий образования горючей смеси:
Диффузионное горение - характеризуется тем, что образование горючей смеси происходит в процессе горения в результате диффузии кислорода в зону горения. Например, горение жидкости с открытой поверхности или газов, выходящих через неплотности оборудования
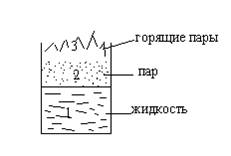
Дефлаграционное горение - это диффузионное горение.
Кинетическое горение соответствует взрывному горению. В этом случае горючее вещество и кислород поступают в зону горения предварительно смешанными. Определяющим фактором является скорость химической реакции окисления между окислителем и горючем веществе, происходящей во фронте пламени. Если процесс кинетического горения происходит в замкнутом объеме, то давление в этом объеме повышается, температура продуктов горения увеличивается.
По соотношению горючего и окислителя выделяют:
А. Горение бедных горючих смесей (в субъекте - окислитель, горение лимитируется соединением горючего компонента).
Б. Горение богатых горючих смесей - соответственно наоборот - горючее лимитирует содержание окислителя (содержит горбчего выше стеклометрического соотношения компонентов).
Возникновение горения связано с обязательным самоускорением реакции. Существует 3 вида самоускорения:
1) тепловой: при условии аккумуляции теплоты в системе повышается температура, что приводит к ускорению химических реакций;
2) цепной: связан с катализом химических превращений промежуточными продуктами реакций, обладает особой химической активностью (активные центры). (т.е. химический процесс происходит не путем непосредственного взаимодействия исходных молекул, а с помощью осколков, образующихся при распаде этих молекул).
Реальные процессы горения обычно осуществляются по комбинированному цепочно-тепловому механизму.
Газовоздушные смеси образуются на ряде производств в нормальных или аварийных условиях и могут стать источником очень мощных взрывов. Наиболее опасны взрывы смесей с воздухом углеводородных газов, а также паров воспламеняющихся жидкостей.
Взрывы ГВС могут происходить во внутренних полостях оборудования и трубопроводов, в помещениях в результате утечки газа, в емкостях для хранения и транспортировки взрыво- и пожароопасных веществ (резервуарах, газгольдерах, цистернах, грузовых отсеках танкеров) или на открытом пространстве при разрушении газопроводов, разливе и испарении жидкостей. Взрывы горючих газов с воздухом с тяжелыми последствиями происходят на шахтах.
Вероятность взрыва ГВС и его опасность определяются:
– пределами взрывной концентрации паров жидкостей и газов в процентах к объему ГВС, например, пропан 3–7%; пропилен 3,5–8,5%; этан 4,0–9,2%;
– температурой воспламенения – нижним пределом температуры, при которой возможно их воспламенение от постороннего источника зажигания;
– плотностью паров и газов по отношению к плотности воздуха;
– температурой самовоспламенения;
– минимальной энергией зажигания или эквивалентом критической энергии электрической искры, необходимой для инициирования детонации.
Воспламенение облака ГВС происходит при наличии источника зажигания. Первоначально скорость распространения пламени относительно невелика и составляет для большинства углеводородных газов 0,32–0,40 м/с. При столь малых скоростях горения образования детонационной волны в ВВ не происходит. Однако в реальных условиях на процесс горения оказывает влияние множество факторов, вызывающих турбулизацию фронта пламени и ускорение его распространения.
Применительно к случайным промышленным взрывам при достижении скоростей распространения пламени несколько метров в секунду возникает дефлаграционное горение, при котором генерируются взрывные волны с максимальным разрушающим избыточным давлением 20–100 кПа. Продолжительность горения до достижения взрывного режима для газов составляет около 0,1–0,2 с. При дальнейшем ускорении горения дефлаграционые процессы могут перерасти в детонационные, скорость распространения которых значительно превышает скорость звука в воздухе и достигает 1–5 км/с.
При больших объемах горючих газовых смесей, наличии источников турбулизации фронта пламени и отражении детонационной волны от препятствий давление за очень короткий промежуток времени достигает высоких значений.
Взрывы газовоздушных смесей (ГВС) часто происходят в жилых домах с газовыми плитами на взрывоопасных производствах, когда нарушается нормальный эксплуатации таких объектов.
В связи с высокой вероятностью аварий со взрывом ГВС преследуется цель объяснить механизм взрывного горения и изложить методику прогнозирования параметров взрывного горения ГВС.
Процесс горения со стремительным высвобождением энергии и образованием при этом избыточного давления (более 5 кПа) называется взрывным горением.
Различают два принципиально разных режима взрывного горения: дефлаграционный и детонационный.
При дефлаграционном горении распространение пламени происходит в слабо возмущенной среде со скоростями значительно ниже скорости звука, давление при этом возрастает незначительно.
При детонационном горении (детонации) распространение пламени происходит со скоростью, близкой к скорости звука или превышающей ее.
Инициирование (зажигание) газовоздушной смеси с образованием очага горения возможно, если будут выполнены следующие условия:
· концентрация горючего газа в газовоздушной смеси должна быть в диапазоне между нижним и верхним концентрационными пределами распространения пламени;
· энергия зажигания от искры, горячей поверхности должна быть не ниже минимальной. Для большинства взрывчатых смесей энергия зажигания не превышает 30 Дж.
Нижний концентрационный предел (Снкп) распространения пламени - это такая концентрация горючего газа в смеси с окислительной средой, ниже которой смесь становится неспособной к распространению пламени.
Верхний концентрационный предел (Свкп) распространения пламени - это такая концентрация горючего в смеси с окислительной средой, выше которой смесь становится неспособной к распространению пламени.
Минимальная энергия инициирования (зажигания) (Эи) - наименьшее значение энергии электрического разряда, способное воспламенить смесь стехиометрического состава.
Концентрация газа стехиометрического состава (Ссх) - концентрация горючего газа в смеси с окислительной средой, при которой обеспечивается полное без остатка химическое взаимодействие горючего и окислителя смеси.
При сгорании газовоздушной смеси стехиометрического состава образуются только конечные продукты реакции горения и выделившаяся теплота их сгорания не расходуется на нагревание несгоревших окислителя или горючего - последних не образуется. По этой причине продукты сгорания нагреваются до максимальной температуры.
В случае дефлаграционного горения такой смеси в замкнутом герметичном и теплоизолированном объеме образуются максимальные температура и давление. Величина максимального давления является характеристикой соответствующей газовоздушной смеси.
Режим дефлаграционного горения может переходить в режим детонационного горения (при быстром росте скорости распространения пламени). Такому переходу способствует турбулизация процесса горения при встрече фронта пламени с препятствиями. При этом поверхность фронта пламени становится неровной, а толщина пламени увеличивается - все это вызывает рост скорости распространения пламени.
В режиме детонационного горения нагрузки значительно возрастают. Поэтому режим детонационного горения принят за расчетный случай для прогнозирования инженерной обстановки при авариях со взрывом.
К основным факторам, влияющим на параметры взрыва, относят: массу и тип взрывоопасного вещества, его параметры и условия хранения или использования в технологическом процессе, место возникновения взрыва, объемно-планировочные решения сооружений в месте взрыва.
Взрывы на промышленных предприятиях и базах хранения можно разделить на две группы - в открытом пространстве и производственных помещениях.
В открытом пространстве на промышленных предприятиях и базах хранения возможны взрывы газовоздушных смесей (ГВС), образующихся при разрушении резервуаров со сжатыми и сжиженными под давлением или охлаждением (в изотермических резервуарах) газами, а также при аварийном разливе легковоспламеняющихся жидкостей.
В производственных помещениях, наряду со взрывом ГВС, возможны также взрывы пылевоздушных смесей (ПВС), образующихся при работе технологических установок.
При воспламенении ГВС в “ точке-сфере ” теплота сгорания повышает параметры сгоревшей части ГВС. Горящий слой передает теплоту прилегающим слоям сферы, вызывая их последовательное воспламенение. В результате горение распространяется от слоя к слою во всем объеме ГВС и воспринимается как распространение сферообразного пламени от центра к внешней поверхности ГВС. Распространение пламени таким способом называется тепловым. В неразогретом и спокойном состоянии ГВС горение протекает в очень тонком слое (доли миллиметра), называемом пламенем. В первые моменты пламя представляет сферу, которая увеличивается во времени. Величина скорости распространения пламени в ГВС в неразогретом и спокойном состоянии является характеристикой ГВС. Эта скорость называется нормальной скоростью распространения пламени. Для большинства ГВС нормальная скорость распространения пламени лежит в области от 0.3 до 1.5 м/с.
При составлении расчетной схемы (рис. 1) для определения параметров горения ГВС в замкнутом объеме принимаются следующие допущения: во всем объеме помещения горючий газ и воздух полностью перемешаны с образованием смеси стехиометрического состава; точечный источник инициирования расположен в центре помещения, а энергия зажигания и термодинамические параметры обеспечивают режим дефлаграционного горения смеси; помещение абсолютно герметично, потери теплоты отсутствуют.
| Начальное состояние “0“ |
| Конечное состояние “1“ | |
| V0, n0, р0, T0, n0 ( ГВС: Мо = Мг+Мв ) Газовоздушная смесь стехиометрического состава | V1, n1, p1, T1, n1 V0=V1, М0=М1 Продукты сгорания и азот воздуха М1=Мг+Мв |
Рис. 1. Схема для оценки параметров квазистатического процесса горения ГВС в замкнутом теплоизолированном объеме:
V0 - объем ГВС; р0,n0,T0,n0 и р1,n0,T1,n1 - соответственно, давление, удельный объем, температура и число молей газа в объеме V0 до и после реакции горения; МГ, МВ - соответственно масса газа и воздуха
В термодинамическом процессе без потерь теплоты, но с выделением теплоты при сгорании газа и возможным изменением количества молей газа в процессе реакции горения, изменение конечного давления (оно же и максимальное давление горения ГВС) будет пропорционально изменению температуры и количества молей газа, то есть:
pмах=p1=p0 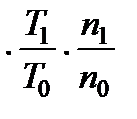 (1)
(1)
Значения n1 и n0 определяются из уравнения химической реакции.
Температура продуктов сгорания определяется в зависимости от удельной теплоты сгорания газа и средней теплоемкости продуктов сгорания при адиабатном их расширении.
Масса горючего газа в объеме V0 равна:
МГ= 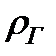 VГ=
VГ= 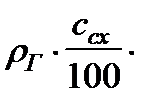 V0, кг, (2)
V0, кг, (2)
где 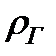 - плотность горючего газа, кг/м3;
- плотность горючего газа, кг/м3;
cсх – стехиометрическая концентрация, % об.
Теплота, выделившаяся в объеме V0 :
Q=Q 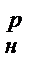 МГ= Q
МГ= Q 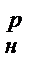
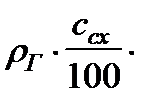 V0, кДж, (3)
V0, кДж, (3)
где Q 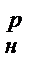 - удельная теплота сгорания горючего газа, кДж/кг.
- удельная теплота сгорания горючего газа, кДж/кг.
Увеличение температуры газов при известных теплоемкостях продуктов сгорания определится из соотношения:
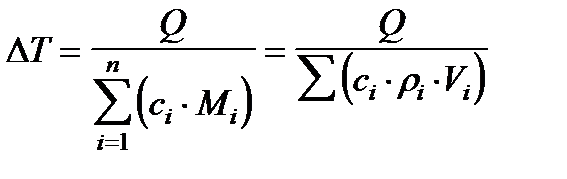 , К , (4)
, К , (4)
где: 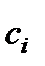 – удельная теплоемкость i-го газа в продуктах сгорания (количество газов – “n”) , кДж/(кг· К);
– удельная теплоемкость i-го газа в продуктах сгорания (количество газов – “n”) , кДж/(кг· К);
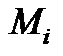 – масса i-го газа в объеме V0 , кг;
– масса i-го газа в объеме V0 , кг;
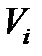 – объем i-го газа в объеме V0 продуктов сгорания, м3.
– объем i-го газа в объеме V0 продуктов сгорания, м3.
Для практических расчетов можно пренебречь различием в физических свойствах горючего газа и воздуха, поскольку содержание воздуха в ГВС превышает содержание газа в несколько раз. Пренебрегая изменением молекулярного состава (n1=n0) в процессе горения и принимая в качестве рабочего тела воздух, приходим к упрощенной формуле для определения увеличения температуры газов при реакции горения:
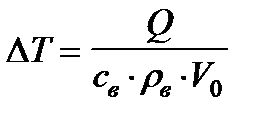 , К , (5)
, К , (5)
где 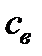 – удельная теплоемкость воздуха, кДж/(кг К);
– удельная теплоемкость воздуха, кДж/(кг К);
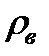 – плотность воздуха в состоянии “0” , кг/м3.
– плотность воздуха в состоянии “0” , кг/м3.
Подставляя в это уравнение формулу для теплоты горения, получим:
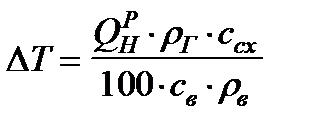 , К , (6)
, К , (6)
Тогда максимальное давление дефлаграционного горения ГВС равно:
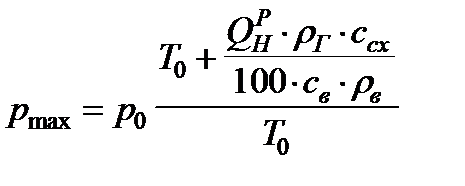 , кПа; (7)
, кПа; (7)
Перепишем последнее уравнение в следующем виде (для определения избыточного давления):
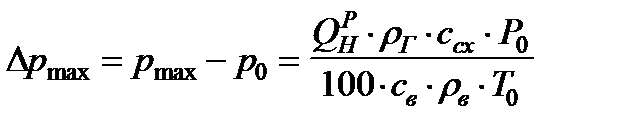 , кПа , (8)
, кПа , (8)
где 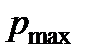 – максимальное давление при дефлаграционном взрыве ГВС, кПа,
– максимальное давление при дефлаграционном взрыве ГВС, кПа,
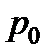 – атмосферное давление, 101.3 кПа,
– атмосферное давление, 101.3 кПа,
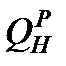 – удельная теплота сгорания горючего газа, кДж/кг,
– удельная теплота сгорания горючего газа, кДж/кг,
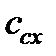 – стехиометрическая концентрация газа в смеси с воздухом, % об.
– стехиометрическая концентрация газа в смеси с воздухом, % об.
Если горючие газы и пары поступают в атмосферу через отверстия (из горелки, трубки, сопла, трещины), то их смеси с воздухом горят устойчивым пламенем.
Горение смесей горючих газов и паров с воздухом в замкнутом объеме (например, в отсеке корабля) происходит в виде химического объемного взрыва.
Для взрыва в замкнутом объеме концентрация смесей должна лежать между НКПВ и ВКПВ. Их называют взрывоопасными. При концентрациях за указанными пределами смеси являются взрывобезопасными. При концентрации, превышающей ВКПВ, смеси считаются пожароопасными, так как на выходе через отверстие из замкнутого отверстия объема в атмосферу они способны гореть диффузионным пламенем. Значения НКПВ и ВКПВ зависят от мощности источника зажигания, наличия в составе смеси инертных газов, температуры и давления смеси.
На рис.2. показано изменение давления при взрыве в зависимости от концентрации смеси. Наибольшее давление соответствует смеси с концентрацией горючего газа, несколько превышающей стехиометрическую, т.е. рассчитанную по уравнению химической реакции. Наибольшее давление взрыва для большинства смесей равно 1,0 МПа, для смеси водорода и ацетилена в воздухе - 1,1 МПа.
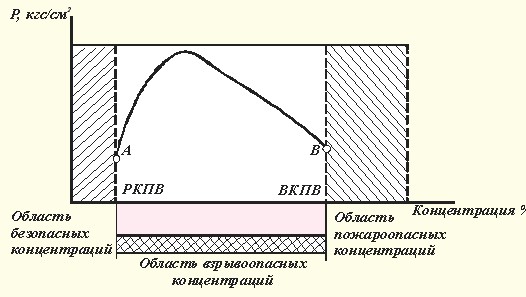
Рис. 2. Характер изменения давления при взрыве
в замкнутом объеме в зависимости от концентрации горючей смеси
Замена воздуха в смеси кислородом резко увеличивает температуру и давление взрыва, так как в этом случае не затрачивается тепло на нагревание негорючего азота, содержащегося в воздухе.
Нормальное горение неустойчиво и в закрытом пространстве склонно к самоускорению. Причиной этому является искривление фронта пламени вследствие трения газа о стенки сосуда и изменения давления в смеси.
Рассмотрим процесс распространения пламени в трубе (рис. 3).

Рис. 3. Схема возникновения взрывного горения.
Сначала у открытого конца трубы пламя распространяется с нормальной скоростью, т.к. продукты горения свободно расширяются и выходят наружу. Давление смеси не изменяется. Длительность равномерного распространения пламени зависит от диаметра трубы, рода горючего и его концентрации.
По мере продвижения фронта пламени внутрь трубы продукты реакции, имея больший объем по сравнению с исходной смесью, не успевают выходить наружу и их давление возрастает. Это давление начинает давить во все стороны, и поэтому впереди фронта пламени исходная смесь начинает двигаться в сторону распространения пламени. Прилегающие к стенкам слои тормозятся. Наибольшую скорость имеет пламя в центре трубы, меньшую – у стенок (изза теплоотвода в них). Поэтому фронт пламени вытягивается в сторону распространения пламени, а поверхность его увеличивается. Пропорционально этому увеличивается количество сгораемой смеси в единицу времени, которое влечет за собой возрастание давления, а то в свою очередь – увеличивает скорость движения газа и т.д. Таким образом, происходит лавинообразное повышение скорости распространения пламени до сотен метров в секунду.
