Количественные характеристики гидролиза
Гидролизу подвергается не вся соль, а лишь её часть, т.е. в растворе устанавливается равновесие между солью и образующими её кислотой и основанием. Поэтому часть вещества, подвергающаяся гидролизу, характеризуется степенью гидролиза. Степень гидролиза зависит от константы равновесия, температуры и концентрации соли, а также от её природы. Природа соли проявляется в величине константы гидролиза соли.
Константа гидролиза соли Кг характеризует способность данной соли подвергаться гидролизу. Чем больше Кг, тем в большей степени протекает гидролиз (при постоянстве Т и концентрации соли).
Константа гидролиза соли, образованной слабой кислотой и сильным основанием, равна:
Кг= 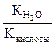 , где Ккислоты – константа диссоциации кислоты. Анализ уравнения показывает, что чем слабее кислота, тем в большей степени подвергаются гидролизу её соли.
, где Ккислоты – константа диссоциации кислоты. Анализ уравнения показывает, что чем слабее кислота, тем в большей степени подвергаются гидролизу её соли.
Константа гидролиза соли, образованной сильной кислотой и слабым основанием, равна:
Кг=  , где Коснования – константа диссоциации основания. Анализ уравнения показывает, что чем слабее основание, тем в большей степени подвергаются гидролизу им образованные соли.
, где Коснования – константа диссоциации основания. Анализ уравнения показывает, что чем слабее основание, тем в большей степени подвергаются гидролизу им образованные соли.
Константа гидролиза соли, образованной слабой кислотой и слабым основанием, равна:
Кг= 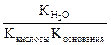 .
.
Управление процессом гидролиза

Гидролиз - обратимый процесс.
Гидролитическое
равновесие можно смещать
с помощью нескольких факторов
 |
Контрольные задания
221.Написать уравнение гидролиза следующих солей: К2S MgCl2. Дать характеристику pH водного раствора данных солей: вычислить константу гидролиза.
222.Написать уравнение гидролиза в ионном виде, дать характеристику pH водного раствора соли AlCl3 .
223.Написать уравнение гидролиза в ионном виде, дать характеристику pH водного раствора солей NH4NO2,Na2SO3 .Вычислить константу гидролиза.
224.Какие из солей подвергаются гидролизу: Li2SO4, CuCl2, KNO3 . Для гидролизующихся солей написать уравнение гидролиза в ионном виде; дать характеристику pH водного раствора солей; вычислить константу гидролиза.
225.Написать уравнение гидролиза в ионном виде, дать характеристику pH водного раствора соли CrCl3 .Вычислить константу гидролиза данной соли
226.Дать характеристику pH водного раствора солей; K2S , Mg(CN)2 , Al2(SO4)3, CuCl2. Написать уравнение гидролиза в ионном виде соли Mg(CN)2,вычислить константу гидролиза.
227.Написать уравнение гидролиза в ионном и молекулярном виде соли CrCl3; вычислить константу гидролиза данной соли
228.Какие из перечисленных солей будут подвергаться гидролизу: NaCN, KNO3, Ca(HCO3)2, HCOOK, BaCl2. Для гидролизующихся солей написать уравнения гидролиза в ионном виде.
229.Написать уравнение гидролиза следующих солей; FeSO4, Na3PO4 , NaClO . Дать характеристику pH водного раствора соли, вычислить константу гидролиза.
230.Написать уравнение гидролиза дать характеристику pH водного раствора соли: ZnBr2 ; вычислить константу гидролиза.
231.Написать уравнение гидролиза следующих солей в ионном виде; Cr2(SO4)3, CuSO4, NaNO2. Дать характеристику pH водного раствора данных солей. Вычислить константу гидролиза.
232.Написать уравнение гидролиза в ионном виде соли CuCl2 ; Дать характеристику pH водного раствора. Вычислить константу гидролиза .
233.Написать уравнение гидролиза в ионном виде соли NiSO4, FeCl2, Na2SO3 . Дать характеристику pH водного раствора данных солей. Вычислить константу гидролиза соли FeCl2 .
234.Какие из солей подвергаются гидролизу KJ, Na3PO4, LiNO3, Pb(NO3)2. Написать уравнение гидролиза в ионном виде для данных солей. Вычислить константу гидролиза для Pb(NO3)2.
235.Написать уравнение гидролиза в ионном виде для соли K3AsO4 . Дать характеристику pH водного раствора. Вычислить константу гидролиза.
236.Какие из солей подвергаются гидролизу KJ, Na3PO4. Написать уравнение гидролиза в ионном виде. Вычислить константу гидролиза 237.Какие из солей подвергаются гидролизу LiNO3, Pb(NO3)2. Написать уравнение гидролиза в ионном Вычислить константу гидролиза.
248. Написать уравнение гидролиза в ионном виде для CuCl2.. Вычислить константу гидролиза.
239. Написать уравнение гидролиза в ионном виде для NaCN. Вычислить константу гидролиза.
240. Написать уравнение гидролиза в ионном виде для HCOOK. Вычислить константу гидролиза.
