Окислительно-восстановительные реакции
Реакции, протекающие с изменением степени окисления атомов, входящих в состав реагирующих веществ, называются окислительно-восстановительными. Степень окисления – это условный заряд атомов в молекуле, вычисленный из предположения, что молекула состоит только из ионов. Степень окисления может иметь нулевое, отрицательное и положительное значение, которое обычно указывают над символом элемента: Na2+O-2, H+N+5O3-2, K+Cl-1. Нулевое значение степени окисления имеют атомы в молекулах простых веществ и атомы в электронейтральном состоянии: Cl02, H02, O02, N02, Al0, Ba0. Отрицательное значение степени окисления имеют атомы, которые приняли электроны:
Cl0 + 1  ® Cl-; S0 + 2
® Cl-; S0 + 2  ® S2-.
® S2-.
Такой процесс называется восстановлением. При этом степень окисления понижается.
Положительное значение степени окисления имеют атомы, отдающие электроны:
Ba0 - 2  ® Ba2+; Р0 - 5
® Ba2+; Р0 - 5  ® Р+5.
® Р+5.
Такой процесс называется окислением. В общем случае степень окисления атома понижается на столько единиц, сколько электронов принимает данный атом:
Mn+7 + 1  ® Mn+6; Fe+3 + 3
® Mn+6; Fe+3 + 3  ® Fe0; S+6 + 2
® Fe0; S+6 + 2  ® S+4.
® S+4.
При отрыве определенного количества электронов степень окисления повышается на соответствующее число единиц:
S-2 - 6  ® S+4; Cl- - 1
® S+4; Cl- - 1  ® Cl0; Mn+2 - 2
® Cl0; Mn+2 - 2  ® Mn+4.
® Mn+4.
У одноатомных ионов степень окисления равна заряду иона: для иона K+ - +1, для иона Ba2+ - +2, для иона S2- - -2 и т.д. Пользуясь этими сведениями, можно вычислять степени окисления атомов в сложных соединениях. При этом следует помнить: алгебраическая сумма степеней окисления атомов в молекуле равна нулю.
Пример 1. Вычислите степень окисления фосфора в молекуле Н3РО4.
Решение. Обозначив степень окисления фосфора через х –Н3+1 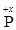 О4-2– и умножив известные нам степени окисления водорода (+1) и кислорода (-2) на число этих атомов в молекуле, составим уравнение
О4-2– и умножив известные нам степени окисления водорода (+1) и кислорода (-2) на число этих атомов в молекуле, составим уравнение
(+1)×3 + х + (-2)×4 = 0.
Отсюда х = +5. Таким образом, степень окисления фосфора равна +5, т.е Н3Р+5О4.
Пример 2. На основании электронных уравнений расставьте коэффициенты в уравнении реакции, идущей по схеме
SnO + KMnO4 + HCl ® SnCl4 + MnCl2 + KCl + H2O.
Укажите окислитель и восстановитель, какое вещество окисляется, какое – восстанавливается.
Решение. 1. Определите, какие атомы в левой и правой частях уравнения меняют степени окисления, подсчитайте и надпишите величины степеней окисления над символом соответствующего атома.
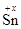 О-2; х + (-2) = 0; х = +2;
О-2; х + (-2) = 0; х = +2; 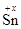 Cl-14; х + (-1)×4 = 0; х = +4;
Cl-14; х + (-1)×4 = 0; х = +4;
К+1 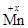 О4-2; +1 + х + (-2)×4 = 0; х = +7;
О4-2; +1 + х + (-2)×4 = 0; х = +7;
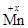 Cl2-1; х + (-1)×2 = 0; х = +2.
Cl2-1; х + (-1)×2 = 0; х = +2.
Таким образом, степени окисления изменяются у атомов Sn и Mn:
Sn+2О + KMn+7O4 + HCl ® Sn+4Cl4 + Mn+2Cl2 + KCl + H2O.
2. Составьте электронные уравнения, т.е. схемы изменения зарядов атомов в левой и правой частях:
Sn+2 - 2  = Sn+4;
= Sn+4;
Mn+7 + 5  = Mn+2.
= Mn+2.
3. Принимая во внимание, что число отданных и принятых электронов должно быть одинаковым, найдите дополнительные множители, поменяв их местами, поставьте за вертикальной чертой и укажите восстановитель и окислитель, процессы окисления и восстановления:
восстановитель Sn+2- 2  = Sn+4 = Sn+4 | 5 процесс окисления; |
окислитель Mn+7 + 5  = Mn+2 = Mn+2 | 2 процесс восстановления. |
4. Дополнительные множители 5 и 2 и будут коэффициенты, стоящие перед формулами соединений олова и марганца. Их перенесите в общее уравнение:
5Sn+2О + 2KMn+7O4 + HCl ® 5Sn+4Cl4 + 2Mn+2Cl2 + KCl + H2O.
5. Коэффициенты перед формулами веществ, атомы которых не меняют свою степень окисления, подберите в следующей последовательности: а) коли-чество атомов металлов (здесь – К); б) количество атомов неметаллов (здесь – Cl); в) количество атомов водорода; г) кислорода.
Если процесс доуравнивания проводился верно, то количество всех атомов в правой и левой частях уравнения будет одинаковым.
Выполненное задание имеет вид:
5Sn+2О + 2KMn+7O4 + 26HCl ® 5Sn+4+ 2Mn+2Cl2 + 2KCl + 13H2O.
восстановитель Sn+2- 2  = Sn+4 = Sn+4 | 5 процесс окисления |
окислитель Mn+7 + 5  = Mn+2 = Mn+2 | 2 процесс восстановления. |
