Полифенолоксидаза (1.14.18.1)
Это фермент известен под различными тривиальными названиями: о - дифенолоксидаза, тирозиназа, фенолаза, катехолаза и др. Фермент может катализировать окисление моно-, ди- и полифенолов.
Типичная реакция, катализируемая полифенолоксидазой, имеет вид:
| Н ½ | Н ½ | ||||
| С // \ | С // \ | ||||
| Н¾ С С ¾ ОН ½ || + 1/2 О2 | полифенолоксидаза ¾¾¾¾¾¾¾¾¾¾¾> | Н¾ С С = О ½ | + Н2О | |||
| Н¾ С С ¾ ОН \\/ С | Н¾ С С = О \\/ С | ||||
| ½ Н | ½ Н |
пирокатехин о - бензохинон
Молекула фермента обладает четвертичной структурой. Полифенолоксидаза - купропротеид. Содержание меди - 0,2 %.
В зависимости от того, из какого источника выделен фермент, способность его к окислению различных фенолов различна. Более того, даже в одном и том же объекте полифенолоксидаза может содержаться в виде различных молекулярных форм, отличающихся по способности к окислению различных фенолов:
монофенол о-дифенол о-хинон
| Н ½ | Н ½ | Н ½ | |
| С // \ | С // \ | С // \ | |
 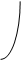  Н¾ С С ¾ ОН ½ || ¾¾¾¾> Н¾ С С ¾ ОН ½ || ¾¾¾¾> | Н¾ С С ¾ ОН ½ || ¾¾¾¾> | Н¾ С С = О + Н2О ½ | | |
| R ¾ С С¾Н \\/ С | R ¾ С С¾ ОН \\/ С | R¾ С С = О \\/ С | |
 ½ Н 1/2О2 ½ Н 1/2О2 | ½ 2Н Н | ½ Н | |
   монофенолазное действие монофенолазное действие | 1/2О2 | катехолазное действие | |
| О2 Н2О | |||
фенолоксидазное действие
При окислении монофенолов фермент действует бифункционально. Во - первых, происходит связывание атома кислорода с ароматическим кольцом с образованием о-дифенола (монофенолазное действие), далее, от о-дифенола отнимаются два атома водорода, которые переносятся на кислород с образованием воды (катехолазное действие, поскольку окисляются производные пирокатехина). Большинство препаратов фенолоксидаз способны окислять дифенолы без сопряжения с окислением монофенолов.
Темноокрашенные продукты (флобафены, меланины), возникающие как следствие действия фермента, образуются в результате чисто химической нонденсации двух образовавшихся хинонов.
С действием этого фермента связано образование темноокрашенных соединений меланинов при окислении кислородом воздуха аминокислоты - тирозина. Потемнение срезов картофеля, яблок, грибов и др. в значительной степени или полностью зависит от действия полифенолоксидазы.
В пищевой промышленности интерес к этому ферменту сосредоточен на предотвращении, рассмотренного нами ферментативного потемнения, которое имеет место при сушке плодов, овощей, при выработке соков, а также при производстве макаронных изделий из муки с повышенной активностью полифенолоксидазы. Эта цель достигается путем тепловой денатурации фермента (бланшировка), добавлением ингибиторов (NаНSО3, SО2, NаСI) или добавлением высоких концентраций аскорбиновой кислоты, которая вызывает восстановление хинонов, тем самым предотвращая их полимеризацию.
Положительная роль фермента отмечается при ферментации чая, табака. Окисление дубильных веществ чая под действием фермента приводит к образованию темноокрашенных ароматических соединений, определяющих цвет и аромат чая.
