Механизм действия буферных систем
Если в организм вводится условно сильная кислота, например, соляная, то при попадании ее в кровь будет происходить реакция нейтрализации с участием бикарбонатов металлов:
NaHCО3 + НСl = NaCI + Н2СО3(1)
Как видно из уравнения (1) сильная кислота (НСl) заменяется эквивалентным количеством слабой кислоты (Н2СО3). В соответствии с законом Оствальда повышение концентрации угольной кислоты понижает, и так небольшую (0,011%), степень ее диссоциации. В результате этого концентрация поступающих в кровь извне, ионов Н+ не достигает значительных величин.
При введении в организм другого «агрессора», например, сильного основания (NaOH), концентрация водородных ионов и рН изменится также незначительно. Щелочь при этом будет реагировать с другим компонентом буфера (Н2СО3) по реакции нейтрализации:
Н 2СО 3 + NaOH = NaHCО3 + Н2О(2)
В результате этого добавленная щелочь заменяется эквивалентным количеством слабоосновной соли, в меньшей степени влияющей на реакцию среды. Анионы HCО3-,образующиеся при диссоциации этой соли, будут оказывать некоторое угнетающее действие на диссоциацию угольной кислоты.
В процессе этой реакции расходуется угольная кислота, и можно было ожидать значительное снижение содержания ионов Н+. Однако, активная кислотность смеси почти не изменяется, т к вместо прореагировавших ионов кислоты (Н + и НСО3-) за счет потенциальной кислотности образуются новые ионы Н + и НСО3-.
Для врача наиболее ценным являются сведения о количественной характеристике всех буферных систем и особенно бикарбонатной.
Расчетное уравнение рН крови по бикарбонатному буферу можно получить из уравнения Гендерсона - Гассельбаха, вывод которого представлен ниже.
РН буферных систем
Согласно закону действующих масс константа диссоциации угольной кислоты будет:
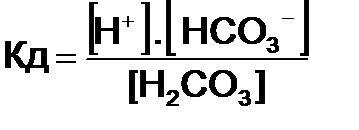 (2)
(2)
откуда
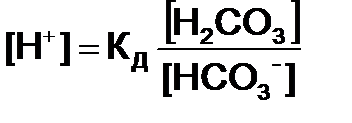 (3)
(3)
Слабая диссоциация угольной кислоты еще в большейстепени подавляется при добавлении хорошо диссоциирующей соли (NaHCO3). Практически концентрация недиссоциированных молекулH2CO3 может быть принята равной общей концентрации кислоты. Так как, соль полностью диссоциирует, можно принять общую концентрацию аниона равной концентрации соли в буферном растворе. Исходя из этого уравнение (3) можно представить в следующем виде:
 (4)
(4)
 (4)
(4)
Логарифмируя уравнение (4) с обратным знаком, получаем основное расчетное уравнение теории буферных растворов - уравнение Гендерсона - Гассельбаха:
рН = -lgК – lg  или
или
рН = рК -lg 
Дляосновного буфера, каким является, например, аммиачный, соответственно будет:
рН = рК -lg 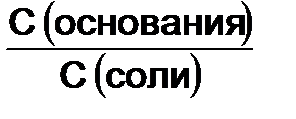
рН = 14 - рК + lg 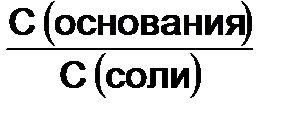
Из приведенных уравнений видно, что рН буферных смесей зависит от константы диссоциации кислоты или основания и от соотношения концентраций компонентов буферных смесей.
Анализ этого уравнения показывает, что рН крови 7,4 по бикарбонатному буферу возможно при соотношении бикарбонатов (NaHCО3) и угольной кислоты (Н2СО3) равном 20. Такое соотношение и соблюдается в крови человека. Так как расчетное значение рН крови по бикарбонатному буферу (7,39) совпадает с экспериментальным (7,4), то, следовательно, величина рН крови может определяться, в основном, бикарбонатной буферной системой.
